
- •Міністерство освіти і науки україни
- •Передмова
- •Загальні методичні вказівки
- •Робоча програма
- •Додаткова література
- •Основні поняття та закони хімії основні поняття та визначення
- •Приклади виконання завдань
- •28 Г n2займають об’єм 22,4 л
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: 27822,2 кДж/кг
- •Відповідь: 25,12 кДж.
- •Можливість та напрямленість перебігу реакцій основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: - 91,016 кДж
- •Відповідь: -131,58 кДж
- •Відповідь: -1235,18 кДж
- •Відповідь: - 35,75 кДж
- •Відповідь: 313,94 кДж
- •230. Користуючись значеннями стандартних теплот утворення та абсолютних стандартних ентропій, обчислити реакції, що відбувається за рівнянням
- •Хімічна кінетика та рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Швидкість реакції зросла у
- •Контрольні завдання
- •Відповідь: 2,6.
- •Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
- •Розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів основні поняття і визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Розчини електролітів основні поняття та визначення
- •Приклади виконання завдань
- •У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ().
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Періодична система елементів д.І.Менделєєва приклади розв’язання задач
- •Контрольні завдання
- •Хімічний зв’язок основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Окиcно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електродні потенціали. Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання. Схема даного гальванічного елемента
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електроліз основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Метали контрольні завдання
- •Неметали контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання.Оскільки твердість води показує число ммоль еквівалентів солей в 1 л її, розрахуємо твердість води за формулою:
- •20 (Мг/ммоль).
- •5 (Ммоль е/л).
- •Приклад 3 Визначити масу фосфату натрію, необхідну для пом’якшення 1м3 води з загальною твердістю 8 ммоль е/л.
- •Контрольні завдання
- •2,3 Ммоль е/л.
- •Відповідь: 8 ммоль е/л
- •Неорганічні в’яжучі речовини основні поняття та визначення
- •Контрольні завдання
- •Елементи органічної хімії. Органічні полімерні матеріали основні поняття та визначення
- •Контрольні завдання
- •Правила техніки безпеки та перша допомога в нещасних випадках
- •Деякі основи та їхні залишки
- •Деякі кислоти та їхні залишки
- •Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
- •Питання для самоперевірки
- •Лабораторна робота № 3 визначення теплових ефектів хімічних реакцій
- •Порядок виконання роботи
- •Хімічна кінетика
- •Хімічна рівновага
- •Лабораторна робота № 6 приготування розчину даної концентрації і встановлення його титру
- •Питання для самоперевірки
- •Лабораторна робота № 7 електролітична дисоціація. Реакції в розчинах електролітів
- •Гідроліз солей
- •Лабораторна робота № 9 електрометричне визначення рН розчинів електролітів
- •Оформлення результатів роботи
- •Питання для самоперевірки
- •Адсорбція
- •Дослід 1. Приготування суспензії крейди у воді.
- •2 Процес окиснення
- •1. Які реакції називаються окисно-відновними?
- •Властивості алюмінію та заліза
- •Лабораторна робота № 16 комплексні сполуки
- •Корозія металів
- •Дослід 2. Електрохімічна корозія оцинкованого і лудженого заліза.
- •Визначення карбонатної твердості води
- •Лабораторна робота № 19 визначення агресивного діоксиду вуглецю
- •Визначення процентного вмісту оксидів кальцію та магнію у вапні
- •Обчислити процентний вміст у вапні за формулою:
- •Кремній та його сполуки
- •Спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Для прискореної форми навчання спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Періодична система хімічних елементів д.І.Менделєєва
- •Деякі одиниці міжнародної системи (сі)
- •Значення деяких фундаментальних фізичних сталих
- •Термодинамічні константи деяких речовин
- •Растворимость солей, кислот и оснований в воде
- •Відносна електронегативність деяких елементів (таблиця полинга)
- •Стандартні потенціали металевих і газових електродів
Хімічний зв’язок основні поняття та визначення
|
Хімічний зв’язок
|
- сукупність взаємодій атомів, що призводять до утворення стійких систем (молекул, комплексів, кристалів та інш.). |
|
Енергія іонізації
|
- кількість енергії, необхідної для відриву від атома найбільш слабко зв’язаного з ним електрона з утворенням позитивно зарядженого іона. |
|
Спорідненість до електрона (ЕС)
|
- кількість енергії, яка виділяється або поглинається під час приєднання одного електрона до нейтрального атома з утворенням негативно зарядженого іона. |
|
Електронегативність
|
-
узагальнююча характеристика елемента,
яка визначається півсумою енергії
іонізації та спорідненості до електрона
|
|
Ковалентний зв’язок
|
- зв’язок, який згідно з теорією валентних зв’язків, утворюється за рахунок перекриття електронних хмар неспарених електронів взаємодіючих атомів з антипаралельними спінами. |
|
Неполярний ковалентний звязок |
- спільна електронна пара в рівній мірі належить взаємодіючим атомам.
|
|
Полярний ковалентний зв’язок
|
- спільна електронна пара зміщена в бік атома з більшою електронегативністю. |
|
Донорно-акцепторний зв’язок
|
- різновид ковалентного зв’язку, утвореного за рахунок неподіленої електронної пари одного атома (донор) та вільної електронної орбіталі іншого атома (акцептор). |
|
Іонний зв’язок
|
- зв’язок, утворений при взаємодії атомів, що дуже відрізняються значеннями електронегативностей, у результаті чого утворюються протилежно заряджені іони, які притягуються один до одного. |
|
Металічний зв’язок
|
- зв’язок, утворений усуспільненими електронами, які переміщаються по всьому об’єму металу. |
Приклади виконання завдань
Приклад 1.
Користуючись даними
таблиці 6 визначити види хімічних
зв’язків у молекулах
![]() .
.
Відповідь.
До складу молекули
![]() входять атоми елементів, відносні
електронегативності яких різко
відрізняються: для натрію 0,9 а для хлору
3,0. Завдяки цьому атом натрію віддає
електрон зовнішнього енергетичного
рівня атому хлору, перетворюючись в
позитивно заряджений іон, а атом хлору
відповідно в негативно заряджений іон.
Між ними виникає електростатична
взаємодія, тобто в молекулі
входять атоми елементів, відносні
електронегативності яких різко
відрізняються: для натрію 0,9 а для хлору
3,0. Завдяки цьому атом натрію віддає
електрон зовнішнього енергетичного
рівня атому хлору, перетворюючись в
позитивно заряджений іон, а атом хлору
відповідно в негативно заряджений іон.
Між ними виникає електростатична
взаємодія, тобто в молекулі![]() реалізується іонний зв’язок.
реалізується іонний зв’язок.
Схематично цей процес можна представити так:
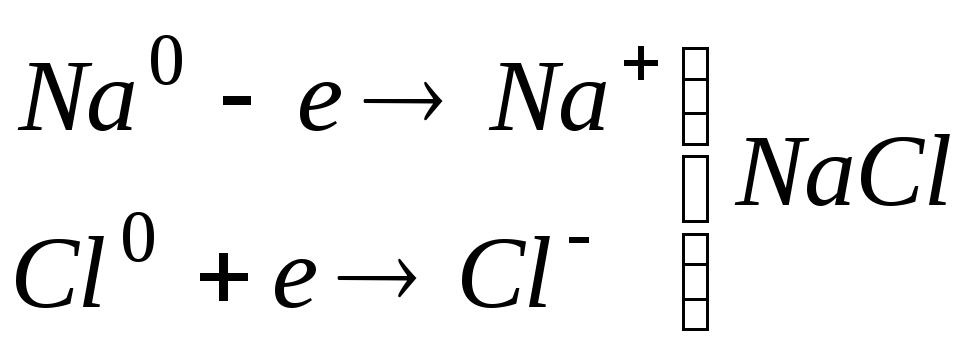
У
молекулі
![]() реалізується ковалентний полярний
зв’язок, оскільки атоми водню і сірки
в незначній мірі відрізняються за
величинами відносних електронегативностей
(ВЕН)
(ВЕНН=2,1;
ВЕНS=2,5).
Спільні електронні пари зміщенні до
атома сірки. У молекулі
реалізується ковалентний полярний
зв’язок, оскільки атоми водню і сірки
в незначній мірі відрізняються за
величинами відносних електронегативностей
(ВЕН)
(ВЕНН=2,1;
ВЕНS=2,5).
Спільні електронні пари зміщенні до
атома сірки. У молекулі
![]() утворюється ковалентний неполярний
зв’язок, оскільки молекула складається
з атомів одного елемента. Схематично
це можна зобразити так:
утворюється ковалентний неполярний
зв’язок, оскільки молекула складається
з атомів одного елемента. Схематично
це можна зобразити так:
![]()
Приклад 2.
У молекулах якої з
наведених сполук:
![]() -ковалентний зв’язок
характеризується найбільшою полярністю?
-ковалентний зв’язок
характеризується найбільшою полярністю?
Розв’язання. Полярність зв’язку між атомами залежить від величин відносних електронегативностей взаємодіючих атомів. Користуючись даними таблиці 6, знаходимо різниці ВЕН: для H-S2,5-2,1=0,4
для H-O 3-2,1=1,4
для HCl3-2,1=0,9
Найбільшою
полярністю характеризується зв’язок
Н-О в
молекулі
![]() .
.
