- •15. Сірковмісні сполуки
- •1. Тіоспирти (тіоли, меркаптани).
- •1.1. Класифікація, номенклатура.
- •2.1. Методи отримання.
- •1.3. Фізичні властивості.
- •1.4. Хімічні властивості.
- •2. Тіоетери (сульфіди).
- •2.1. Класифікація. Номенклатура.
- •2.2. Методи отримання.
- •2.3. Фізичні властивості.
- •2.4. Хімічні властивості.
- •3. Екологічні питання.
15. Сірковмісні сполуки
Серед великої кількості
сірковмісних сполук розглянемо тіоспирти
(![]() )
та тіоетери
(
)
та тіоетери
(![]() ),
які являються тіоаналогами кисневовмісних
сполук, відповідно, спиртів та етерів.
Наявність 3d-атомних орбіталей сульфуру,
на відміну від оксигену, дає змогу
утворюватись іншім сірковмісним сполуки:
сульфоксидам
(
),
які являються тіоаналогами кисневовмісних
сполук, відповідно, спиртів та етерів.
Наявність 3d-атомних орбіталей сульфуру,
на відміну від оксигену, дає змогу
утворюватись іншім сірковмісним сполуки:
сульфоксидам
(![]() )
та сульфонам
(
)
та сульфонам
(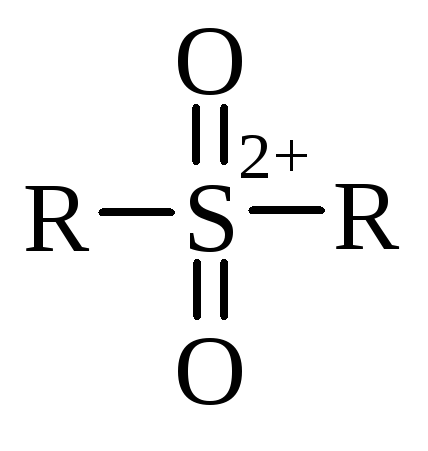 )
з більш високими ступенями окиснення.
)
з більш високими ступенями окиснення.
1. Тіоспирти (тіоли, меркаптани).
Тіоли – похідні сірководню, в молекулі якого атом гідрогену заміщений на вуглеводневий радикал.
1.1. Класифікація, номенклатура.
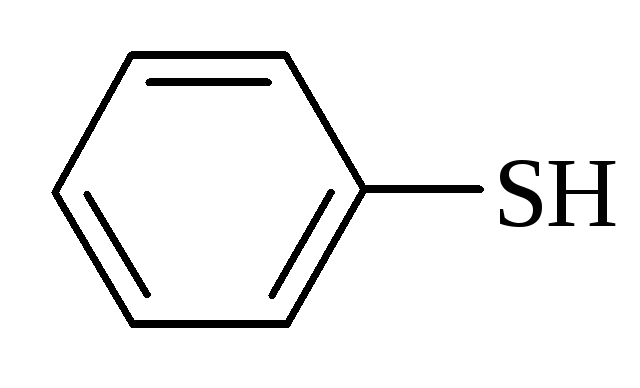
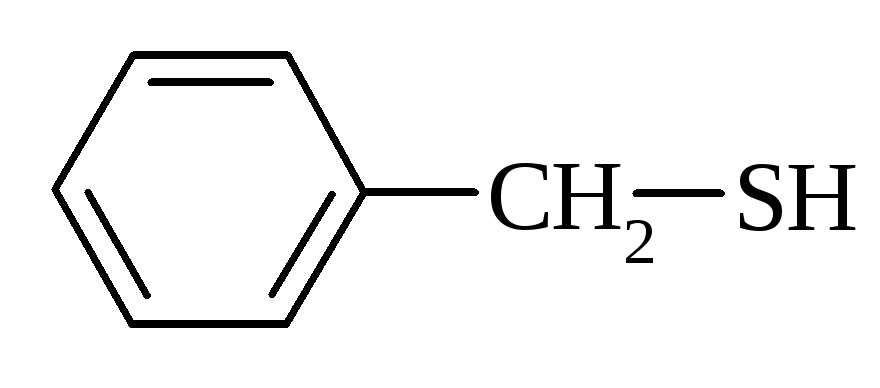
Загальна формула R–SH. В залежності від природи та будови радикалу R тіоли можуть бути, згідно до наведених формул, відповідно, аліфатичними, ароматичними та змішаними:
|
|
– етантіол |
|
– тіофенол |
|
– бензилмеркаптан |
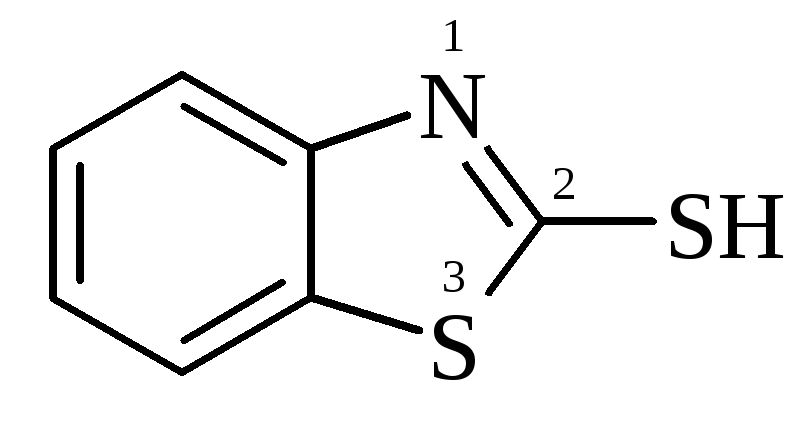
Назва за систематичною номенклатурою: корінний вуглеводень + суфікс -тіол. Якщо SH-група не є гловною, то при її назві застосовують префікс меркапто-:
|
|
2-меркаптобензтіазол (каптакс); |
Назви деяких тіолів та їх фізичні константи приведені у табл. 14.1.
Таблиця 14.1
Назви деяких тіолів та їх фізичні константи.
|
Формула |
Назва |
Тпл., °С |
Ткип., °С |
|
|
метантіол |
-123,1 |
5,9 |
|
|
етантіол |
-144,1 |
37,0 |
|
|
етандітіол |
-41,2 |
146,0 |
|
|
фенілметантіол |
– |
194,0 |
|
|
тіофенол |
– |
169,0 |
2.1. Методи отримання.
Меркаптани отримують взаємодією галогеналканів із сульфідами металів
-
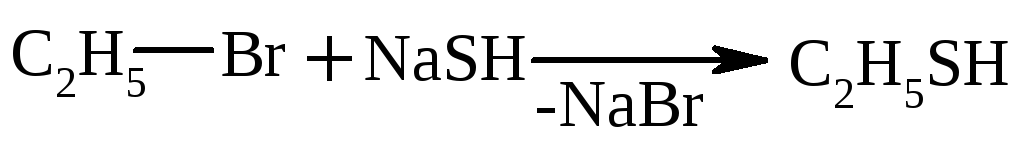
етилмеркаптан (етантіол)
та спиртів із сірководнем:
![]()
або алкенів із сірководнем:
-
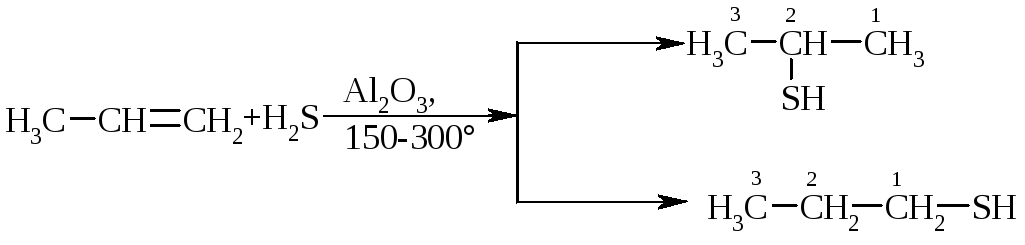
пропантіол-2
(95%)
пропантіол-1
(5%)
Приєднання сірководню проходить по правилу Марковнікова. Побічний продукт пропантіол-1 утворюється за рахунок реакції, що протікає за вільнорадикальним механізмом.
Взаємодією реактивів Гріньяра ароматичного ряду із елементною сіркою отримують арилмеркаптани:
-
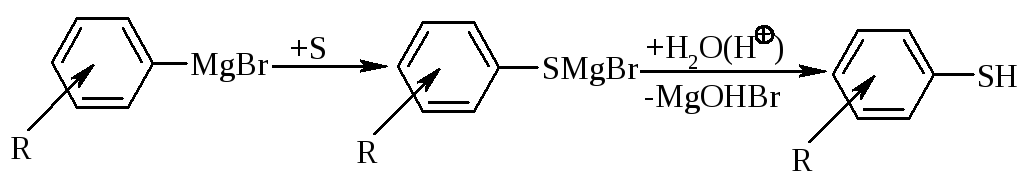
арилмеркаптан
1.3. Фізичні властивості.
За винятком газоподібного метилмеркаптану, інші тіоли – рідини або тверді речовини. Їх температури кипіння вищі ніж у відповідних оксигенпохідних (табл. 14.1). Це пояснюється тим, що атоми сірки, завдяки своїй меншій електронегативності та більшому радіусу, не схильні до утворення водневих зв’язків. І, як наслідок, тіоли є менш розчинними у воді, ніж спирти та феноли. Меркаптани отруйні речовини із надзвичайно неприємним запахом, який помітний дуже у незначних кількостях. Наприклад, гранична кількість для виявлення етилмеркаптану по запаху складає 4,6·10-8 мг.
1.4. Хімічні властивості.
Тіолати (меркаптиди) утворюються при взаємодії лужних металів або лугів із тіолами:
-
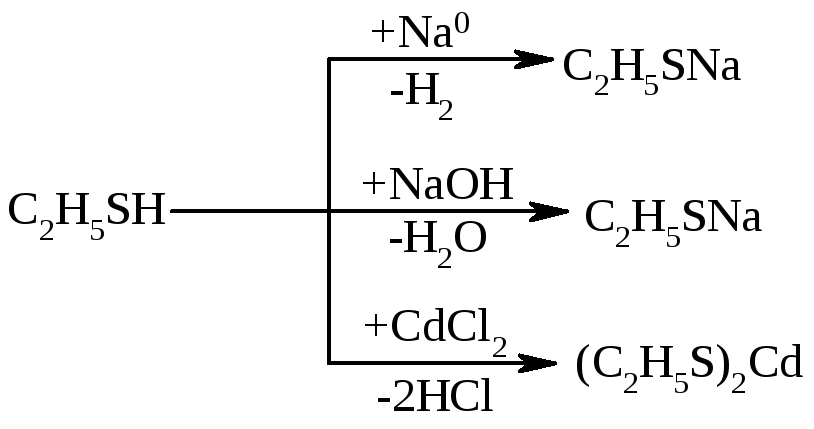
етантіолат натрія
етанмеркаптид натрія
етанмеркаптид кадмія
Взаємодія тіолів з лугами, на відміну від спиртів, вказує на їх більш високі кислотні властивості:
-
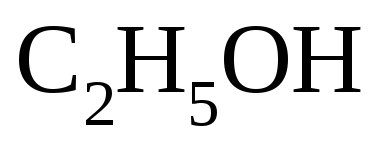
рКа=15,8;

рКа=10,6
Тіоспирти з карбоновими кислотами в присутності сильних кислот (каталізаторів) вступають в реакцію етерифікації:
-

етиловий естер тіолоцтової кислоти
На відміну від спиртів, у яких окиснюється атом карбону, тіоспирти окиснюються по атому сульфуру, і в залежності від сили окисника утворюють різні кінцеві сполуки:
-

диетилдисульфід
етансульфокислота