
Лахтин_Матеориаловедение
.pdf
Сплавы — твердые растворы имеют низкие литейные свойства (плохая жидкотекучесть, склонность к образованию рассеянной пористости и трещинам). Для получения высоких литейных свойств концентрация компонентов в литейных сплавах должна превышать их максимальную растворимость в твердом состоянии (см. рис. 40, б, точка d) и приближаться к эвтектическому составу (точка с). Эвтектические сплавы обладают хорошей жидкотекучестью, и усадка в них проявляется в виде концентрационной раковины.
Сплавы, лежащие левее точки d (предельной растворимости в твердом растворе) и состоящие в основном из α-фазы, пластичны и поэтому хорошо прокатываются, куются, штампуются, прессуются
ит. д. (см. рис. 40, б). Пластичность сильно снижается при появлении в структуре эвтектики. Поэтому в деформируемых сплавах максимум растворимости при эвтектической температуре (см. рис. 40, точка d) является верхним желательным пределом содержания компонентов.
Ликвация по плотности. При кристаллизации сплавов по диаграмме состояния, типа приведенной на рис. 40, нередко можно наблюдать явление, называемое ликвацией по плотности. Например, в сплавах Pb—Sb выделяющиеся в процессе кристаллизации кристаллы а (твердого раствора Sb в РЬ) или B (твердого раствора РЬ в Sb) различаются по плотности от остающейся жидкой части сплава
ивследствие этого либо всплывают кристаллы B и соответственно оседают на дно кристаллы a, либо наоборот. Поэтому в медленно охлажденном доэвтектическом сплаве указанной системы в результате ликвации верхняя часть слитка обогащается сурьмой и. состоит только из эвтектики, а нижняя содержит много избыточных кристаллов α и небольшое количество эвтектики (рис. 41).
61
Чтобы предупредить ликвацию по плотности, сплав быстро охлаждают, а иногда добавляют третий компонент, кристаллизующийся первым в виде разветвленных дендритов, препятствующих расслоению сплава.
Диаграмма состояния сплавов, образующих ограниченные твердые растворы и перитектику. Диаграмма состояния сплавов с перитектикой приведена на рис. 42. Линия tActB на диаграмме соответствует линии ликвидус, а линия tAdetB — линии солидус. Точка d характеризует максимальную растворимость компонента В в А, а точка e — предельную растворимость А в В.
Линия cde называется линией перитектического превращения.
Перитектическое превращение отличается от эвтектического. Если при эвтектическом превращении из жидкой фазы одновременно кристаллизуются две твердые фазы, то при перитектическом превращении кристаллизуется лишь одна фаза, образующаяся за счет ранее выделившейся твердой фазы и жидкой части сплава определенного состава (точка с).
Рассмотрим механизм перитектического превращения. При кристаллизации сплавов, состав которых лежит правее точки d, из жидкого сплава первоначально выделяются кристаллы β- твердого раствора.
По достижении температуры tп в равновесии находится жидкая фаза состава, характеризуемого точкой с, и β-кристаллы состава точки е.
α-кристаллы образуются в результате перитектической реакции, которая сводится к взаимодействию ранее выделившихся кристаллов ββ и жидкой фазы: Жс + βе → αd.
Перитектическая реакция, протекающая при участии трех фаз постоянного состава (Жс, βе и αd), соответствует нонвариантному равновесию (С = 0), т. е. процесс протекает при постоянной температуре.
Для сплавов, концентрация которых лежит в интервале de, соотношение реагирующих фаз характеризуется избыточным количеством β-кристаллов, поэтому в результате перитектического превращения часть фазы останется неизрасходованной:
Жс + βе → αd + βe.
Структура этих сплавов после окончания процесса кристаллизации состоит из перитектической смеси хорошо развитых кристаллов α и β (см. рис. 31, в).
Кристаллизация сплавов, состав которых соответствует линии cd, начинается с выделения из жидкой фазы кристаллов β- твердого раствора. По достижении температуры tп происходит перитектическое превращение:
Жс + βе → Жс + αd.
Вэтих сплавах после перитектического превращения в избытке оказывается жидкая фаза. При дальнейшем понижении темпера-
62

туры из жидкого сплава кристаллизуется α-твердый раствор. После затвердевания сплавы состоят только из кристаллов α- твердого раствора.
В сплавах, расположенных левее точки с, при кристаллизации из жидкой фазы выделяется α-твердый раствор. После затвердевания они состоят только из кристаллов α-твердого раствора. Для этой системы структурный и фазовый состав совпадают.
5. ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ, КОМПОНЕНТЫ КОТОРЫХ ИМЕЮТ ПОЛИМОРФНЫЕ ПРЕВРАЩЕНИЯ
Полиморфные превращения одного или обоих компонентов сплава изменяют его структуру и свойства. Такие превращения происходят во многих промышленных сплавах, например сплавах железа, титана и др.
Диаграмма состояния сплавов, образующих твердые растворы с неограниченной растворимостью, в которых один из компонентов
Аимеет две модификации α и β, представлена на рис. 43, а.
Вслучае, приведенном на рис. 43, а, все сплавы после затвердевания состоят из однородного β-раствора, который является твердым раствором компонентов А (в состоянии, когда он имеет β-модификацию) и В. При понижении температуры β- модификация компонента А превращается в α-модификацию. В связи с этим в области, ограниченной линиями ас и ab, в равновесии находятся две фазы α + β, где α-фаза является твердым раствором компонента В в α-модификации компонента А; β-фаза — твердым раствором В в β-модификации компонента А. Ниже линии ab сплавы состоят только из α-фазы. Кристаллическая решетка α-раствора отлична от решетки β- раствора. На диаграмме (см. рис. 43, а)
63
линия ас при охлаждении соответствует температуре начала, а линия ab — температуре окончания полиморфного α → β- превращения.
При температурах ниже линии ас β-твердый раствор в условиях равновесия становится неустойчивым и в его кристаллах возникают зародыши α-твердого раствора. Развитие превращения β → α возможно только при дальнейшем охлаждении сплава. Образующиеся кристаллы α-твердого раствора при понижении температуры изменяют свой состав по линии ab, а кристаллы β-твердого раствора — по линии ас.
При температурах, отвечающих линии ab, полиморфное β → α- превращение заканчивается; и при более низкой температуре сплавы имеют однофазную структуру α-твердого раствора. В сплавах, находящихся между точками b и с, β → α-превращение при нормальной температуре не заканчивается, и после охлаждения эти сплавы сохраняют двухфазную структуру α + β.
Сплавы, лежащие правее точки с, не претерпевают полиморфного превращения и при всех температурах имеют структуру β-твердого раствора.
Из диаграммы состояния видно, что полиморфное β → α-npeepa- щение при охлаждении в условиях, близких к равновесию, протекает в интервале температур и сопровождается диффузионным перераспределением компонентов между обеими фазами.
Диаграмма состояния сплавов, у которых высокотемпературные модификации компонентов (β) обладают полной взаимной растворимостью, а низкотемпературные (α) — ограниченной, приведена на рис. 43, б. В результате первичной кристаллизации все сплавы этой системы образуют однородный β-твердый раствор.
С понижением температуры β-твердый раствор распадается вследствие ограниченной растворимости компонентов в α- модификации. Линии ас и сb соответствуют температурам начала распада β-твердого раствора. При температурах ниже линии ас в равновесии находятся кристаллы твердых растворов β и α, состав которых определяется линиями ас (β-фаза) и ad (α-фаза).
При температурах ниже линии be в равновесии находятся β- и α'-фазы. Состав β-твердого раствора при понижении температуры изменяется по линии cb, а α'-фазы по линии be. По достижении изотермы dce твердый раствор β, состав которого отвечает точке с, при постоянной температуре распадается (С = 0): βс → αd + αе.
Распад β-раствора на смесь двух фаз α и α' может быть описан аналогично эвтектическому превращению, но в этом случае исходной фазой будет твердый раствор (а не жидкость, как это встречается при эвтектическом превращении). Подобное превращение в отличие от эвтектического называют эвтектоидным, а смесь полученных кристаллов (α + α') — эвтектоидом. Сплавы, расположенные левее точки с, называются
доэвтектоидными; сплав, отвечающий точке с, — эвтектоидным, а
сплавы, лежащие правее точка с, — заэвтектоидными.
64
Линия df указывает на изменение предельной растворимоети компонента В в α-модификации компонента А в зависимости от температуры, а линия ek — компонента А в α-модификации компонента В.
Раепад твердого раствора может проиеходить и в условиях больших степеней переохлаждения. Чем больше етепень переохлаждения, тем меньше будет количество избыточных фаз (α или α') и больше эвтектоида. В области, очерченной линиями b'са' (см. рие. 43, б), избыточные фазы выделяться не будут. В этой области образуется только квазиэвтектоид, который отличается от эвтектоида непостоянством своей концентрации. В доэвтектоидных сплавах квазиэвтектоид обеднен компонентом В относительно равновесного содержания (см. рие. 43, б, точка в), а в заэвтектоид-ных сплавах обогащен компонентом В.
Строение эвтектоида всегда тоньше, чем эвтектики. Чем больше степень переохлаждения β-твердого раствора, тем дисперснее фазы, образующие эвтектоид. Изменяя степень дисперсности фаз в эвтектоиде, можно в широких пределах менять механические и физические свойства сплавов.
При переохлаждении β-твердого раствора до низких температур протекает мартенситное превращение. В результате мартен-ситного превращения, особенно в сталях, сильно повышается твердость. В связи с этим нагрев стали до температур, соответствующих области стабильного β-твердого раствора, и последующее быстрое охлаждение для получения структуры мартенсит также называют закалкой. Распад мартенсита при нагреве называют отпуском.
6. ПОНЯТИЕ О ДИАГРАММАХ СОСТОЯНИЯ ТРОЙНЫХ СПЛАВОВ
Диаграмма состояния тройных сплавов имеет вид трехгранной призмы. Основанием призмы служит равносторонний треугольник, который указывает концентрацию компонентов. Этот треугольник называют
концентрационным.
Компоненты, образующие сплав, указывают в вершинах треугольника, двойные сплавы — на сторонах треугольника, а тройные сплавы — точками внутри треугольника.
Для определения состава тройного сплава используют свойство равностороннего треугольника: если через любую точку внутри треугольника, например, точку Μ (рис. 44), провести прямые, параллельные сторонам, то сумма отрезков а, Ь, с, отсеченных на сторонах, равна стороне треугольника
(а + b + + c = AB = BC = СА).
За 100 % одного из компонентов принимают сторону треугольника. Для определения состава сплава, соответствующего, например, точке М, 1 пользуются отрезками Mh, Mk и Mg, равными соответственно отрезкам Л
а, Ь и с. Концентрации отсчитывают по часовой стрелке. Тогда отрезок а соответствует содержанию компонента А, отрезок b — содержанию компонента В и отрезок с — содержанию компонента С.
Для получения диаграммы состояния тройных сплавов сначала строят (как и для двойных сплавов) кривые охлаждения в координатах температура— время. Эти сплавы отмечают точками в концентрационном треугольнике; из них восстанавливают перпендикуляры, на которых при соответствующих тем-
3 Лахтин |
65 |

пературах откладывают критические точки. Через эти точки проводят поверхности (вместо линий на диаграммах двойных сплавов).
Общий вид тройных диаграмм состояния определяется характером двойных систем, образующих их боковые грани (рис. 45, а) и характеризующих взаимодействие компонентов в разной их комбинации. Тройная диаграмма состояния с неограниченной растворимостью компонентов в жидком и твердом состоянии приведена на рис. 45, а. Начало кристаллизации тройных сплавов соответствует температурам, лежащим на поверхности ликвидус. Окончание кристаллизации тройных α-твердых растворов соответствует температурам, образующим поверхность солидус.
Выше поверхности ликвидус сплавы находятся в жидком состоянии. В интервале температур между поверхностью ликвидус и солидус будет двухфазное состояние Ж + α. При температурах ниже поверхности солидус существует только тройной α- твердый раствор.
На рис. 45, б показана кривая охлаждения для сплава 1. В интервале температур tH — tK число степеней свободы С = 3— 2 + 1 = 2. Следовательно, в двухфазной области тройной системы (между поверхностями ликвидус и солидус) можно одновременно менять и температуру и состав одной из фаз (твердого α или жидкого Ж раствора), не меняя числа фаз в системе.
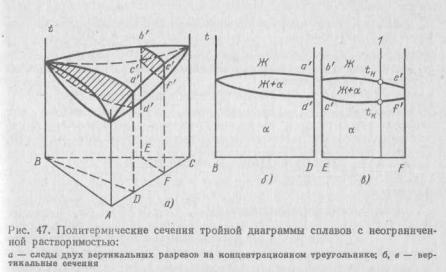
Превращения в тройных сплавах удобнее наблюдать не по пространственной диаграмме, а по сечениям (разрезам) этих диаграмм.
Применяют следующие виды сечения пространственных диаграмм тройных сплавов:
горизонтальные, которые проводят в виде изотермических сечений, указывающих фазовый и структурный составы для всех сплавов при определенной температуре, или в виде проекции отдельных поверхностей и линий на горизонтальную плоскость (концентрационный треугольник);
вертикальные (полиметрические), широко используемые при изучении тройных сплавов.
Горизонтальный разрез тройной диаграммы сплавов — твердых растворов показан на рис. 46, а. Плоскость А'В'С, параллельная плоскости концентрационного треугольника, пересекает поверхность ликвидус по кривой ab, а поверхность солидус по кривой cd. Полученные кривые называют соответственно изотермами ликвидуса и солидуса, их проектируют на концентрационный треугольник (линии а'b' и c'd') и около указывают соответствующие им температуры. Если нанести на концентрационный треугольник проекции линий ликвидус и солидус для нескольких температур, то можно получить сведения о температу-рах начала и конца кристаллизации для всех сплавов системы (рис. 46, б).
На рис. 47, а показаны следы сечения тройной диаграммы двумя вертикальными плоскостями, а на рис. 47, б и в — соответствующие разрезы. Следует иметь в виду, что для сплавов, соответствующих плоскости разреза, составы фаз, находящихся в равновесии в двухфазной области, не могут быть определены с помощью этого разреза, так как они обычно лежат вне его. Нельзя определить и количественное соотношение фаз для двухфазной области.
Однако политермические разрезы дают возможность определить температуры начала и конца фазовых превращений в сплавах, соответствующих разрезу (например, точки tH и tK для сплава l на рис. 47, в, отвечающие температурам начала и конца кристаллизации).
Вопросыдлясамопроверки
1.Что такое эвтектика? Опишите процесс кристаллизации эвтектики.
2.Определите число фаз, их состав и количество при разных температурах
исоставах сплавов между линиями ликвидус и солидус в двухкомпонентной системе с полной взаимной растворимостью в жидком и твердом состояниях. Что такое конода?
3* |
67 |

3.Чем отличаются механизм и кинетика полиморфного превращения в сплавах от чистых металлов?
4.Как получить пересыщенный твердый раствор в системе сплавов с ограниченной растворимостью? Как называется такой технологический процесс?
5.Чем отличается дендритная ликвация от ликвации по плотности? Как устранить эти виды ликвации?
6.Нарисуйте схему структуры твердого раствора и гетерогенную (матричную) структуру сплавов?
7.Как определяется состав тройного сплава?
ГЛ А В А V. ДЕФОРМАЦИЯ ИРАЗРУШЕНИЕ
МЕТАЛЛОВ
1. ВИДЫ НАПРЯЖЕНИЙ
Дeформацией называeтcя измeнeниe размeров и формы тeла под воздeйcтвиeм приложенных cил. Деформация вызывается действием внешних сил, приложенных к телу, или различными физико-механическими процессами, происходящими в самом теле (например, изменением объема отдельных кристаллов при фазовых превращениях или вследствие температурного градиента). При этом напряжения 1 в случае одноосного растяжения S = P/F. Сила Р, приложенная к некоторой площадке F, обычно не перпендикулярна к ней, а направлена под некоторым углом, поэтому в теле возникают нормальные и касательные напряжения (рис. 48, a). Напряжения могут быть: иcтинными — когда силу ОТНОСЯТ К сечению, существующему в данный момент деформации:
1 Понятие напряжение введено для оценки величины нагрузки, не зависящей от размеров деформируемого тела.
68
условными — когда силу относят к исходной площади сечения. Истинные касательные напряжения обозначают t и нормальные S, а условные соответственно τ и σ. Нормальные напряжения подразделяют на растягивающие {положительные) и сжимающие (отрицательные).
Наличие в испытуемом образце (изделии) механических надрезов, трещин, внутренних дефектов металла (металлургического, технологического или эксплуатационного происхождения), сквозных отверстий, резких переходов от толстого к тонкому сечению приводит к неравномерному распределению напряжений, создавая у основания надреза пиковую концентрацию нормальных напряжений (рис. 48, б). В связи с этим такие источники концентрации напряжений называют концентраторами напряжений. Пик напряжений σκ тем больше, чем меньше радиус концентратора напряжения и чем больше глубина надреза с: σК = 2σΗ √c/r, где σΗ — номинальное (среднее) напряжение.
Так как напряжения вызываются разными причинами, то различают временные напряжения, обусловленные действием внешней нагрузки и исчезающие после ее снятия, и внутренние остаточные напряжения, возникающие и уравновешивающиеся в пределах тела без действия внешней нагрузки.
Внутренние остаточные напряжения возникают в процессе быстрого нагрева или охлаждения металла вследствие неоднородного расширения (сжатия) поверхностных и внутренних слоев. Эти напряжения называют тепловыми, или термическими. Кроме того, напряжения появляются в процессе кристаллизации, при неоднородной деформации, при термической обработке вследствие неоднородного протекания фазовых превращений по объему. Их называют фазовыми, или
структурными.
2. УПРУГАЯ И ПЛАСТИЧЕСКАЯ ДЕФОРМАЦИИ МЕТАЛЛОВ
Упругая деформация. Упругой деформацией называют деформацию, влияние которой на форму, структуру и свойства тела устраняется после прекращения действия внешних сил. Упругая деформация не вызывает заметных остаточных изменений в структуре и свойствах металла; под действием приложенной нагрузки происходит только незначительное относительное и обратимое смещение атомов. При растяжении монокристалла возрастают расстояния между атомами, а при сжатии атомы сближаются. При таком смещении атомов из положения равновесия нарушается баланс сил притяжения и электростатического отталкивания, поэтому после снятия нагрузки смещенные атомы вследствие действия сил притяжения или отталкивания возвращаются в исходное равновесное состояние и кристаллы приобретают свою первоначальную форму и размеры.
Пластическая деформация. При возрастании касательных напряжений выше определенной величины деформация становится
69

необратимой. При снятии нагрузки устраняется лишь упругая составляющая деформации. Часть же деформации, которую называют плаcтической, остается. При пластической деформации необратимо изменяется структура металла, а следовательно, и его свойства.
Пластическая деформация осуществляется скольжением и двойникованием.
Схема упругой и пластической деформации металла с кубической структурой, подвергнутого действию касательных напряжений, показана на рис. 49.
Скольжение в кристаллической решетке протекает по плоскостям и направлениям с наиболее плотной упаковкой атомов, где сопротивление сдвигу наименьшее.
Это объясняется тем, что расстояние между соседними атомными плоскостями наибольшее, т. е. связь между ними наименьшая. Плоскости скольжения и направления скольжения, лежащие в этих плоскостях, образуют cиcтему cкольжения. В металлах могут действовать одна или одновременно несколько систем скольжения.
В металлах с ГЦК решеткой — Feγ, Cu, А1 и других — скольжение протекает по плоскостям октаэдра (111) и в направлении диагонали грани куба [110]; а в металлах с ОЦК решеткой — Feα, Mo, V и других — скольжение наиболее легко осуществляется по плоскостям (110), (112) и (123) в направлении пространственной диагонали куба [111] (см. рис. 8); в металлах с ГПУ решеткой — Mg, Zn, Be и др. — скольжение идет по плоскости базиса.
Металлы с кубической кристаллической решеткой (ГЦК и ОЦК) обладают высокой пластичностью, так как скольжение в них происходит во многих направлениях. Металлы с ГПУ структурой менее пластичны и поэтому труднее, чем металлы с кубической структурой, поддаются прокатке, штамповке и другим видам деформации.
Процесс скольжения не следует представлять как одновременное передвижение одной части кристалла относительно другой.
70
