
7.3. Обмін піримідинових нуклеотидів і його порушення
7.3.1. Біосинтез піримідинових нуклеотидів. Фонд піримідинових нуклеотидів, так само як і пуринових, забезпечується завдяки синтезу з простих попередників de novo, і лише 10 – 20 % від загальної їх кількості утворюється завдяки «запасним» шляхам із азотистих основ чи нуклеозидів.
Синтез піримідинових нуклеотидів відбувається в цитозолі клітин із взаємодії СО2, NН3 і аспартату, цей процес майже повністю розшифрований завдяки дослідженням П. Рейхарда.
Послідовність хімічних реакцій синтезу піримідинових нуклеотидів, зокрема УМФ, можна представити наступним чином (рис. 7.9):

Рис. 7.9. Схема синтезу УМФ
Як видно зі схеми, І стадія синтезу УМФ - це утворення карбамоїлфосфату з глутаміну, каталізатором виступає цитоплазматична карбамоїлфосфатсинтетаза.
На II стадії карбамоїлфосфат реагує з аспартатом, внаслідок чого утворюється N-карбамоїласпарагінова кислота. Остання піддається циклізації (під дією дигідрооротази) з відщепленням молекули води, при цьому утворюється дигідрооротова кислота, яка підлягає дегідруванню з перетворенням на оротову кислоту. У цій реакції бере участь специфічний НАД-вмісний фермент дигідрооротатдегідрогеназа. Оротова кислота під впливом УМФ-синтази реагує з ФРПФ, що виступає донором рибозо-фосфату, з утворенням оротидин-5’-фосфату (ОМФ). Декарбоксилювання останнього призводить призводить до утворення піримідинового нуклеотиду - УМФ.
Подальше перетворення УМФ на УДФ і УТФ здійснюється, як і в пуринових нуклеотидів, шляхом фосфотрансферазних реакцій:
Нуклеозидмонофосфаткіназа (НМФ-кіназа) каталізує реакцію утворення УДФ:
УМФ + АТФ → УДФ + АДФ,
а нуклеозиддифосфаткіназа (НДФ-кіназа) – утворення УТФ:
УДФ + АТФ → УТФ + АДФ.
Фермент ЦТФ-синтетаза каталізує АТФ-залежне заміщення кетогрупи урацилу на амідну групу глутаміну з утворенням цитидин-5’-трифосфату (ЦТФ):
УТФ + Глн + АТФ → ЦТФ + Глу + АДФ + Фн
У
Рис. 7.10.
Схема метаболізму піримідинових
нуклеотидів: 1, 2 - дефекти ферментів
при оротацидурії
7
 Рис.
7.11.
Схема регуляції синтезу піримідинових
нуклеотидів
Рис.
7.11.
Схема регуляції синтезу піримідинових
нуклеотидів
1. карбамоїлфосфатсинтетази, активність якої посилює ФРПФ, а алостеричними інгібіторами виступають УТФ – кінцевий продукт біосинтетичного процесу та пуринові нуклеотиди (рис. 7.11);
2. аспартаткарбамоїлтрансферази, активатором якої слугує АТФ, а алостеричним інгібітором виступає ЦТФ.
Такий спосіб регуляції запобігає надлишковому синтезу не лише УМФ, а й усіх інших піримідинових нуклеотидів і забезпечує збалансоване утворення всіх чотирьох основних пуринових і піримідинових нуклеотидів, необхідних для синтезу РНК.
7.3.3. Розпад піримідинових нуклеотидів. На відміну від пуринових, розпад піримідинових нуклеотидів супроводжується розкриттям кільця. Цей процес розпочинається відщепленням рибозофосфату з подальшим окисненням піримідинових основ.
Цитидилові нуклеотиди гідролітично втрачають аміногрупу, перетворюючись на УМФ. Коли за участі нуклеотидази (або фосфатази) і уридинфосфорилази відщеплюється неорганічний фосфат і рибоза, залишається азотиста основа – урацил. Аналогічно розщеплюються дезоксирибонуклеотиди: з дЦМФ утворюється урацил, а з дТМФ – тимін.
Піримідинові основи приєднують 2 атоми водню з утворенням дигідроурацилу чи дигідротиміну. Обидва гетероцикли можуть взаємодіяти з водою з утворенням дигідроурацилу, який перетворюється на -уреїдопропіонову кислоту, та дигідротиміну, який перетворюється на -уреїдоізомасляну кислоту. Обидва уреїдопохідних під впливом уреїдопропіонази розщеплюються з утворенням СО2, NH4 та -аланіну чи -аміноізомасляної кислоти відповідно (рис.7.12):
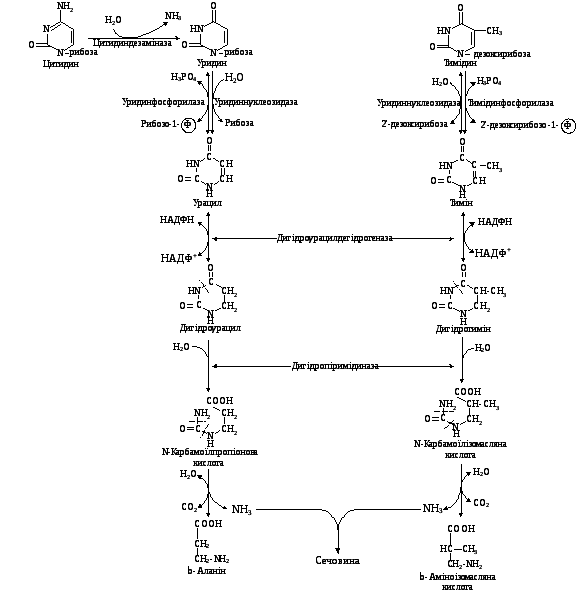
Рис. 7.12. Схема розпаду піримідинових нуклеозидів
Початкові етапи реакції розпаду піримідинових нуклеотидів каталізують специфічні ферменти. Кінцевими продуктами реакції є:
СО2, NН3, сечовина, β-аланін і β-аміноізомасляна кислота. Слід вказати, що гідролітичний розпад піримідинів є, очевидно, головним шляхом утворення β - аланіну, який може служити джерелом для синтезу ансерину і карнозину, а також для утвореннятворення КоА. Відомо, що β – аланін у тваринних тканинах піддається подальшому розпаду. У тканинах тварин відкрита специфічна амінотрансфераза, яка каталізує трансамінування між β-аланіном і піровиноградною кислотою. В процесі цієї зворотної реакції синтезуються α-аланін і формілацетат:

Формілацетат далі підлягає окиснювальному декарбоксилуванню з утворенням вуглекислоти та ацетил-КоА.
7.3.4. Порушення синтезу піримідинових нуклеотидів. Спадкове порушення синтезу оротової кислоти, відоме як оротацидурія, характеризується утворенням її надлишку Кількість виведеної оротової кислоти в складі сечі при цьому може зростати до 1,0 – 1,5 г , що в 1 000 разів перевищує норму.
Оротатацидурія І типу- порушення піримідинового обміну, зумовлене дефіцитом двох ферментів:оротатфосфорибозилтрансферази, яка каталізує перетворення оротату на оротидилат, ідекарбоксилази, що каталізує перетворення оротидилату на уридинмонофосфат. Діти народжуються нормальними, але впродовж першого року життя в них розвивається мегалобластична анемія, згодом вони відстають у рості і розумовому розвитку. У сечі виявляють кристали оротової кислоти помаранчевого кольору (помаранчева кристалоурія).
Захворювання ставить дітей у залежність від зовнішніх джерел уридину. Вживання уридину чи цитидину призводить до зменшення утворення й екскреції оротової кислоти, відновлює нормальний ріст і розвиток. Таке лікування повинно продовжуватися впродовж усього життя.
Оратацидурія ІІ типурозвивається при нестачі тільки одного ферменту –оротидин-5-фосфатдекарбоксилази. У таких пацієнтів у сечі виявляють оротидин на відміну від І типу патології, при якій більшою мірою екскретується оротова кислота.
Вторинна оротова ацидурія(синдром Рейє) виникає при пошкодженні мітохондрій печінки. У результаті порушується утилізація карбамоїлфосфату, він включається в цикл синтезу оротової кислоти.
7.3.5. порушення катаболізму піримідинових нуклеотидів. Відомі порушення в робті двох ферментів цього метаболічного шляху. При недостатності піримідин-5’-нуклеотидази порушується відщеплення неорганічного фосфату від піримідинових мононуклеотидів і, відповідно, утворення нуклеозидів. Неактивна ізоформа зазначеного фермента виявлена в еритроцитах, там відбувається накопичення піримідинових НТФ, котрі інгібують пентозофосфатний шлях перетворення глюкози і створюють умови для гемолізу цих клітин крові.
Дигідропіримідиндегідрогеназа – фермент катаболізму піримідинів, який регулює його швидкість. Порушення роботи цього фермента супроводжується відхиленнями в функціонуванні нервової системи та діагностується на основі підвищення рівня вільних піримідинів – урацилу та тиміну в плазмі крові.
