
- •Биологическое окисление
- •Содержание
- •Биологическое окисление
- •Биомедицинское значение
- •Превращение энергии:
- •Цикл
- •Роль ЦТК
- •Пластическая роль ЦТК
- •Регуляторная роль «велосипеда
- •Пути утилизации О2 в
- •Митохондриальное
- •Митохондрии: локализация в клетке
- •Общая структура Мх
- •Сравнительная характеристика мембран Мх
- •Липидный состав мембран Мх
- •Электрон-транспортная
- •Схема ДЦ и действие ингибиторов
- •Участки связывания ингибиторов ДЦ и ОФ
- •Структура ДЦ : Обзор
- •Механизм образования АТФ в
- •Общая
- •Отношение P/O
- •Электрон-транспортная (дыхательная) цепь ЭТЦ (ДЦ)
- •Функции ДЦ Мх
- •Структура протонного
- •Функциональная схема ДЦ
- •Комплекс I (NADH-CoQ reductase)
- •Коэнзим Q10 (КoQ10) или
- •Комплекс II (Сукцинат-КoQ редуктаза) или СДГ
- •Комплекс II и III
- •Комплекс IV: Цитохром c
- •ATФ/AДФ - транслоказа
- •Функционирование ДЦ
- •Функциональная схема ДЦ
- •Inhibitors of Oxidative Phosphorylation
- •The Structures of Several Inhibitors of ETC
- •Several Uncouplers of OP
- •Действие разобщителей
- •Эндогенные разобщители генерируют тепло
- •Разобщающие белки
- •Энергетика Протонная Натриевая
- •Нарушения
- •Митохондриальные болезни
- •Некоторые Мх заболевания
- •Клинические проявления и лечение Мх заболеваний
- •Мх - источник образования АФК
- •LHON
- •MERRF, MELAS et al.
- •Can Mitochondrial Diseases be Treated?
- •Микросомальное окисление
- •Сравнительная характеристика Мх и Мс ДЦ
- •Цитохром P450 монооксигеназы
- •Cytochrome b5
- •Monooxygenase System (Microsomal
- •Функционирование микросомальной ДЦ
- •Роль цитохрома P450 в микросомальном окислении
- •Механизм микросомального окисления
- •Цикл цитохрома Р450
- •Варианты строения микросомальной ДЦ
- •Мх - продуцент АФК
- •Механизм образования АФК
- •Повреждающее действие АФК на клетку
- •Антиоксидантная защита
Механизм образования АТФ в
Мх
(гипотезы сопряжения ТД и ОФ)
• Химического сопряжения (Э. Слейтер) при
транспорте е- в ДЦ образуется интермедиант с (~ ) макроэрг связью, идущей на образование АТФ
• Конформационного сопряжения (П.
Бойер) конформационные изменения белков при
транспорте е- в ДЦ депонируют энергию (модель мыш сокращение)
•Хемиосмотического сопряжения (П. Митчел, 1961) Нобелевская премия 1978
г

Общая
структу ра ДЦ Мх
NAD -
зависимые
Изоцитрат
Малат α-кетоглутар Пируват Глутамат Окси-ЖК-ты
М А Т Р И К С |
Межмембранное пространство |
|||||
|
NAD+ |
-0,32v |
|
I |
|
|
H |
NADH•H+ |
|
|
H+ |
||
|
FMN |
FeS- |
|
|||
S |
|
|
||||
|
|
|
белки |
|
||
H |
|
-0,30v |
|
|||
S |
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|
|
|
|
FAD - |
H |
|
|
|
|
зависимые |
S |
FAD |
|
|
||
Сукцинат |
H |
FeS |
|
|
|
|
ЖК-ты |
|
|
|
|
|
|
|
|
|
+0,04v |
Q |
|
H+ |
|
|
|
|
|
||
|
|
|
+0,23v |
Цит b |
3 |
|
|
|
|
|
|
||
|
|
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|
|
Цит C1 |
|
|
|
|
|
+0,25v |
C |
|
|
|
|
|
Цит a |
|
4 |
|
|
|
|
|
|
|
H+ |
|
|
+0,55v |
4 , 4H+ |
Цит a3 |
|
|
|
|
|
|
|
|
|
|
|
|
e |
|
|
|
|
|
+0,82v |
H2O |
2O2 |
|
|
|
F1 |
|
|
|
|
|
|
|
ADP+P |
F0 |
|
|
|
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ |
|
|
|
|
ATP |
|
|
|
|
Дыхательная цепь и 5-й комплекс
Отношение P/O
•P/O количественный показатель степени сопряжения (эффективности) ОФ
•Отношение P/O отражает отношение кол-ва молекул Фн, пошедших на образование АТФ к кол-ву поглощенных атомов О2
АДФ + Фн → АТФ
•При транспорте электронов с NADH в ДЦ образуется ≈3 молей АТФ
•При транспорте электронов с FADH2 в ДЦ образуется ≈2 молей АТФ
– |
NADH зависимые субстраты |
P/O = 3 |
– |
FADH2 зависимые субстраты |
P/O = 2 |
– |
Адреналин, аскорбат |
P/O = 1 |
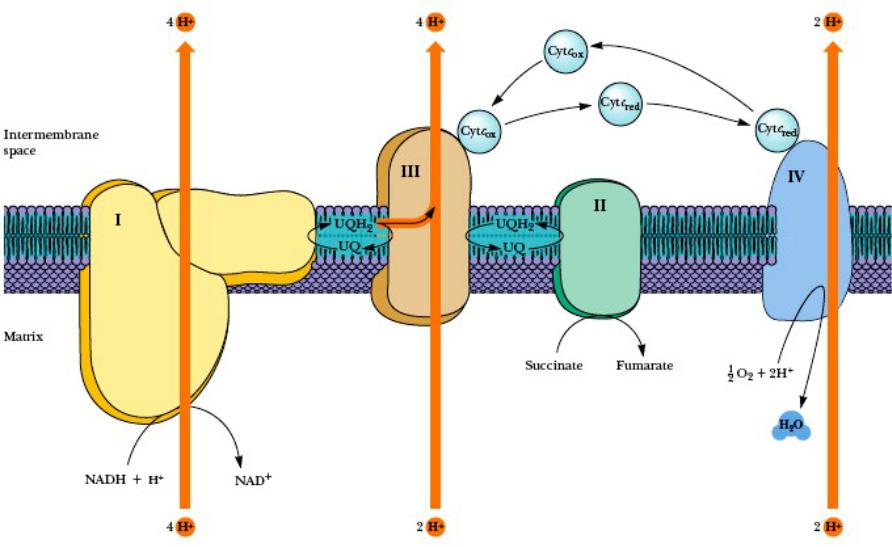
Электрон-транспортная (дыхательная) цепь ЭТЦ (ДЦ)
Функции ДЦ Мх
ДЦ Мх - общая финальная стадия БО всех аэробных клеток
1. За счет энергии окисления NADH+ H+ и FADH2 до NAD+ и FAD в ДЦ образуется μН+,
2.Сопряжение ТД и ОФ - в сопрягающих комплексах (I, III и IV) ДЦ Мх энергия транспорта электронов ( μН+) конвертируется
в энергию АТФ и др виды:
3.Главный источник АТФ и др. видов биологически конвертируемой энергии аэробных клеток
Эн хим связи →Эн μН+ → др виды Эн
(хим связи АТФ, механич, осмотич, световая, t )

|
|
|
Хемиосмотическое |
||||||||||
|
|
|
|
|
|
сопряжение |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
• Общий путь используется Мх, ХП |
|
|
|
|
|
|
|
|
|
|
|
|
|
и прокариотами для |
|
|
|
|
|
|
|
|
|
|
|
|
|
производства энергии на |
|
|
|
|
|
|
|
|
|
|
|
|
|
биологические нужды |
|
солнце |
|
|
пиша |
|
|
|
• Хемиосмотическое сопряжение |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
отражает связь между |
|
|
|
|
|
|
|
|
|
|
|
|
|
химическими реакциями («хеми») |
|
|
|
|
NADH, FADH2 |
|
|
|
|
|
генерации АТФ и мембранным |
||||
|
|
|
|
|
|
|
|
транспортом («осмотическое») |
|||||
|
|
энергизованные |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
электроны |
|
|
|
|
|
• Процесс сопряжения протекает в |
||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
две связанные стадии, каждая из |
|
|
|
|
|
μН+ |
|
||||||||
|
|
|
|
|
|
|
|
которых происходит с участием |
|||||
|
|
(Δ Ψ и ΔрН+ ) |
|
|
|
|
комплексов ДЦ внутренней |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
мембраны Мх |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
t |
|
|
||
Активный |
|
|
|
|
|
|
|||||||
ембранный |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
транспорт |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
Вращени |
|
|
Свечен |
|
||||||
|
|
|
Синтез |
|
|
|
|
|
|||||
|
|
|
|||||||||||
|
|
|
АТФ |
|
|
е |
|
|
|
ие |
|
||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
жгутиков |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
Структура протонного
градиента
• μН+ состоит из Ψ и ΔрН+
•
•Величина μН+ ≈ 180 мВ (≈ 250
кВ/см2 внутр мембраны Мх)
•ΔрН+ составляет ≈ 1 рН
•Общая площадь внутр мембр Мх клеток
H.s. ≈ 100 000 м2
• Рассеить энергию μН+ (разобщить ОФ) можно воздействуя на оба компонента

Функциональная схема ДЦ
4H+ |
4H+ |
2H+ |
F-цикл |
QH2 |
Q-цикл |
O-цикл |
|
NADH + H+
|
|
|
|
|
|
4H+ + O |
NAD+ |
FADH2 |
|
|
H2O |
|
2 |
|
|
|
|
|||
|
4H+ |
|
+ |
2H |
+ |
|
|
FAD |
|
||||
|
|
2H |
|
|
TCA
•В ДЦ имеется 3 цикла: F-цикл, Q-цикл и O- цикл.
•Протонные насосы формируют H+
•Энергия H+ используется для совершения полезной работы (синтез АТФ, осмотической, механической и др.)
ADP + Pi
H+
ATP synthase
ATP

Комплекс I (NADH-CoQ reductase)
• Содержит:
1. FMN
2. FeS центры
(22-24 (Fe-S)
белка в 5-7 кластерах
• Акцептор электронов
Ко Q

Коэнзим Q10 (КoQ10) или
Убихинон
O
H3C O

 CH3 H3C O
CH3 H3C O





O |
CH3 10 |
•КoQ10 компонент расположенный в «середине» ДЦ
•транспортирует электроны с NADH, с сукцината,
ацил-КоА и α-глицерофосфата

КoQ10
|
O |
|
|
|
|
|
|
|
|
|
|
H3C |
O |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
CH3 |
CH3 |
CH3 |
CH3 |
CH3 |
CH3 |
CH3 |
CH3 |
CH |
CH |
|
|
|
|
|
|
|
|
|
|
3 |
3 |
•Окисляется цитохромами
•Это коллектор электронов нескольких FAD-зависимых ДГ
