
- •27 Декабря 2009, протокол № 5
- •Введение
- •Правила техники безопасности и пожарной безопасности в лаборатории химии Общие требования безопасности
- •Требования безопасности перед началом работ
- •Правила безопасности при выполнении работ
- •Первая помощь при несчастных случаях в лаборатории
- •Требования безопасности по окончании работ
- •Меры пожарной безопасности
- •Лабораторная работа № 1 скорость химических реакций и химическое равновесие
- •Краткие теоретические сведения Скорость химических реакций
- •Химическое равновесие
- •Экспериментальная часть
- •Содержание отчета
- •Контрольные вопросы
- •Лабораторная работа № 2 растворы
- •Краткие теоретические сведения
- •Общее для растворов и механических смесей
- •Общее для растворов и химических соединений
- •Способы выражения состава раствора
- •Экспериментальная часть
- •Содержание отчета
- •Контрольные вопросы
- •Лабораторная работа № 3 окислительно-восстановительные реакции
- •Краткие теоретические сведения Основные понятия, связанные с реакциями окисления-восстановления
- •Основные положения теории окислительно-восстановительных реакций (овр)
- •Классификация овр
- •Методы расстановки коэффициентов в уравнениях овр
- •1. Расстановка коэффициентов
- •2. Расстановка коэффициентов методом полуреакций
- •I вариант
- •II вариант
- •Экспериментальная часть
- •1. Реакции межмолекулярного окисления-восстановления
- •2. Реакции внутримолекулярного окисления-восстановления
- •Краткие теоретические сведения
- •Экспериментальная часть
- •Часть I. Метод протекторной защиты.
- •Часть II. Метод катодной защиты (электрозащита).
- •Содержание отчета
- •Контрольные вопросы
- •Литература
- •Содержание
Содержание отчета
Название и цель работы.
Используемые приборы, реактивы и оборудование.
Записать в отчет краткие теоретические сведения.
Приведите расчеты количества вещества для каждого опыта согласно полученному заданию.
Для первого опыта определите молярную концентрацию полученного раствора бихромата калия (или другой соли).
Для третьего опыта рассчитайте массовую долю серной кислоты в полученном растворе.
Выводы по работе.
Контрольные вопросы
Плотность раствора, содержащего 40%
 ,
равна 1,25 г/см3.
Рассчитайте молярную концентрацию
азотной кислоты, если объем раствора
равен 600 см3.
,
равна 1,25 г/см3.
Рассчитайте молярную концентрацию
азотной кислоты, если объем раствора
равен 600 см3.В какой массе воды надо растворить 6,72 дм3
 (объем измерен при н.у.), чтобы получить
соляную кислоту, содержащую 9%
(объем измерен при н.у.), чтобы получить
соляную кислоту, содержащую 9% ?
?В каком объеме воды необходимо растворить
 ,
чтобы получить 400 см3
раствора с массовой долей медного
купороса, равной 0,15 и плотностью 1,15
г/см3?
,
чтобы получить 400 см3
раствора с массовой долей медного
купороса, равной 0,15 и плотностью 1,15
г/см3?Найдите молярную концентрацию раствора гидроксида калия с массовой долей
 ,
равной 0,22, и плотностью 1,196 см3.
,
равной 0,22, и плотностью 1,196 см3.Какой объем раствора хлорида меди (II) концентрации 0,5 моль/дм3, содержащего 20 % этой соли можно приготовить из 50 см3? (
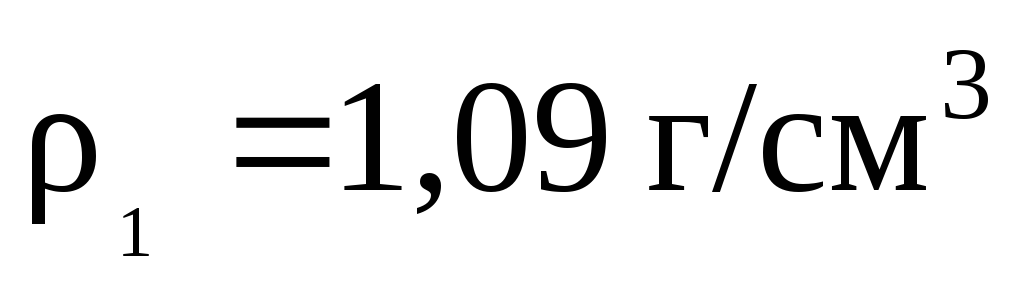 )?
)?
Таблица 3 – Плотность и массовая для кислот и щелочей в водных растворах при 18º С
|
Массовая доля |
Плотность, г/см3 | |||||
|
Н2SO4 |
HNO3 |
HCl |
KOH |
NaOH |
NH3 | |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
0,02 |
1,013 |
1,011 |
1,009 |
1,016 |
1,023 |
0,992 |
|
0,04 |
1,027 |
1,022 |
1,019 |
1,133 |
1,046 |
0,983 |
|
0,06 |
1,040 |
1,033 |
1,029 |
1,048 |
1,069 |
0,973 |
|
0,08 |
1,055 |
1,044 |
1,039 |
1,065 |
1,092 |
0,967 |
|
0,10 |
1,069 |
1,056 |
1,049 |
1,082 |
1,115 |
0,960 |
|
0,12 |
1,083 |
1,068 |
1,059 |
1,100 |
1,137 |
0,953 |
|
0,14 |
1,098 |
1,080 |
1,069 |
1,118 |
1,159 |
0,946 |
|
0,16 |
1,112 |
1,093 |
1,079 |
1,137 |
1,181 |
0,939 |
|
0,18 |
1,127 |
1,106 |
1,089 |
1,156 |
1,203 |
0,932 |
|
0,20 |
1,143 |
1,119 |
1,100 |
1,176 |
1,225 |
0,926 |
|
0,22 |
1,158 |
1,132 |
1,110 |
1,196 |
1,247 |
0,919 |
|
0,24 |
1,174 |
1,145 |
1,121 |
1,217 |
1,268 |
0,913 |
|
0,26 |
1,190 |
1,158 |
1,132 |
1,240 |
1,289 |
0,908 |
|
0,28 |
1,205 |
1,171 |
1,142 |
1,263 |
1,310 |
0,903 |
|
0,30 |
1,224 |
1,184 |
1,152 |
1,286 |
1,332 |
0,898 |
|
0,32 |
1,238 |
1,198 |
1,163 |
1,310 |
1,352 |
0,893 |
|
0,34 |
1,255 |
1,211 |
1,173 |
1,334 |
1,374 |
0,889 |
Продолжение таблицы 3
|
1 |
2 |
3 |
4 |
5 |
6 |
7 | |||
|
0,36 |
1,273 |
1,225 |
1,183 |
1,358 |
1,395 |
0,884 | |||
|
0,38 |
1,290 |
1,238 |
1,194 |
1,384 |
1,416 |
| |||
|
0,40 |
1,307 |
1,251 |
|
1,411 |
1,437 |
| |||
|
0,42 |
1,324 |
1,264 |
|
1,437 |
1,458 |
| |||
|
0,44 |
1,342 |
1,277 |
|
1,460 |
1,478 |
| |||
|
0,46 |
1,361 |
1,290 |
|
1,485 |
1,499 |
| |||
|
0,48 |
1,380 |
1,303 |
|
1,511 |
1,519 |
| |||
|
0,50 |
1,399 |
1,316 |
|
1,538 |
1,540 |
| |||
|
0,52 |
1,419 |
1,328 |
|
1,564 |
1,560 |
| |||
|
0,54 |
1,439 |
1,340 |
|
1,590 |
1,580 |
| |||
|
0,56 |
1,460 |
1,351 |
|
1,616 |
1,580 |
| |||
|
0,58 |
1,482 |
1,362 |
|
|
1,622 |
| |||
|
0,60 |
1,503 |
1,373 |
|
|
1,643 |
| |||
|
0,62 |
1,525 |
1,384 |
|
|
|
| |||
|
0,64 |
1,547 |
1,394 |
|
|
|
| |||
|
0,66 |
1,571 |
1,403 |
|
|
|
| |||
|
0,68 |
1,594 |
1,412 |
|
|
|
| |||
|
0,70 |
1,617 |
1,421 |
|
|
|
| |||
|
0,72 |
1,640 |
1,429 |
|
|
|
| |||
|
0,74 |
1,664 |
1,437 |
|
|
|
| |||
|
0,76 |
1,687 |
1,445 |
|
|
|
| |||
|
0,78 |
1,710 |
1,453 |
|
|
|
| |||
|
0,80 |
1,732 |
1,460 |
|
|
|
| |||
|
0,82 |
1,755 |
1,467 |
|
|
|
| |||
|
0,84 |
1,776 |
1,474 |
|
|
|
| |||
|
0,86 |
1,793 |
1,480 |
|
|
|
| |||
|
0,88 |
1,808 |
1,486 |
|
|
|
| |||
|
0,90 |
1,819 |
1,491 |
|
|
|
| |||
|
0,92 |
1,830 |
1,496 |
|
|
|
| |||
|
0,94 |
1,837 |
1,500 |
|
|
|
| |||
|
0,96 |
1,840 |
1,504 |
|
|
|
| |||
|
0,98 |
1,841 |
1,510 |
|
|
|
| |||
|
1,00 |
1,848 |
1,522 |
|
|
|
| |||
Таблица 4 – Плотность водных растворов K2Cr2O7
|
Массовая доля |
Плотность, г/см3 |
Массовая доля |
Плотность, г/см3 |
|
0,01 |
1,0052 |
0,06 |
1,0408 |
|
0,02 |
1,0122 |
0,07 |
1,0481 |
|
0,03 |
1,0193 |
0,08 |
1,0554 |
|
0,04 |
1,0264 |
0,09 |
1,0628 |
|
0,05 |
1,0336 |
0,10 |
1,0703 |
Таблица 5 – Плотность
водных растворов
![]()
|
Массовая доля |
Плотность, г/см3 |
Массовая доля |
Плотность, г/см3 |
|
0,01 |
1,008 |
0,06 |
1,053 |
|
0,02 |
1,016 |
0,08 |
1,072 |
|
0,04 |
1,035 |
0,10 |
1,091 |
