
- •Техническая тЕрмодинамика
- •Содержание
- •Введение
- •Основные понятия и определения
- •Предмет технической термодинамики и ее методы
- •Рабочее тело. Основные параметры состояния.
- •Термодинамическая система и окружающая среда.
- •Уравнение состояния
- •Термодинамический процесс. VP-диаграмма и термодинамические процессы в ней /равновесные и неравновесные, обратимые и необратимые, круговой процесс/.
- •Теплота и работа как формы передачи энергии.
- •Идеальные и реальные газы
- •2.1 Определения и основные законы идеальных газов.
- •Уравнение состояния идеальных газов. Газовая постоянная.
- •Газовая постоянная одного килограмма газа:
- •Смеси идеальных газов
- •Основные определения. Способы задания газовых смесей
- •Вычисление параметров состояния смеси
- •Реальные газы
- •Первый закон термодинамики
- •Сущность первого закона термодинамики
- •Основные формулировки 1 закона
- •3.2 Внутренняя энергия. Аналитическое выражение 1 закона термодинамики.
- •3.3 Энтальпия. Энтропия.
- •4 Теплоемкость газов
- •4.1 Основные определения. Массовая, объемная и молярная теплоемкости
- •4.2 Теплоемкость при постоянном давлении и при постоянном объеме. Уравнение Майера.
- •Теплоемкость смеси газов
- •Основные термодинамические процессы идеальных газов.
- •Общие принципы исследования термодинамических процессов.
- •Вычисление энтропии идеального газа.
- •Изохорный процесс
- •Изобарный процесс
- •Изотермический процесс
- •Адиабатный процесс
- •Политропный процесс
- •6. Второй закон термодинамики
- •Термодинамические циклы тепловых машин. Прямые и обратные циклы, обратимые и необратимые
- •Термический кпд и холодильный коэффициент циклов
- •Прямой и обратный циклы Карно и их свойства
- •Прямой цикл Карно
- •Обратный цикл Карно
- •Аналитическое выражение iIзакона термодинамики.
- •Определение термического кпд цикла через среднеинтегральные температуры.
- •Методы сравнения термических кпд обратимых циклов
- •Обобщенный цикл Карно
- •Водяной пар
- •Фазовые переходы веществ
- •Диаграммы воды и водяного пара в vPиvTкоордината. Пограничные кривые. Критические точки
- •7.3 Определение параметров состояния воды и водяного пара
- •Основные параметры сухого насыщенного пара
- •Основные параметры перегретого пара
- •Основные параметры влажного насыщенного пара
- •Диаграмма sTдля водяного пара
- •7.8 Термодинамические процессы изменения состояния водяного пара
- •7.8.1.1Изохорный процесс
- •Изобарный процесс
- •Изотермический процесс
- •7.8.4Адиабатный процесс
- •8.Влажный воздух
- •Основные понятия и определения
- •Расчет основных параметров влажного воздуха
- •Течение газов
- •Уравнения движения
- •Уравнение первого закона термодинамики для потока газа
- •Располагаемая работа газа в потоке
- •Уравнение неразрывности
- •Скорость истечения
- •Секундный расход идеального газа через сопло
- •Истечение газа из сосуда неограниченной емкости
- •Основные условия течения идеального газа по каналам переменного сечения
- •Сопло Лаваля
- •При дозвуковом и сверхзвуковом течении
- •Истечение газов и паров с учетом трения
- •Дросселирование газов и паров
- •Дросселирование водяного пара
- •Компрессоры
- •Классификация и принципы действия компрессоров
- •Одноступенчатый поршневой компрессор
- •Ротационный (пластинчатый) компрессор
- •10.1.3 Центробежный компрессор
- •Компрессора
- •10.2 Теоретическая индикаторная диаграмма поршневого компрессора
- •Компрессора
- •10.3 Влияние процесса сжатия на величину работы одноступенчатого компрессора
- •В компрессоре в зависимости от способа сжатия:
- •Действительная индикаторная диаграмма компрессора
- •Многоступенчатое сжатие
- •Охлаждением рабочего тела
- •Циклы поршневых двигателей внутреннего сгорания (двс)
- •1Цикл двс с подводом теплоты при постоянном объеме (цикл Отто)
- •Теплоты при постоянном объеме:
- •С подводом теплоты при и
- •11.2 Цикл двс с подводом теплоты при постоянном давлении (цикл Дизеля)
- •С подводом теплоты при постоянном давлении:
- •Цикл со смешанным подводом теплоты (цикл Тринклера)
- •Сравнение циклов двс
- •Сравнение циклов поршневых двс с подводом теплоты при и
- •При одинаковой степени сжатия
- •С различной степенью сжатия .
- •При и регенерацией теплоты:
- •Циклы паросиловых установок
- •Обратные термодинамические циклы
- •14.1 Цикл воздушной холодильной установки
- •14.2 Цикл парокомпрессорной холодильной установки
- •Список использованной и рекомендуемой литературы
Прямой и обратный циклы Карно и их свойства
Цикл Карно - обратимый круговой процесс, в котором совершается наиболее полное превращение теплоты в работу (или работы в теплоту). Термический КПД и холодильный коэффициент цикла Карно не зависят от физических свойств рабочего тела. Прямой (обратный) цикл Карно имеет максимально возможный термический КПД (холодильный коэффициент) в заданном интервале температур.
Т.к. t цикла Карно всегда больше 1, не зависит от рода рабочего тела и имеет наибольшее значение по сравнению с t любых других циклов, ограниченных тем же интервалом температур, то:
а) никакими новыми конструкциями тепловых двигателей или применением новых рабочих тел нельзя всю подведенную в цикле теплоту превратить в полезную работу;
б) для увеличения t нужно стремиться к таким процессам, образующим цикл, в которых средняя температура подвода теплоты была бы как можно больше, а средняя температура отвода теплоты - как можно меньше.
Прямой цикл Карно
-
а

б
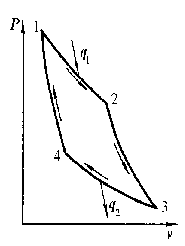
Рис. 6.2. Прямой цикл Карно: а- в vP-диаграмме; б- в sT-диаграмме
Два процесса 1-2 и 3-4 (рис. 6.2) протекают при постоянных температурах, причем Т1- температура горячего источника (нагревателя), Т2 – температура холодного источника (холодильника, т.е. Т1Т2. Процессы 2-3 и 4-1 - адиабатные. В соответствии с первым законом термодинамики
![]()
Внутренняя энергия при Т = const не меняется, а изменение внутренней энергии в адиабатных процессах, протекающих в одном и том же интервале температур, одно и то же, поэтому работа цикла:
![]()
и термический КПД
![]()
Согласно sT-диаграмме:
![]() ,
тогда
,
тогда
![]() . (6.4)
. (6.4)
Таким образом, КПД цикла Карно определяется обращением температур горячего и холодного источников теплоты. Его значение возрастает при увеличении Т1 или уменьшении Т2. В случае отсутствия перепада температур t = 0. Цикл Карно состоит из обратимых процессов и поэтому является обратимым.
Обратный цикл Карно
-

а
б
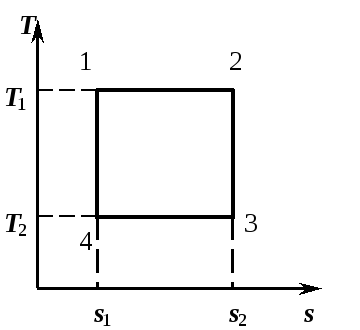
Рис. 6.2. Обратный Карно: а- в vP-диаграмме; б- в sT-диаграмме
Обратный
цикл Карно характеризуется затрачиваемой
извне работой
![]() .
При этом теплота от холодного источника
передается горячему. Это цикл холодильной
машины. Ее холодильный коэффициент
всегда больше 1:
.
При этом теплота от холодного источника
передается горячему. Это цикл холодильной
машины. Ее холодильный коэффициент
всегда больше 1:
![]() (6.5)
(6.5)
Аналитическое выражение iIзакона термодинамики.
Для обратимого цикла Карно имеем:
![]() ,
,
тогда
![]() или
или![]() .
.
Если учесть в этом соотношении, что q1 0 (теплота подводится к рабочему телу) и q20 (теплота отводится от рабочего тела), то
![]() или
или
![]() (6.6)
(6.6)
Отношение подводимой или отводимой теплоты к соответствующей абсолютной температуре называется приведенной теплотой. Выражение (6.6) показывает, что алгебраическая сумма приведенных теплот для обратимого цикла Карно равна нулю, т.е.
![]() .
(6.7)
.
(6.7)
Отношение![]() считаютполным
дифференциалом функции состояния
считаютполным
дифференциалом функции состояния
![]() ,
называемой энтропией. Т.к.dq
= Tds,
то
,
называемой энтропией. Т.к.dq
= Tds,
то
![]() (6.8)
(6.8)
Таким образом, алгебраическая сумма приведенных теплот для любого обратимого цикла равна нулю. Энтропия рабочего тела в результате совершения произвольного обратимого цикла не изменяется.
Уравнение (6.8), выведенное Клаузиусом в 1854 году, представляет собой аналитическое выражение II закона термодинамики для произвольного обратимого цикла и называется первым интегралом Клаузиуса.
В цикле с необратимыми процессами при прочих равных условиях работа, совершаемая рабочим телом меньше, чем в цикле с обратимым процессом, и при одинаковх температурах источника теплоты и холодильника
tнеобрt
Поэтому при наличии в цикле необратимых процессов:
![]() 0
(6.9)
0
(6.9)
или после интегрирования по контуру
![]() 0
(6.10)
0
(6.10)
Это неравенство представляет собой аналитическое выражение II закона термодинамики для произвольного необратимого цикла и называется вторым интегралом Клаузиуса.
Объединяя (6.7) и (6.10), можно записать одно уравнение II закона термодинамики для обратимых (=) и необратимых () циклов:
![]() 0
(6.11)
0
(6.11)
Энтропия есть функция состояния рабочего тела, поэтому изменение энтропии как для обратимого, так и необратимого процессов будет одним и тем же.
Для элементарного необратимого процесса
![]()
![]() (6.12)
(6.12)
В общем виде для любого процесса изменение энтропии удовлетворяет соотношению
![]() ,
(6.13)
,
(6.13)
где dq - количество теплоты, полученное телом от источника теплоты; Т- абсолютная температура источника теплоты. Знак равенства относится к обратимым, знак неравенства - к необратимым процессам.
Следует различать понятия энтропия тела и энтропия системы.
Энтропия не является функцией состояния системы, состоящей из нескольких тел (рабочее тело, холодильники и источники теплоты), каждое из которых характеризуется своими параметрами. Поэтому на изменение энтропии системы влияет характер процесса теплообмена между рабочим телом и источником теплоты. При протекании обратимых процессов энтропия системы остается постоянной; при необратимых процессах энтропия системы возрастает.
Если в адиабатной изолированной системе протекают только обратимые процессы, то
ds = dq/T,
для адиабатной системы это уравнение принимает вид: dq = Tds = 0
Так как Т 0, то для всей системы ds = 0 и s = const.
Таким образом, если в изолированной адиабатной системе протекают только обратимые процессы, то энтропия всей системы остается величиной постоянной.
Для адиабатной системы при наличии в ней необратимых процессов:
![]()
![]() .
.
Т.к. dq = 0, то для адиабатной изолированной системы ds 0, т.е. происходит увеличение энтропии.
В термодинамике большое значение имеет понятие работы, которую совершает система при изменении своего состояния и условий, при которых получается максимальная работа.
Получение работы возможно только от такой системы, которая не находится в равновесном состоянии с окружающей средой. По мере совершения работы система будет приближаться к равновесному состоянию со средой. Тепловая энергия, переданная в окружающую среду, становится полностью неработоспособной, т.к. при этом происходит выравнивание температур источника и приемника. Очевидно, наибольшая работа в системе может быть совершена при достижении в ней равновесного состояния путем обратимых процессов.
Максимальная
работоспособность системы, получаемая
в обратимом цикле Карно в температурном
интервале от
![]() до
до![]() ,
называетсяэксергией
(ex).
,
называетсяэксергией
(ex).
![]() .
(6.14)
.
(6.14)
Работа
необратимого цикла Карно, в котором
теплота
![]() передается
рабочему телу при температуре
передается
рабочему телу при температуре![]() ниже
температуры нагревателя
ниже
температуры нагревателя![]() :
:
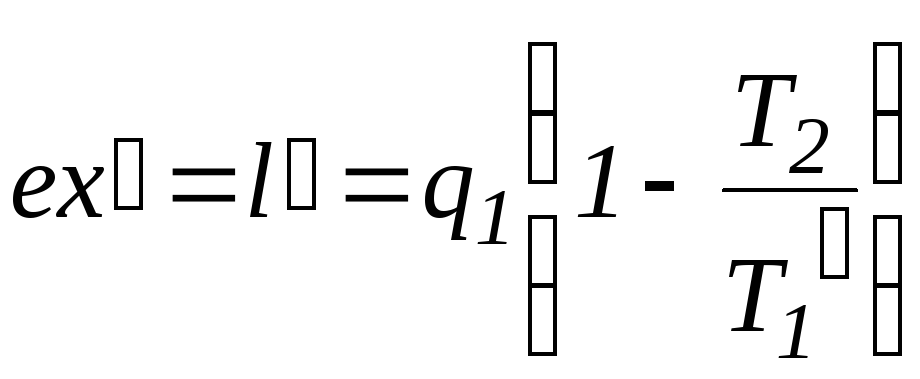 .
(6.15)
.
(6.15)
Потеря работы :
 .
(6.17)
.
(6.17)
Эксергия
является обобщенной качественной и
количественной характеристикой для
потока теплоты и потока вещества,
зависящей одновременно от параметров
системы и окружающей среды. В отличии
от энергии в реальных процессах, эксергия
количественно не сохраняется. Всякая
необратимость в системе приводит к
уменьшению работоспособности, т.е. к
потерям энергии. Уменьшение работы
ведет к увеличению энтропии
![]() :
:
![]() .
(6.18)
.
(6.18)
Уравнение (6.18) называют уравнением Гюи-Стодолы.
