
- •ПРОСТРАНСТВЕННАЯ ОРГАНИЗАЦИЯ БЕЛКА
- •ПЕРВИЧНАЯ СТРУКТУРА БЕЛКА
- •БЕЛКИ – БИОПОЛИМЕРЫ, МОНОМЕРАМИ КОТОРЫХ ЯВЛЯЮТСЯ АМИНОКИСЛОТЫ.
- •АМИНОКИСЛОТЫ, ВХОДЯЩИЕ В СОСТАВ БЕЛКА
- •АМИНОКИСЛОТЫ, ВХОДЯЩИЕ В СОСТАВ БЕЛКА
- •ОБРАЗОВАНИЕ ПЕПТИДНОЙ СВЯЗИ
- •ПЕРВИЧНАЯ СТРУКТУРА БЕЛКА
- •ОДИНАРНАЯ СВЯЗЬ
- •ПЛОСКАЯ ФОРМА ПЕПТИДНОЙ ГРУППЫ
- •ДЕЛОКАЛИЗАЦИЯ -ЭЛЕКТРОНОВ В
- •ДЕЛОКАЛИЗАЦИЯ -ЭЛЕКТРОНОВ
- •ПРИ ДЕЛОКАЛИЗАЦИИ ЭНЕРГИЯ ЭЛЕКТРОНОВ
- •ДЛИНЫ СВЯЗЕЙ
- •ДЛИНЫ СВЯЗЕЙ В ПЕПТИДНОЙ ГРУППЕ
- •ВАЛЕНТНЫЕ УГЛЫ СОСТАВЛЯЮТ ОКОЛО
- •ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ ВАЛЕНТНЫЕ СВЯЗИ
- •ГИБКОСТЬ ПОЛИПЕПТИДНОЙ ЦЕПИ, А, ЗНАЧИТ, И ЕЕ СПОСОБНОСТЬ ОБРАЗОВЫВАТЬ СПИРАЛИ И ГЛОБУЛЫ ОБЕСПЕЧИВАЕТ
- •Отсчет величины угла поворота:
- •ПОВОРОТ ВОКРУГ СВЯЗИ С-N (УГОЛ ) МАЛОВЕРОЯТЕН ИЗ-ЗА ЕЕ ЧАСТИЧНО ДВОЙНОГО ХАРАКТЕРА.
- •ВТОРИЧНАЯ СТРУКТУРА БЕЛКА
- •ГЛОБУЛА
- •НАИБОЛЕЕ ВАЖНЫМИ ДЛЯ ВТОРИЧНОЙ СТРУКТУРЫ БЕЛКА ЯВЛЯЮТСЯ ВОДОРОДНЫЕ
- •ВОДОРОДНЫЕ СВЯЗИ В БЕЛКОВОЙ МОЛЕКУЛЕ
- •ПРАВЫЕ
- •Правая -спираль.
- •Водородные связи в спирали
- •ПАРАМЕТРЫ -СПИРАЛИ
- •ПОСТУЛАТЫ ПОЛИНГА –
- •Некоторые остатки аминокислот могут нарушать формирование -спирали.
- •участки, где последовательно расположены несколько одинаково заряженных радикалов, между которыми возникают электростатические силы
- •-складчатые структуры
- •-складчатые
- •АНТИПАРАЛЛЕЛЬНЫЕ И ПАРАЛЛЕЛЬНЫЕ -СКЛАДЧАТЫЕ СТРУКТУРЫ
- •-СКЛАДЧАТАЯ СТРУКТУРА
- •ИМЕЮТСЯ СПИРАЛИ И БЕЗ ВОДОРОДНЫХ СВЯЗЕЙ,
- •Нерегулярные вторичные структуры
- •ДРУГИЕ СПИРАЛЬНЫЕ КОНФОРМАЦИИ
- •СВЕРХВТОРИЧНЫЕ СТРУКТУРЫ
- •СВЕРХВТОРИЧНЫЕ СТРУКТУРЫ –
- •1.Белки, в структуре которых обнаружены только -спирали.
- •Примеры суперспиралей
- •СУПЕРСПИРАЛЬ, СОСТОЯЩАЯ ИЗ НЕСКОЛЬКИХ -СПИРАЛЕЙ
- •Взаимодействие -спиралей в двойной (а) и тройной (б) суперспирали (вид с торца спирали).
- •2. Белки с -спиралями и -структурами
- •3. Белки, имеющие только -структуры.
- •4.Белки, имеющие в своём составе лишь незначительное количество регулярных вторичных структур.

ПОСТУЛАТЫ ПОЛИНГА –
КОРИ
•Длины связей и валентных углов всех пептидных групп одинаковы
•Полипептидная цепь насыщена водородными связями
•Конформационное состояние всех звеньев полипептидной цепи является эквивалентным

Некоторые остатки аминокислот могут нарушать формирование -спирали.
ПРОЛИН
Его атом азота входит в состав жёсткого кольца, что исключает возможность вращения вокруг -N-CH- связи.
Пролин не способен образовать водородную связь в данном месте пептидного остова, и -спиральная структура нарушается. Обычно в этом месте пептидной цепи возникает петля или изгиб.

участки, где последовательно расположены несколько одинаково заряженных радикалов, между которыми возникают электростатические силы отталкивания
участки с близко расположенными объёмными радикалами, механически нарушающими формирование - спирали, например метионин, триптофан

-складчатые структуры

-складчатые
структуры
-формы бывают параллельные, антипараллельные и смешанные.

АНТИПАРАЛЛЕЛЬНЫЕ И ПАРАЛЛЕЛЬНЫЕ -СКЛАДЧАТЫЕ СТРУКТУРЫ

-СКЛАДЧАТАЯ СТРУКТУРА
Водородные связи перпендикулярны оси спирали

ИМЕЮТСЯ СПИРАЛИ И БЕЗ ВОДОРОДНЫХ СВЯЗЕЙ,
КОТОРЫЕ СУЩЕСТВУЮТ ЗА СЧЕТ
ВАНДЕРВААЛЬСОВЫХ СИЛ.
ЭТО ПОЛИПРОЛИНОВАЯ
СПИРАЛЬ, КОТОРАЯ РЕАЛИЗУЕТСЯ В КОЛЛАГЕНЕ.
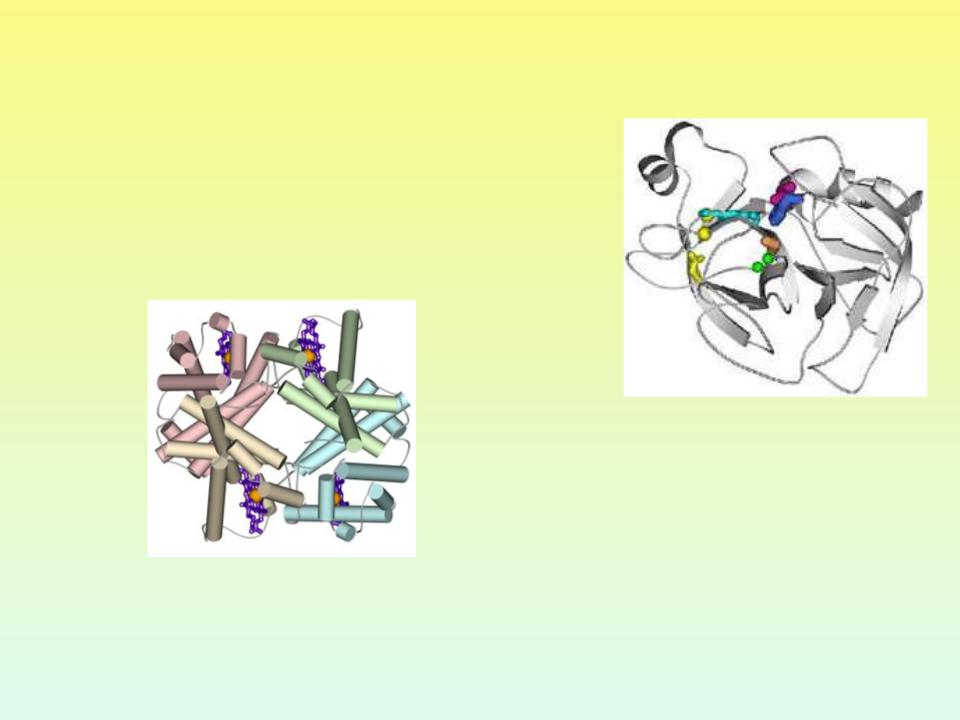
Нерегулярные вторичные структуры
Области с нерегулярной вторичной структурой, которые представлены петлеобразными и кольцеобразными структурами, имеющими меньшую регулярность укладки, чем -спиралъ и - структура
|
ТРИПСИН: |
|
ПОЛИПЕПТИДНАЯ |
|
ЦЕПЬ |
ГЕМОГЛОБИН: |
СПИРАЛИЗОВАНА |
НА 30% |
ПОЛИПЕПТИДНЫЕ ЦЕПИ СПИРАЛИЗОВАНЫ НА 75%

ДРУГИЕ СПИРАЛЬНЫЕ КОНФОРМАЦИИ
СПИРАЛЬ 310
•3 ОСТАТКА АМИНОКИСЛОТ НА ШАГ (ВИТОК) СПИРАЛИ
•РАДИУС 0,19 НМ
СПИРАЛЬ
4,4 ОСТАТКА НА ШАГ СПИРАЛИ
РАДИУС 0,28 НМ
