
- •Теоретический курс
- •Раздел 1. Металловедение.
- •1.1. Общая характеристика металлов.
- •1.1.1. История познания металлов человеком
- •1.1.2. Кристаллическое строение
- •1.1.3. Типы кристаллических решеток
- •1.1.4. Анизотропия свойств кристаллов
- •1.1.5. Полиморфизм в металлах
- •1.1.6. Строение реальных кристаллов
- •Вопросы для самопроверки
- •2.2. Кристаллизация металлов
- •2.2.1. Теоретические основы
- •1.2.2. Механизм процесса кристаллизации
- •1.2.3. Основные явления кристаллизации слитков. Влияние формы кристаллов на служебные характеристики металла
- •Вопросы для самопроверки
- •1.3. Основы теории сплавов.
- •1.3.1. Внутреннее строение и свойства механических смесей, твердых растворов и химических соединений
- •1.3.2. Диаграммы состояния сплавов. Их типы и построение
- •Вопросы для самопроверки
- •1.4. Железоуглеродистые сплавы.
- •1.4.1. Железо
- •1.4.2. Углерод
- •1.4.3. Структурные составляющие системы железо-углерод
- •1.4.4. Диаграмма состояния железо – цементит (метастабильное равновесие)
- •Вопросы для самопроверки
- •1.5. Термическая обработка стали
- •1.5.1. Основы технологии термической обработки
- •1.5.2. Основные параметры процессов термической обработки
- •1.5.3. Основные виды термической обработки
- •1.5.4. Основные превращения в сталях в процессах термообработки
- •1.5.5. Химико-термическая обработка стали. Общая характеристика процессов
- •1.5.6. Термомеханическая обработка (тмо)
- •Вопросы для самопроверки
- •1.6. Физические основы пластичности и прочности металлов
- •1.6.1. Виды деформации
- •1.6.2. Механические свойства металлов
- •1.6.3. Влияние дефектов кристаллической решетки на прочность металла
- •1.6.4. Методы исследования строения, структуры и свойств металлов
- •Вопросы для самопроверки
- •1.7. Влияние температуры на структуру и свойства металлов
- •1.7.1. Диффузия ядер в металлах
- •1.7.2. Влияние повышения температуры на механические свойства
- •1.7.3. Возврат и рекристаллизация деформированного металла при нагреве
- •1.7.4. Сфероидизация и графитизация цементита в сталях
- •Вопросы для самопроверки
- •1.8. Углеродистые и легированные стали
- •1.8.1. Условия эксплуатации и требования к сплавам
- •1.8.2. Структура и основные свойства сталей
- •1.8.3. Принципы классификации и маркировки сталей
- •1.8.4. Конструкционные стали
- •1.8.5. Инструментальные стали
- •1.8.6. Легированные стали в энергетике
- •Вопросы для самопроверки
- •1.9. Чугуны
- •1.9.1. Классификация чугунов
- •1.9.2. Серые чугуны
- •1.9.3. Высокопрочные чугуны
- •1.9.4. Ковкие чугуны
- •1.9.5. Специальные чугуны
- •1.9.6. Маркировка чугунов
- •Вопросы для самопроверки
- •1.10. Сплавы на основе железа с различными металлами
- •Вопросы для самопроверки:
1.4.4. Диаграмма состояния железо – цементит (метастабильное равновесие)
Как уже упоминалось чуть выше, железо, взаимодействуя с углеродом, может образовывать ряд химических соединений. Поскольку каждое устойчивое химическое соединение может быть рассмотрено как компонент, то и диаграмму системы железо-углерод можно проанализировать только до образования в ней карбида железа - Fе3С – концентрация углерода 6,67 % (табл. 1.3).
Таблица 1.3 - Точки диаграммы Fе -Fе3С
|
Обозначение точек |
Температура, °С |
Концентрация углерода, % масс |
Пояснение |
|
1 |
2 |
3 |
4 |
|
A |
1539 |
0,00 |
температура плавления железа |
|
D |
1500 |
6,67 |
температура плавления цементита |
|
H |
1499 |
0,10 |
предельная концентрация углерода в -феррите |
|
J |
1499 |
0,16 |
максимальное количество углерода в аустените |
|
B |
1499 |
0,50 |
концентрация углерода в жидкой фазе, находящейся в равновесии с -ферритом и аустенитом |
|
N |
1392 |
0,00 |
полиморфное превращение |
|
E |
1147 |
2,14 |
предельное содержание углерода в аустените |
|
C |
1147 |
4,31 |
максимальное количество углерода в ледебурите (+Fe3C) |
|
F |
1147 |
6,67 |
наибольшая концентрация углерода в цементите |
|
1 |
2 |
3 |
4 |
|
G |
911 |
0,00 |
полиморфное превращение |
|
P |
727 |
0,02 |
предельное содержание углерода в феррите () |
|
S |
727 |
0,80 |
максимальное количество углерода в перлите (+Fe3C) |
|
K |
727 |
6,67 |
наибольшая концентрация углерода в цементите |
|
Q |
25 |
0,006 |
минимальное содержание углерода в феррите |
|
L |
25 |
6,67 |
предельное количество углерода в цементите |
Это связано с тем, что наибольшее практическое значение имеет только часть диаграммы состояния железо-углерод, в которой показано формирование цементита, так как сплавы, содержащие большое количество углерода, очень хрупкие и практически не применяются в промышленности. Поэтому диаграмму состояния системы железо-углерод изображают только до концентрации углерода 6,67 % масс и называют диаграммой состояний железо-цементит (рис. 1.36). Ось абсцисс на данном рисунке двойная: концентрация углерода и цементита соответственно.
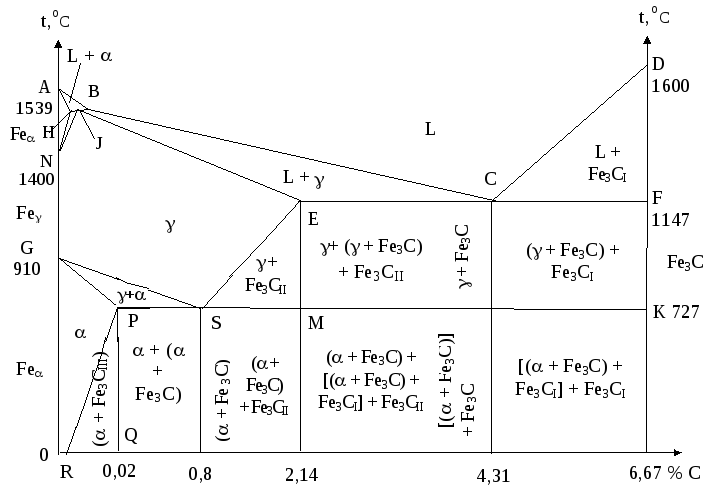
Рис.1.36 - Диаграмма состояния железо - цементит
В целом диаграмму железо – цементит можно рассматривать как комбинированную: с образованием механических смесей (эвтектики и эвтектоида), формированием твердых растворов с ограниченной растворимостью углерода и химического соединения.
Диаграмма довольно сложная, и поэтому ее анализ удобнее проводить, разделив на отдельные части. Линии диаграммы состояния Fе -Fе3С, определяющие первоначальный процесс кристаллизации сплавов с концентрацией углерода до 0,5 %, имеют следующие обозначения, принятые в классическом материаловедении и научной литературе, и физический смысл:АВ(ликвидус) показывает температуру начала кристаллизации-феррита () из жидкого сплава (L); АН(солидус) является температурной границей области расплава и кристаллов-феррита (); ниже этого участка существует только-феррит;НJВ - прямая перитектического нонвариантного (c=k–f+ 1 = 2 – 3 + 1 = 0) равновесия (1499 °С); по достижении соответствующей ей температуры, протекает реакцияLв+н=J(жидкостьLвзаимодействует с кристаллами-ферритаНс образованием аустенита составаJ). ОтрезокHN определяет температуру начала выделения кристаллов аустенитаиз(-феррита). ЛинияJN– температурный рубеж зоны обоих твердых растворови, ниже ее сплав имеет лишь структуру аустенита (рис. 1.37).
Проведем анализ процесса кристаллизации на данном участке диаграммы. Возьмем сплав с содержанием углерода меньше 0,1 %. В интервале 1 - 2 из жидкой фазы (L) начинают выделяться кристаллы-феррита, и он становится двухфазным (L+). При этом концентрация жидкости варьируется по кривойАВ, а количество твердой фазы определяется отрезкомАН.

Рис. 1.37 - Фрагмент диаграммы состояния Fe-Fe3C. Первичная кристаллизация малоуглеродистых сплавов
То есть в точке аони будут определяться
проекциями пунктовсиb,
а количества отвечающих им фаз
рассчитываться по отношению отрезков![]() и
и![]() соответственно (правило рычага). В пункте
2 количество жидкого сплава становится
равным нулю, процесс кристаллизации
заканчивается с образованием однородного
твердого раствора-феррита.
До точки 3 наблюдается простое охлаждение
данной структуры. Далее в диапазоне 3 -
4 осуществляется превращение-феррита
в аустенит ().
Концентрация состояний меняется согласно
положениям линийHNиJN. Так для пунктаdони могут обуславливаться проекциями
точекfиe,
а количество фаз – соотношением участков,
а именно,/=
соответственно (правило рычага). В пункте
2 количество жидкого сплава становится
равным нулю, процесс кристаллизации
заканчивается с образованием однородного
твердого раствора-феррита.
До точки 3 наблюдается простое охлаждение
данной структуры. Далее в диапазоне 3 -
4 осуществляется превращение-феррита
в аустенит ().
Концентрация состояний меняется согласно
положениям линийHNиJN. Так для пунктаdони могут обуславливаться проекциями
точекfиe,
а количество фаз – соотношением участков,
а именно,/=![]() .
И наконец в пункте 4 сплав полностью
обретает структуру аустенита. При
концентрации углерода 0,16 % вначале
затвердевание системы осуществляется
аналогично предыдущему сплаву с
формирования-феррита
переменного состава. В точкеJ,исходные кристаллы твердого раствора-феррита в результате
взаимодействия с жидкой фазой при
перитектической реакции полностью
превращаются в аустенит. Для нашей
системы с содержанием углерода в
интервале 0,1 - 0,5 % отличие будет наблюдаться
лишь во второй части процесса
кристаллизации. То есть справа или слева
от точкиJпо завершении
перитектической реакции состояние
сплава будет определяться избытком
твердой(-феррита)
или жидкой (L) фаз, при
последующем охлаждении превращающихся
в однофазную структуру аустенит в
соответствии с кривымиJNиJE(точка Eна данном отрезке диаграммы не указана).
.
И наконец в пункте 4 сплав полностью
обретает структуру аустенита. При
концентрации углерода 0,16 % вначале
затвердевание системы осуществляется
аналогично предыдущему сплаву с
формирования-феррита
переменного состава. В точкеJ,исходные кристаллы твердого раствора-феррита в результате
взаимодействия с жидкой фазой при
перитектической реакции полностью
превращаются в аустенит. Для нашей
системы с содержанием углерода в
интервале 0,1 - 0,5 % отличие будет наблюдаться
лишь во второй части процесса
кристаллизации. То есть справа или слева
от точкиJпо завершении
перитектической реакции состояние
сплава будет определяться избытком
твердой(-феррита)
или жидкой (L) фаз, при
последующем охлаждении превращающихся
в однофазную структуру аустенит в
соответствии с кривымиJNиJE(точка Eна данном отрезке диаграммы не указана).
На основании изложенного можно отметить, для сплавов с концентрацией углерода менее 0,5 % масс первоначальный процесс кристаллизации в любом случае будет заканчиваться формированием аустенита.
Основываясь на сделанном заключении, для исследования системы железо-цементит преимущественно в твердом состоянии, можно использовать упрощенный вариант диаграммы (рис. 1.38). На данном варианте диаграммы отсутствуют кривые перитектического превращения и условно принимается, что жидкий сплав с концентрацией углерода до 0,5 % непосредственно трансформируется в аустенит (). КриваяАСD- линия ликвидус, которая на участкеАС соответствует температурам начала выпадения кристаллов аустенита () из жидкого сплава (L), в областиСD- представляет геометрическое место точек, отвечающих температурам начала кристаллизации первичного цементита (Fe3СI) из жидкой фазы (L). ЛинияАЕСF- солидус, криволинейный кусочекАЕкоторой определяет окончание затвердевания аустенита. Прямолинейный же участокECF является геометрическим местом точек, соответствующих также концу кристаллизации аустенита (ЕС) и первичного цементита -Fe3CI(CF), и одновременно отвечает температурам изотермического превращения жидкого сплава состава пункта С в двухфазную эвтектику - ледебурит –LcЕ+Fe3C. Данная реакция наблюдается только у сплавов с содержанием углерода более 2,14 % масс.

Рис. 1.38 - Упрощенный вариант диаграммы состояния железо - цементит
Кривые ограничения максимальной растворимости углерода в фазовых составляющих железоуглеродистых сплавов DC, ES иPQрасположены на диаграмме в интервалах трех уровней температур: 1 – от 1600 до 1147С(DC), 2 – 1147 – 727С(ES) и 3 – от 727 до 25С(в некоторых источниках до 600 °С –PQ). Эти линии имеют одну общую особенность: по форме они обращены выпуклой стороной к оси температур чистого железа и определяют максимальную растворимость углерода в той фазе, которая расположена на диаграмме левее данной кривой. Это значит, что отвечающие им областиDC,ESиPQхарактеризуют предельную концентрацию неметалла: 1 в жидком сплавеLот 6,67 % в точкеDи 4,31 % - пунктС; 2 в аустенитеот 2,14 % точкаЕдо 0,8 % для точкиS; 3 в феррите- 0,02 - 0,006 % в пунктахРиQ. При понижении температуры системы меньше точек растворимости углерода из фазы, находящейся слева от соответствующей им кривой, выделяется избыток неметалла, образуя цементит определенного уровня: 1 - треугольникDCF– первичный (Fe3CI); 2 -ESM– вторичный (Fe3CII) и 3 - PQR– третичный (Fe3CIII). ОтрезкиЕС иSPограничивают соответственно изотермическое превращение жидкого сплава в ледебурит и аустенита в перлит (рис. 1.38).
Диаграмму состояния Fе -Fе3С по оси абсцисс – концентрация углерода – делят на следующие участки: 0 - 0,02 % (точкаР); 0,02 - 0,80 % (областьPS); 0,80 % (точкаS); 0,80 - 2,14 % (интервалSM); 2,14 % (пунктЕ); 2,14 - 4,31 % (диапазонEC); 4,31 % (точкаС) и 4,31 - 6,67 % (отрезокCF). Сплавы соответственно такому делению называют: 1 - технически чистое железо; 2 - доэвтектоидные; 3 - эвтектоидная; 4 - заэвтектоидные стали; 5 - доэвтектические; 6 - эвтектический и 7 - заэвтектические чугуны. Данное разделение принято называть классификацией железоуглеродистых сплавов по диаграмме состояния.
На каждом из вышеуказанных участков рассмотрим кристаллизацию типовых сплавов, обозначенных римскими цифрами I-VII(рис. 1.39 и 1.40).
Сплав I- технически чистое железо (с содержанием углерода от 0 до 0,02 %). При температурах выше точки 1 система однофазна и находится в жидком состоянии (L). В диапазоне 1 - 2 осуществляется кристаллизация сплавов в виде-твердого раствора – аустенита и система становится двухфазной -L+. В пункте 2 количество жидкого состояния становится равным нулю, затвердевание сплавов заканчивается и существует лишь однородный твердый раствор аустенита -. На участке 2 - 3 структурных превращений системы не наблюдается, а фиксируется лишь простое ее охлаждение.
В точке пересечения прямой сплава с линией GSдиаграммы - 3 - начинается перекристаллизация аустенита в феррит (→превращение), которая заканчивается в точке 4 полным образованием-твердого раствора и отрезок 4 - 5 характеризует обычное его остывание.

Рис. 1.39 - Часть диаграммы состояния железоуглеродистых сплавов (до 2,14 % С) и их кривые равновесного охлаждения
И наконец на последнем участке 5 - 6 из -феррита происходит выделение избыточного количества углерода в виде третичного цементита -Fe3CIII. Таким образом, конечная структура сплавов с концентрацией углерода от 0 до 0,02 % представляет зерна феррита с включениями третичного цементита в наиболее напряженных точках границ зерен (рис. 1.40,а).

Рис. 1.40. Структура сталей с различной концентрацией углерода: а– 0,05;б– 0,25;в– 0,40;г– 0,70;д– 0,80;е– 1,20 %
Сплав II– доэвтектоидные стали (0,02 - 0,80 % С).Здесь, как и в предыдущем сплаве кристаллизация до точки 4 имеет те же закономерности и также приводит к перекристаллизации аустенита в феррит. И на этом сходство заканчивается. Далее в пункте 4 температура системы достигает 727С, что соответствует ее значению при изотермическом превращении аустенита в перлит – двухфазную структуру, представляющую, как уже отмечалось, механическую смесь феррита и первичного цементита. Данная трансформация аустенита называется его перлитным распадом. Он возможен при выполнении двух условий в системе: когда температура будет равна 727Си концентрация углерода в аустените будет достигать 0,8 %.
При наличии трех фаз (при этой температуре): феррит (0,02 % С), цементит (6,67 % С) и аустенит (0,8 % С) - система нонвариантна (с = 2 + 1 - 3 = 0). В точке 4’ не перешедший в феррит аустенит превращается в перлит и дальнейшее охлаждение сплава до комнатной температуры протекает без каких-либо изменений его структуры.
В итоге после окончательного (равновесного) охлаждения наш сплав и все доэвтектоидные стали имеют структуру феррит + перлит (рис. 1.40, б-г).Чем выше содержание углерода в сплаве, тем больше в структуре стали образуется перлита и меньше избыточного феррита. При концентрации углерода до 0,6 - 0,7 % феррит выделяется в виде оторочки вокруг зерен перлита (ферритная сетка).
Если знать общее содержание неметалла
в сплаве, то можно рассчитать предполагаемый
состав его структуры: а именно количество
перлитной составляющей. Для этого
необходимо составить следующую пропорцию:
если концентрация углерода составляет
0,8 %, то структура будет на 100 % состоять
из перлита, а для сплава с содержанием
0,4 % С масс (сталь 40) количество перлита
будет равно Х %. Отсюда концентрацию
перлита в стали 40 вычислим по уравнению:
![]() .
.
Сплав III– эвтектоидная
сталь (концентрация углерода 0,8 %).
Затвердевание системы до температуры
727Св пункте 3, соответствующей точкеSна диаграмме, протекает аналогично двум
первым сплавам с формированием аустенита
(отрезок 1 - 2) и простым его охлаждением
(участок 2 - 3). Достигнув точки 3 сплав
охлаждается до 727Си начинает претерпевать изотермическое
разложение-твердого
раствора![]() (+Fe3C),
которое продолжается некоторое время
и конец его определяется пунктом 3’,
когда последние зерна аустенита
превратятся в перлит. Ниже точки 3' идет
простое остывание данной итоговой
структуры сплава – перлита (рис. 1.40,д).
(+Fe3C),
которое продолжается некоторое время
и конец его определяется пунктом 3’,
когда последние зерна аустенита
превратятся в перлит. Ниже точки 3' идет
простое остывание данной итоговой
структуры сплава – перлита (рис. 1.40,д).
Сплав IV– заэвтектоидные стали (от 0,80 до 2,14 % С). Подобно всем предыдущим сплавам до точки 3 в системе осуществляются те же процессы, которые приводят к формированию аустенита и его охлаждению. Однако в самом месте пересечения кривойESс линией сплава-твердый раствор пересыщается углеродом, т. е. его концентрация в аустените при температурах ниже пункта 3 становится больше, чем предельная растворимость данного неметалла в этой структурной составляющей в тех же условиях. Поэтому избыток углерода по границам перлитных зерен образует сетку вторичного цементитаFe3CII. Это происходит на участке 3 - 4, который также характеризуется уменьшением концентрации углерода по линииESдо 0,8 % в точке 4. Здесь же температура сплава достигает 727С. То есть в данный момент выполняются оба условия протекания перлитного распада аустенита, осуществляющегося на отрезке 4 - 4’. Толщина цементитной оболочки растет пропорционально содержанию углерода в стали. При этом увеличивается и хрупкость сплава. При температурах ниже точки 4’ регистрируется простое охлаждение сформировавшейся итоговой структуры вторичного цементита и перлита (рис. 1.40,е). Стали с концентрацией 1,3 - 1,5 % С практически не применяются из-за высокой хрупкости.
Чугуны, имеющие равновесную структуру согласно диаграмме железо-цементит и содержащие углерод в связанном состоянии в виде карбида железа, носят название «белых», так как их излом имеет белый цвет по сравнению с таковым у промышленных серых, в которых весь присутствующий неметалл находится в аллотропной модификации графита.
Сплав V– доэвтектические чугуны (2,14 - 4,31 % углерода). До точки 2 аналогично рассматриваемым выше системам протекает образование-твердого раствора из жидкой фазы и структура сплава складывается из двух составляющихLс+E (рис. 1.41).
Общим для всех данных пяти сплавов
является то, что состав жидкой фазы
определяется кривой АС, а твердой
– линиейАЕ. Дальнейший отвод тепла
нарушает устойчивое состояние жидкости
и в точке 2 – 1147С- она начинает превращаться в эвтектику,
называемую ледебуритом, по реакцииL![]() (+Fe3C).
Данный процесс заканчивается в пункте
2’. При более низких температурах в
интервале 2’ - 3 по границам первичных
зерен аустенита образуются и растут
зародыши вторичного цементита. То есть
на этом участке сплав будет состоять
из+ (+Fe3C)
+Fe3CII.
В точках 3 начинается и 3’ заканчивается
перлитный распад аустенита всех
существующих в этот момент структур. В
пункте 3’ формируется конечное строение
сплаваV, складывающееся
из зерен перлита (+Fe3C),
вокруг которого располагается оболочка
вторичного цементита, а расстояния
между перлитными составляющими заполняют
включения низкотемпературного ледебурита
– [(+Fe3C)
+Fe3C].
Ниже точки 3’ происходит простое
остывание данной структуры (рис. 1.41 и
1.42,а).
(+Fe3C).
Данный процесс заканчивается в пункте
2’. При более низких температурах в
интервале 2’ - 3 по границам первичных
зерен аустенита образуются и растут
зародыши вторичного цементита. То есть
на этом участке сплав будет состоять
из+ (+Fe3C)
+Fe3CII.
В точках 3 начинается и 3’ заканчивается
перлитный распад аустенита всех
существующих в этот момент структур. В
пункте 3’ формируется конечное строение
сплаваV, складывающееся
из зерен перлита (+Fe3C),
вокруг которого располагается оболочка
вторичного цементита, а расстояния
между перлитными составляющими заполняют
включения низкотемпературного ледебурита
– [(+Fe3C)
+Fe3C].
Ниже точки 3’ происходит простое
остывание данной структуры (рис. 1.41 и
1.42,а).

Рис. 1.41. Фрагмент диаграммы состояния железо-цементит (2,14 - 6,67 % С) с соответствующими кривыми охлаждения
Сплав VI– эвтектический
чугун. В интервале 1 - 1’ (линияЕСF)
существует нонвариантное (с = 0) равновесие
аустенитаЕ,
цементита (Fе3С) и
жидкой фазы Lс. В результате
кристаллизации жидкости по реакцииLсЕ+Fe3Cобразуется эвтектика, также называемая
ледебурит и состоящая в момент образования
из аустенита и цементита. До точки 2
происходит лишь ее простое охлаждение,
которое с достижением 727 °С нарушается
и характеризуется разложением аустенита
в перлит![]() (+Fe3C),
которое продолжается некоторое время
и конец его определяется пунктом 2’,
когда последние зерна аустенита
превратятся в перлит. Ниже точки 2' идет
простое остывание итоговой структуры
сплава, состоящей из низкотемпературного
ледебурита – [(+Fe3C)
+Fe3C]
(рис. 1.42, б).
(+Fe3C),
которое продолжается некоторое время
и конец его определяется пунктом 2’,
когда последние зерна аустенита
превратятся в перлит. Ниже точки 2' идет
простое остывание итоговой структуры
сплава, состоящей из низкотемпературного
ледебурита – [(+Fe3C)
+Fe3C]
(рис. 1.42, б).


Рис. 1.42. Микроструктура белых чугунов: а – доэвтектический (ледебурит + перлит); б – эвтектический (ледебурит); в – заэвтектический (ледебурит + первичный цементит)
Сплав VII- заэвтектические чугуны (4,30 - 6,67 % С) Он начинает затвердевать с понижением температуры по линии ликвидусСD,когда в жидкой фазе зарождаются и растут кристаллы цементита 0 отрезок 1 - 2. Концентрация углерода в жидком сплаве с понижением температуры уменьшается по линии ликвидус. При 1147С– точка 2 - жидкость достигает эвтектической концентрации 4,3 % С (пунктС) и кристаллизуется на участке 2 - 2’ с образованием ледебуритаЕ+Fe3C. До точки 3 никаких превращений не наблюдается, а регистрируется охлаждение трехфазной структуры (Е+Fe3C) +Fe3C. В точке 3 при пересечении линии сплава с эвтектоидной прямойPSK, как и для всех предыдущих, наступает перлитное разложение аустенита, которое заканчивается в пункте 3’, и конечная структура ниже этой точки сплава будет следующей - [(+Fe3C) +Fe3C] +Fe3C(рис. 1.42, в).
Для полного понимания процесса кристаллизации в системе железо-углерод отдельно рассматривается кристаллизация чистого железа (рис. 1.43).
Таким образом, индивидуальные железоуглеродистые сплавы после окончания процесса кристаллизации каждый имеет свою структуру, указанную выше. Однако, как можно заметить, ниже 727 С для всех фазовый состав обусловливается лишь различным соотношением в нем феррита и цементита, относительное содержание которых можно определить в зависимости от концентрации углерода в сплаве по диаграмме состояния.

Рис. 1.43. Кривая охлаждения чистого железа со структурами его полиморфных модификаций
