
- •Первый закон термодинамики
- •2. Второй и третий законы термодинамики
- •3. Термодинамические потенциалы
- •4. Химическое равновесие
- •5. Гетерогенное равновесие в однокомпонентных системах
- •6. Растворы
- •7. Электрохимия
- •8. Химическая кинетика
- •Термодинамические величины для некоторых веществ
- •Органические соединения
- •Криоскопические /к/ и эбуллиоскопические /е/ константы
- •Константы диссоциации некоторых слабых электролитов
4. Химическое равновесие
Что такое химическое равновесие? Определите этот термин, исходя из термодинамических представлений и исходя о скоростях химических реакций в системе.
Что такое смещение химического равновесия?
Какая разница между истинным равновесием и “замороженным” состоянием? Как доказать истинность равновесия?
В чем заключается разница между
 и
и ?
Как связаны эти величины? В каких случаях
?
Как связаны эти величины? В каких случаях ?
?Напишите уравнения для
 для реакций:
для реакций:
а)
![]() /
/![]() /
/
б)
![]() /
/![]() /
/
в)
![]() /
/![]() /
/
Найти соотношения
между
![]() ,
,![]() ,
,
![]() .
.
Сформулируйте принцип Ле-Шателье.
Как изменяется химическое равновесие в системе при повышении температуры. Покажите это на основе принципа Ле-Шателье и уравнения Вант-Гоффа.
Как зависит константа равновесия от температуры?
Какой параметр процесса определяет смещение равновесия в системе с химической реакцией.
Как рассчитать
 и
и реакции по табличным термодинамическим
данным? Что вы можете сказать о точности
полученных значений?
реакции по табличным термодинамическим
данным? Что вы можете сказать о точности
полученных значений?Если в трубку, содержащую смесь
 и
и при
температуре около 1000℃,
подавать поток
при
температуре около 1000℃,
подавать поток
 ,
то в выходящем газе содержатся пары
,
то в выходящем газе содержатся пары
 .
Если при тех же условиях в трубку
подавать пары
.
Если при тех же условиях в трубку
подавать пары
 ,
то в выходящих газах обнаруживается
,
то в выходящих газах обнаруживается
 .
Таким образом реакция
.
Таким образом реакция
 проходит
при одной и той же температуре, либо
слева направо, либо справа налево.
Объясните это явление. Что можно сказать
о
проходит
при одной и той же температуре, либо
слева направо, либо справа налево.
Объясните это явление. Что можно сказать
о
 реакции?
реакции?При повышении температуры давление водяного пара над
 возрастает.
Экзотермическим или эндотермическим
процессом является дегидратация
возрастает.
Экзотермическим или эндотермическим
процессом является дегидратация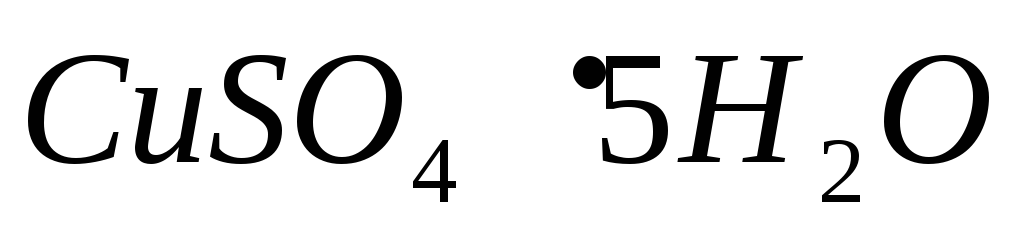 .
.
4 .12. Зависимость
константы равновесия от температуры
можно выразить уравнением
.12. Зависимость
константы равновесия от температуры
можно выразить уравнением![]() .
Таким образом, зависимость
.
Таким образом, зависимость![]() от1/Т представляет
прямую линию,
как показано на рисунке. Чем отличаются
реакции, характеристики которых
представлены прямыми 1 и 2?
от1/Т представляет
прямую линию,
как показано на рисунке. Чем отличаются
реакции, характеристики которых
представлены прямыми 1 и 2?
В какую сторону сместится равновесие в системе
 при
добавлении в систему инертного газа
при
при
добавлении в систему инертного газа
при ?
При
?
При ?
?В какую сторону сместится равновесие в системе
 ,
если ввести туда некоторое количество
,
если ввести туда некоторое количество ?
?Как влияет повышение температуры и давления на равновесие в следующих системах:
а)
![]()
б)
![]()
в)
![]()
как установить истинность равновесия в этих системах?
Предложите экспериментальные методы определения констант равновесия в системах:
а)
![]()
б)
![]()
в)
![]()
В сосуде смешали 3 л.
 и
2 л.
и
2 л. при
давлении 1 атм. Какое давление установится
в сосуде после протекания реакции и
установлении начальной температуры?
при
давлении 1 атм. Какое давление установится
в сосуде после протекания реакции и
установлении начальной температуры?В системе протекает реакция
 .
Если смешать по 2 моляA
и B,
то к моменту равновесия прореактирует
0,5 моля A.
Найдите константу равновесия.
.
Если смешать по 2 моляA
и B,
то к моменту равновесия прореактирует
0,5 моля A.
Найдите константу равновесия.При некоторой температуре в смеси 1 моля
 и
1 моля
и
1 моля в
1 литре после протекания реакции
содержится 1,6 моля
в
1 литре после протекания реакции
содержится 1,6 моля .
Рассчитайте состав смеси, образующейся
при этой температуре, если смешаны (2
моля
.
Рассчитайте состав смеси, образующейся
при этой температуре, если смешаны (2
моля и
3 моля
и
3 моля )
2 моля
)
2 моля ,
2 моля
,
2 моля ,
2 моляHI
?
,
2 моляHI
?Рассчитайте равновесные концентрации в системе

 ,
если смешаны по 3 моляA,
B
и C.
,
если смешаны по 3 моляA,
B
и C.
Как рассчитать давление пара
 над
над при 100℃?
Как изменится равновесие, если при
при 100℃?
Как изменится равновесие, если при
P
= const
повысить температуру? Повысить давление
при
![]() ?
?
Рассчитайте давление над
 при
1000℃.
при
1000℃.
