Гепарин Распространение в природе
Гепарин – природный полисахарид класса сульфатированных гликозаминогликанов. Содержится в тканях млекопитающих: печени, легких, селезенке, почках, коже, в стенках кровеносных сосудов; синовиальной жидкости суставов; стекловидном теле глаза. В живом организме гепарин в свободном состоянии не встречается, поскольку всегда связан с молекулами белка, образуя так называемый углевод-белковый комплекс (протеогликан).
Получение
В организме животных и человека гепарин синтезируется (базофильными) тучными клетками, являющимися разновидностью клеточных элементов соединительной ткани. В связи с этим важнейшим источником для получения гепарина в фармакологических и медицинских целях является ткань легких и печени животных.
В промышленности получают два типа гепарина: высокомолекулярный (ВМГ) инизкомолекулярный (НМГ) гепарины. Производят ВМГ на заводах эндокринных препаратов, как правило, в виде Na-соли. При получении препарата гепарина медицинской степени чистоты применяютпротеолизи обработку основаниями, что приводит к деградации белковой части молекул протеогликанов. Для очистки раствора гепарина используютионообменную хроматографиюилифракционное осаждениеиз водных растворов ПАВ (например, N-ацетилпиридинийхлоридом, ацетилтриметил-аммонийхлоридом).
НМГ получают путем химической или ферментативной деполимеризации ВМГ.Например,далтепаринполучают методом деполимеризации с использованием азотистой кислоты,эноксапарин–методом бензилирования с последующей щелочной деполимеризацией, для получениятинзапаринаиспользуют метод ферментативного расщепления с помощьюгепариназы.
Один из методов получения НМГ заключается в использовании иммобилизованного на силохроме ферментного хитинолитического комплекса из Streptomyces kurssanovii.В процессе используется Na-ацетатный буфер с рН = 7-7.5, температура 40 - 45 С. Продолжительность гидролиза 3 ч. В зависимости от соотношения гепарин/иммобилизо-ванный ферментный комплекс были получены образцы с молекулярной массой от 1.7 до 4.7 кДа, обладающие ингибирующей фактор Ха активностью в 2.0 - 3.7 раз большей, чем у исходного гепарина.
Количественно гепарин определяют фотоколометрически по смещению длины волны максимума поглощения (макс) растворов некоторых красителей (например, азура А) в присутствии гепарина.
Химическое строение и молекулярная структура
Наиболее изучено химическое строение и молекулярная структура макромолекул гепарина различных видов соединительной ткани и некоторых жидкостей организма (синовиальная жидкость суставов, стекловидное тело глаза).
Гепарин – линейный гетерополисахарид, построенный в основном из чередующихся остатков a-D-глюкопиранозилуроновой(глюкуроновой)кислотыи2-сульфамино-2-дезокси-a-D-глюкопиранозы(сульфатированногоN-ацетилглюкозамина), связанныхa-1,4-гликозидными связями.Кроме сульфатных групп гепарин содержит и сульфоэфирные группы (при С6остатков сульфо-N-глюкозамина и, частично, при С2глюкуроновой кислоты). На каждый тетрасахаридный фрагмент приходится приблизительно 5 остатков серной кислоты. Структурная формула гепарина представлена на рис.1.
|
|
|
Рис.1. Структурная формула макромолекулы гепарина. |
Таким образом, гепарин – типичный сополимер, содержащий в составе одной макромолекулы дисахаридные звенья нескольких типов (рис.2).
|
|
|
Рис.2.Повторяющаяся дисахаридная единица высокомолекулярного гепарина. |
Дисахаридной единице гепарина близка по структуре дисахаридная единица гепарансульфата.Отличие этих гликозаминогликанов заключается в следующем: в гепарине большеN-сульфатных групп, а в гепарансульфатеN-ацетильных. Гепарин и гепарансульфат отличаются по локализации и функции в животных тканях. Гепарансульфат в отличие от гепарина содержится в плазматических мембранах различных клеток и в межклеточном веществе.
Изучение структуры гепарина методом ЯМР показало, что звенья остатков глюкуроновой кислоты находятся в макромолекуле в конформации С1 (рис.3).
|
|
|
Рис.3.Энергетически выгодная конформация повторяющейся дисахаридной единицы макромолекулы гепарина. |
По ширине рентгеновских отражений установлено, что молекула гепарина содержит 10 тетрасахаридных повторяющихся единиц.
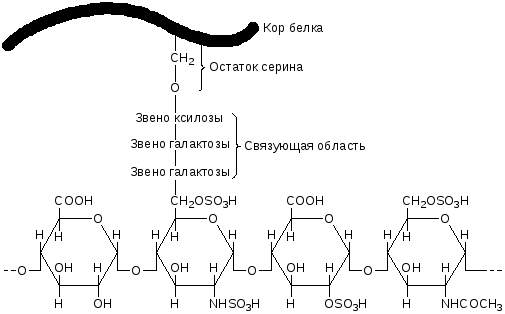
В молекуле нативного гепарина протяженные полисахаридные цепи присоединены к белковой молекуле, которая называетсякором (рис.4).Структура кора определяется местоположением и функциямиуглевод-белкового комплекса в живом организме. Связь белковой и углеводной компоненты осуществляется посредством трисахаридного мостика ксилоза – галактоза – галактоза (рис.4). Белковая часть протеогликана составляет ~5%, углеводная – ~95%.
|
|
|
Рис.4.Структура гепарин-белкового комплекса (протеогликана). |
Препараты низкомолекулярного гепарина (НМГ) различаются по химической структуре, методам получения, периоду полураспада, специфическому действию на организм. Химическая структура некоторых НМГ представлена на рис.5.
|
(а) |
|
|
|
(б) |
|
|
|
(в) |
|
|
|
Рис.5. Химическая структура некоторых низкомолекулярных гепаринов: далтепарин (а), эноксипарин (б), тинзапарин (в). |
Доказано, что ~1/3 молекулы гепарина обусловливает его антикоагулянтную активность. НМГ обладают более широким спектром фармакологических эффектов в сравнении с ВМГ.