
- •Введение
- •1. Основа стехиометрических расчетов
- •2. Расчеты по химическим формулам веществ
- •Методика расчетов по химической формуле вещества
- •3. Расчеты по схемам химических реакций
- •4. Расчеты по уравнениям химических реакций
- •5. Газовые законы
- •6. Химический эквивалент и закон эквивалентов
- •7. Растворы
- •8. Химическая кинетика и равновесие.
- •9. Термохимические расчеты
- •10. Электролиз и окислительно-восстановительные реакции
- •Активность металла возрастает
9. Термохимические расчеты
Любые химические превращения связаны с изменением числа и характера химических связей и поэтому сопровождаются некоторым энергетическим эффектом, проявляющимся чаще всего в форме выделения или поглощения теплоты.
Уравнение химической реакции, записанное с ее тепловым эффектом Qr и указанием агрегатного состояния исходных веществ и продуктов реакции, называется термохимическим уравнением. В школьных задачах знак теплового эффекта обычно указывают в рамках термохимической системы знаков, где экзотермической реакции, идущей с выделением тепла (происходит разогревание реакционной смеси), приписывается положительный тепловой эффект Qr > 0, а эндотермической реакции, идущей с поглощением тепла (происходит охлаждение реакционной смеси), - отрицательный, Qr < 0 .
(В термодинамической системе знаков их выбор противоположен и тепловой эффект реакции в этом случае равен изменению энтальпии:
Hr = Qr (термод.) = – Qr (термохим.)).
Тепловой эффект реакции должен быть обязательно соотнесен со строго определенным количеством исходных веществ, поэтому важно помнить, что в термохимическом уравнении выставляется та его величина, где количества вещества взятых для реакции реагентов (числа молей) равны соответствующим стехиометрическим коэффициентам в уравнении реакции:
3H2(г) + N2(г) = 2NH3(г) + 92,4 кДж,
но 3/2H2(г) + 1/2N2(г) = NH3(г) + 46,2 кДж
Основу
термохимических расчетов составляет
закон Гесса (1826 г.): тепловой эффект
химической реакции зависит только от
состояния исходных и конечных веществ,
но не зависит от пути перехода от
реагентов к продуктам, то есть от числа
и последовательности промежуточных
стадий. Важно помнить, что введение в
исходную реакционную смесь катализатора
приводит к ускорению реакции за счет
изменения ее пути (механизма), то есть
природы промежуточных стадий, но не
изменяет величину теплового эффекта.
Предполагается, что химический процесс
протекает в изобарических условиях (P
= const),
а температура исходной и конечной
реакционной смеси одинакова. В частном
случае, когда Р = 1атм и Т = 298К или 25 0С
(стандартные условия), тепловой эффект
реакции называется стандартным и
обозначается
![]() ,
далее для краткости –Qr.
,
далее для краткости –Qr.
Следствия из закона Гесса:
1) Тепловой эффект обратной реакции равен по величине, но противоположен по знаку тепловому эффекту прямой реакции (закон Лавуазье-Лапласа):
![]() .
.
2)
Величину Qr
можно легко рассчитать на основе молярных
стандартных теплот образования веществ
![]() ,
кДж/моль, которые приводятся в справочниках
или могут быть заданы в условии задачи.
,
кДж/моль, которые приводятся в справочниках
или могут быть заданы в условии задачи.
По определению Qf представляет собой стандартный тепловой эффект реальной или чаще гипотетической реакции образования одного моля сложного вещества из необходимого количества простых веществ, взятых в наиболее устойчивых состояниях при стандартных условиях:
1/2 Н2(г) + 1/2 Сl2(г) = НСl(г) + Qf(HCl) – реальная реакция
К(т)
+ 1/2 Сl2(г)
+ 3/2 О2(г)
= КСlО3(т)
+
![]() (
КСlО3)
–
(
КСlО3)
–
гипотетическая реакция
Теплоты образования простых веществ в их наиболее устойчивых аллотропных модификациях и агрегатных состояниях при стандартных условиях считаются равными нулю.
Итак, для химической реакции:
аА + вВ + … = сС + dD + …
ее тепловой эффект рассчитывают по уравнению:
Qr, кДж = c моль Qf (С) кДж/моль + d Qf (D) + … –
– a Qf(A) – в Qf(В) – …
В условии задачи иногда приводят удельные теплоты образования сложных веществ Q уд.,f[кДж/г] и
Q .f[кДж/моль] =Q уд.,f[кДж/г]М [г/моль].
Понятие “теплота образования” относится не только к обычным сложным веществам, но и к ионам в растворе и эти величины также приводятся в справочниках.
3). Алгебраический метод расчета Qr: если некоторую химическую реакцию можно представить в виде алгебраической суммы реакций с известными тепловыми эффектами, то ее тепловой эффект равен аналогичной алгебраической сумме тепловых эффектов данных реакций.
4). Тепловой эффект реакции Qrравен разности суммы теплот (энергий) образования всех возникающих химических связей в продуктах реакции и суммы теплот (энергий) образования всех разрывающихся химических связей в исходных веществах.
Пример 1. При сгорании одного литра пропана выделяется 23,7 кДж теплоты. Напишите термохимическое уравнение реакции.
Стехиометрическое уравнение горения пропана имеет вид:
С3Н8(г)+ 5 О2(г)= 3 СО2(г)+ 4 Н2О(ж)
В соответствии с ним тепловой эффект реакции Qrдолжен соответствовать сгоранию одного моля или 22,4 л (н.у.) пропана, тогда Qr= 22,4 л23,7кДж/л = 530,9 кДж и термохимическое уравнение имеет вид:
С3Н8(г)+ 5 О2(г)= 3 СО2(г)+ 4 Н2О(ж)+ 530,9 кДж
Пример 2. Окисление углеводов – один из важнейших источников энергии в организме человека.
В аэробных условиях (в организм поступает достаточное количество кислорода) окисление глюкозы идет через цепочку ферментативных реакций и результирующее уравнение имеет вид:
C 6H12O6(т)
+ 6О2(г)
= 6СО2(г)
+ 6Н2О(ж)
+ Qr
6H12O6(т)
+ 6О2(г)
= 6СО2(г)
+ 6Н2О(ж)
+ Qr
Qf, кДж/моль 1274,45 0 393,51 285,84
Согласно следствию из закона Гесса:
Qr = 6 моль 285,84 кДж/моль + 6 393,51 – 6 0 – 1 1274,45 =
= 2801,69 кДж > 0 – это экзотермический процесс.
Обратная реакция отражает эндотермический процесс фотосинтеза и Qr(фотосинтез) = – 2801,69 кДж < 0.
2) В анаэробных условиях (в организме возникает дефицит кислорода, например, при интенсивных физических нагрузках) ферментативное окисление части глюкозы идет до образования молочной кислоты:
С6Н12О6(т)
![]() 2СН3
– СН(ОН) –
СООН.
2СН3
– СН(ОН) –
СООН.
Ее накопление в мышцах вызывает боли и далее она постепенно вымывается в кровь и почти полностью перерабатывается в глюкозу в печени. Анаэробное окисление глюкозы приводит к потерям энергии по сравнению с аэробным.
Определим тепловой эффект последней реакции, если известны тепловые эффекты сжигания одного моля глюкозы (2801,69 кДж) и молочной кислоты (321,21 кДж).
Для расчета будем использовать алгебраический метод:
 1
С6Н12О6
= 2СН3-СН(ОН)-СООН
+ Qr(1)
(I)
1
С6Н12О6
= 2СН3-СН(ОН)-СООН
+ Qr(1)
(I)
+
2 СН3-СН(ОН)-СООН + 3O2 = 3CO2 + 3H2O + Qr(2) (II)

C6H12O6 + 6O2 = 6CO2 + 6H2O + Qr(3) (III)
Итак, (III) = (I) + 2(II),
тогда Qr(3) = Qr(1) + 2 Qr(2) и
Qr(1) = Qr(3) – 2 Qr(2) = 2801,69 – 2 21,21 = 2159,27 кДж
Пример 3. Для реакций, протекающих в растворах, расчет теплового эффекта проводят на основе сокращенного ионного уравнения. Например, реакции нейтрализации сильной кислоты щелочью соответствует ионное уравнение:
 Н+(р-р)
+ ОН–(р-р)
= Н2О(ж)
+ Qr
Н+(р-р)
+ ОН–(р-р)
= Н2О(ж)
+ Qr
Qf, кДж/моль 0 230,02 285,83
Qr = 1 285,83 – 1 230,02 – 1 0 = 55,81 кДж > 0.
Таким образом, реакция нейтрализации является экзотермической, а обратным ей процесс диссоциации Н2О – эндотермический: Qr(дисс.Н2О) = – 55,81 кДж < 0.
Пример 4. Оцените величину теплоты образования связи в молекуле N2, если теплоты образования газообразных аммиака и гидразина равны :
Qf(NH3) = 46,2 кДж/моль, Qf(N2H4) = – 95,4 кДж/моль, а теплота образования связи N – N в N2H4 равна 160 кДж/моль.
В соответствии с определением теплоты образования сложного вещества можно записать следующие термохимические уравнения:
1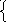 /2N2
+ 3/2H2
= NH3
+ 46,2 кДж
/2N2
+ 3/2H2
= NH3
+ 46,2 кДж
N2 + 2H2 = H2N – NH2 – 95,4 кДж
Выразим тепловые эффекты этих реакций через теплоты образования связей, затем для выделения искомой величины из полученной системы уравнений первое из них умножим на коэффициент 4, второе – на 3 и из первого вычтем второе:
 4
3Q
(N–H)
– 1/2Q
(NN)
– 3/2Q
(H–H)
= 46,2
4
3Q
(N–H)
– 1/2Q
(NN)
– 3/2Q
(H–H)
= 46,2
–
3 4Q (N–H) + Q (N – N) – Q (NN) – 2Q (H – H) = –95,4

Q (NN) – 3 Q (N–N) = 4 46,2 + 3 95,4
или Q (NN) = 4 46,2 + 3 95,4 + 3 160 = 951 кДж/моль
