
- •Росжелдор
- •Введение
- •Демонстрационные тесты
- •Тема 1. Классы неорганических соединений
- •Тема 2. Термодинамика и направленность химических реакций
- •Тема 3. Химическая кинетика
- •Тема 4. Химическое равновесие
- •Тема 5. Строение атома. Периодическая система
- •Тема 6. Химическая связь
- •Тема 7. Растворы неэлектролитов
- •Тема 8. Растворы электролитов
- •Тема 9. Дисперсные системы
- •Тема 10. Окислительно-восстановительные реакции
- •Тема 11. Электрохимические процессы. Гальванический элемент. Коррозия металлов
- •Тема 12. Электрохимические процессы. Электролиз
- •Тема 13. Высокомолекулярные вещества
- •Тема 14. Химическая идентификация
- •Тема 15. Свойства элементов
- •Библиографический список
- •Содержание
- •Доронькин Владимир Николаевич
Тема 2. Термодинамика и направленность химических реакций
2-1. Стандартным условиям соответствуют:
а) Т = 273К, Р = 101325 Па, = 1 моль
б) Т = 273К, V = 1 м3, = 1 моль
в) t = 25˚С, p = 101325 Па, = 1 моль
г) Т = 298˚, p = 101325 Па, = 1 моль
2-2. Термодинамическими функциями являются:
|
а) H – энтальпия |
г) U – внутренняя энергия |
|
б) V – объем |
д) p – давление |
|
в) S– энтропия |
|
2-3. Стандартная размерность энтальпии
|
а) Дж/г |
б) кДж/кг |
в) кДж/м3 |
г) кДж/моль |
д) Дж/мольּК |
2-4. Стандартная размерность энергии Гиббса
|
а) Дж/г |
б) кДж/кг |
в) кДж/м3 |
г) кДж/моль |
д) Дж/мольּК |
2-5. Уравнение 1-го закона термодинамики
|
а) HОБР = –HРАЗЛ |
в) G = H – TS |
|
б) Q = U + АВНЕШ |
г) H = U – pv |
2-6. Функцию «энтальпия» определяет выражение
|
а) HОБР = –HРАЗЛ |
в) G = H – TS |
|
б) Q = U + АВНЕШ |
г) H = U – pV |
2-7. Эндотермическим процессам отвечает неравенство:
|
а) SХР < 0 |
в) HХР > 0 |
д) UХР = 0 |
|
б) HХР < 0 |
г) HХР = 0 |
|
2-8. Изолированные системы
а) не обмениваются ни веществом, ни энергией с окружающей средой
б) обмениваются веществом и не обмениваются энергией
в) обмениваются и веществом, и энергией
г) обмениваются энергией и не обмениваются веществом
2-9. Открытые системы
а) не обмениваются ни веществом, ни энергией с окружающей средой
б) обмениваются веществом и не обмениваются энергией
в) обмениваются и веществом, и энергией
г) обмениваются энергией и не обмениваются веществом
2-10. Система – это группа тел, которые
а) находятся в окружающей среде
б) отделены от окружающей среды поверхностью
в) находятся во взаимодействии и мысленно или фактически обособлены от окружающей среды
г) находятся во взаимодействии, обособлены от окружающей среды и совершают работу против внешних сил
2-11. Функция состояния системы зависит от
|
а) параметров состояния |
в) теплоты и работы |
|
б) пути процесса |
г) теплоты сгорания |
2-12. Реакции, протекающие с поглощением теплоты, называются
|
а) эпизодические |
в) экзотермические |
|
б) эндотермические |
г) эзотерические |
2-13. Энтальпией образования вещества называется тепловой эффект
а) реакции образования этого вещества
б) образования сложного вещества из простых веществ
в) образования 1 моль сложного вещества из простых веществ, устойчивых при стандартных условиях
г) образования сложного вещества из простых веществ, устойчивых при обычных условиях
2-14. Энтальпией сгорания вещества называется тепловой эффект реакции
сгорания
а) 1 моль вещества с образованием оксидов в кислороде при обычных условиях
б) 1 моль вещества с образованием высших оксидов в кислороде при стандартных условиях
в) вещества
г) вещества в воздухе при обычных условиях
2-15. Изохорный процесс протекает при постоянном(ой)
|
а) давлении |
в) объеме |
|
б) количестве вещества |
г) температуре |
2-16. Изобарный процесс протекает при
|
а) постоянном давлении |
в) постоянном объеме |
|
б) постоянном количестве вещества |
г) постоянной температуре |
2-17. Тепловой эффект реакции, в соответствии с законом Гесса, зависит от
а) конечного и начального состояний системы и от пути процесса
б) конечного и начального состояний системы, но не зависит от пути проведения процесса
в) конечного и начального состояний системы и условий проведения процесса
г) условий проведения процесса, но не зависит от начального и конечного состояний системы
2-18. Теплота, подводимая к системе, расходуется на изменение внутренней энергии в
|
а) изохорном процессе |
в) изотермическом процессе |
|
б) изобарном процессе |
г) адиабатическом процессе |
2-19. Самопроизвольное протекание процесса в изолированной системе, в соответствии со 2-м законом термодинамики, сопровождается
а) возрастанием энтропии
б) уменьшением энтропии
в) увеличением энтальпии
г) неизменностью внутренней энергии
д) неизменностью энергии Гиббса
2-20. Самопроизвольное протекание процесса в неизолированной системе сопровождается
а) возрастанием энтропии
б) увеличением энергии Гиббса
в) уменьшением энергии Гиббса
г) неизменностью энергии Гиббса
д) совершением работы против внешних сил
2-21. Условием равновесия является
а) возрастание энтропии
б) увеличение энергии Гиббса
в) уменьшение энергии Гиббса
г) неизменность энергии Гиббса
д) совершение работы против внешних сил
2-22. Теплотой образования CO2 является тепловой эффект реакции
а) Na2CO3(Т) + 2HCl(Г) = 2NaCl(Т) + H2O(Ж) + CO2(Г)
б) 2CO(Г) + O2(Г) = 2CO2(Г)
в) C(Т) + O2(Г) = CO2(Г)
г) C(Т) + 2/3O3(Г) = CO2(Г)
2-23. Экзотермической является реакция
а) BaCO3(Т) = BaO(Т) + CO2(Г); H = 258,7 кДж
б) CaCO3(Т) = CaO(Т) + CO2(Г); H > 0
в) Ca(Т) + 0,5O2(Г) = CaO(Т); H = –645,6 кДж
г) MgCO3(Т) = MgO(Т) + CO2(Г); H = 101,6 кДж
2-24. Первое следствие из закона Гесса: тепловой эффект химической реакции равен
а) разности между суммой теплот образования исходных веществ и суммой теплот образования продуктов реакции
б) разности между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ
в) разности между суммой теплот образования продуктов реакции и суммой теплот сгорания исходных веществ
г) сумме теплот образования продуктов реакции и теплот образования исходных веществ
2-25. Второе следствие из закона Гесса: тепловой эффект химической реакции равен
а) разности между суммой теплот сгорания исходных веществ и суммой теплот сгорания продуктов реакции
б) разности между суммой теплот сгорания продуктов реакции и суммой теплот сгорания исходных веществ
в) разности между суммой теплот образования продуктов реакции и суммой теплот сгорания исходных вешеств
г) сумме теплот сгорания продуктов реакции и теплот сгорания исходных веществ
2-26. Изменение энтальпии реакции сгорания метана CH4 + 2O2 = CO2 + 2H2O рассчитывается по уравнению
|
а)
|
в)
|
|
б)
|
г)
|
2-27. Изменение энтальпии при сгорании ацетилена
2C2H2 + 5O2 = 4CO2 + 2H2O рассчитывается по уравнению
|
а)
|
в)
|
|
б)
|
г)
|
2-28. Энтропия при протекании реакции 4NH3(Г) + 3O2(Г) = 2N2 (Г) + 6H2O(Ж)
|
а) увеличивается |
в) не изменяется |
|
б) уменьшается |
г) зависит от условий проведения реакции |
2-29. Энтропия при протекании реакции 2SO2(Г) + O2(Г) = 2SO3(Г)
|
а) увеличивается |
в) не изменяется |
|
б) уменьшается |
г) зависит от условий проведения реакции |
2-30. Изменение энтальпии реакции:
C2H5OH(Ж) + CH3COOH(Ж) = CH3COOC2H5(Ж) + H2O(Ж)
[![]() ;
;![]() ;
;
![]() ;
]
;
]
|
а) –13 кДж |
б) +13 кДж |
в) –26 кДж |
г) +26 кДж |
2-31. Энтальпия образования HBr
2HBr(Г) = H2(Г) + Br2(Г); H = 72,6 кДж.
|
а) 72,6 кДж/моль |
в) –36,3 кДж/моль |
|
б) 143,2 кДж/моль |
г) –72,6 кДж/моль |
2-32. Энтальпия образования HCl составляет ___ кДж/моль, если при протекании реакции H2(Г) + Cl2(Г) = 2HCl(Г) выделяется 92,31 кДж.
|
а) 92,31 |
б) –92,31 |
в) 46,155 |
г) –46,155 |
2-33. Изменение энтальпии реакции C6H6(Ж) + 7,5O2(Г) = 6CO2(Г) + 3H2O(Г) равно:
[![]() ;
;![]() ;
;![]() ]
]
|
а) +3133 кДж/моль |
в) –3133 кДж/моль |
|
б) +1566,5 кДж/моль |
г) –1566,5 кДж/моль |
2-34. Условие, характеризующее самопроизвольность протекания процессов в неизолированной системе:
|
а) H > 0 |
в) G = 0 |
д) G > 0 |
|
б) H = 0 |
г) G < 0 |
|
2-35. Условие, характеризующее самопроизвольность протекания процессов в изолированной системе:
|
а) H > 0 |
б) H = 0 |
в) S < 0 |
г) S > 0 |
2-36. Изменение энергии Гиббса при протекании химической реакции вычисляется по формуле:
|
а)
|
в)
|
|
б)
|
г)
|
2-37. Формула для расчета изменения энтропии в ходе реакции:
|
а)
|
в)
|
|
б)
|
г)
|
2-38. Самопроизвольные процессы в изолированной системе сопровождаются
|
а) увеличением энтальпии |
в) уменьшением энтропии |
|
б) увеличением энтропии |
г) уменьшением объема |
2-39. Самопроизвольные процессы в неизолированной системе сопровождаются
|
а) уменьшением энергии Гиббса |
в) уменьшением энтропии |
|
б) увеличением энергии Гиббса |
г) уменьшением объема |
2-40. Энергия Гиббса является функцией состояния, и ее изменение равно
а) сумме энергий Гиббса исходных веществ и конечных продуктов
б) разности между суммой энергий Гиббса начальных веществ и суммой энергий Гиббса конечных веществ
в) разности между суммой энергий Гиббса конечных веществ и суммой энергий Гиббса начальных веществ
г) определяется способом проведения процесса
2-41. Энтропия является функцией состояния, и ее изменение равно
а) сумме энтропий исходных веществ и конечных продуктов
б) разности между суммой энтропий начальных веществ и суммой энтропий веществ
в) разности между суммой энтропий конечных веществ и суммой энтропий начальных веществ
г) определяется способом проведения процесса
2-42. Качественно определите: энтропия при протекании реакции
N2(Г) + O2(Г) = 2NO(Г)
|
а) увеличится |
в) равна нулю |
|
б) не изменится |
г) уменьшится |
2-43. Соответствие между словами и цифрами
S
Т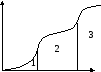
|
1) |
твердое |
а) |
2 |
|
2) |
жидкое |
б) |
1 |
|
3) |
газообразное |
в) |
3 |
|
4) |
ионное |
|
|
2-44. Качественно определите изменение энтропии при протекании реакции 2C4H10(Г) + 13O2(Г) = 8CO2(Г) + 10H2O(Г)
|
а) S > 0 |
б) S < 0 |
в) S = 0 |
г) S 0 |
2-45. Реакции, протекающие самопроизвольно в обратном направлении:
а) CH4(Г) + CO2(Г) 2CO(Г) + 2H2(Г); G = 170,63 кДж
б) Fe2O3(Т) + 3H2(Г) 2Fe(Т) + 3H2O (Г), G = 55,28 кДж
в) 4NH3(Г) + 5O2(Г) 4NO(Г) + 6H2(Г), G = –959,81 кДж
г) CO(Г) + Cl2(Г) COCl2(Г), G < 0
2-46. Самопроизвольно в системе
Fe2O3(Т) + 3H2(Г) 2Fe(Т) + 3H2O (Г), G = 55,28 кДж
будет протекать
|
а) прямая реакция |
в) прямая и обратная реакции равновероятны |
|
б) обратная реакция |
г) химические изменения невозможны |
2-47. Прямая реакция протекает самопроизвольно, если изменение свободной энергии Гиббса равно
|
а) GХР = –190 кДж/моль |
в) GХР = 0 кДж/моль |
|
б) GХР = +190 кДж/моль |
г) GХР = –HХР |
2-48. Качественно определите: энтропия при протекании реакции
2C(Т) + 3H2(Г) = C2H6(Г)
|
а) увеличится |
в) равна нулю |
|
б) не изменится |
г) уменьшится |
2-49. Качественно определите: энтропия при протекании реакции
3Fe(Т) + 2CO(Г) = Fe3C(Т) + CO2(Г)
|
а) уменьшится |
в) не изменится |
|
б) увеличится |
г) равна нулю |
2-50. Изменение энтропии реакции:
2C4H10(Г) + 13O2(Г) = 8CO2(Г) + 10H2O(Г),
если SC4H10 = a, SO2 = b, SCO2 = c, SH2O = d, вычисляется по уравнению
|
а) S = 2a – 13b + 8c – 10d |
в) S = 8c + 10d – 2a – 13b |
|
б) S = 8c + 10d – a – 13b |
г) S = 2a + 13b – 8c – 10d |
_*_ _*_ _*_
2-51. Количество
теплоты, выделяющее при сгорании 16 г
серы, равно ___ кДж (![]() ).
).
|
а) 297 кДж |
б) 594 кДж |
в) 74,25 кДж |
г) 148,5 кДж |
2-52. Количество
теплоты (кДж), выделяемое в организме
при окислении 45 г глюкозы (![]() )
до углекислого газа равно (
)
до углекислого газа равно (![]() и
воды (
и
воды (![]() ),
),
|
а) 700,25 |
б) 2801 |
в) 466,8 |
г) 1400,5 |
2-53. В соответствии с термохимическим уравнением
FeO(Т) + H2(Г) Fe(Т) + H2O(Г), H0 = 23 кДж для получения 560 г железа необходимо затратить ____ кДж тепла.
|
а) 115 |
б) 23 |
в) 230 |
г) 560 |
2-54. При разложении 1 моль CaCO3 поглощается 178,5 кДж теплоты. Объем выделившегося при этом газа равен
|
а) 22,4 л |
б) 11,2 л |
в) 5,6 л |
г) 16,8 л |
2-55. При нагревании 56 г железа с 32 г серы (H0 = –100 кДж/моль) выделяется ___ кДж теплоты.
|
а) 50 кДж |
б) 25 кДж |
в) 100 кДж |
г) 75 кДж |
2-56. При получении 2 моль этанола, согласно термохимическому уравнению C2H4(Г) + H2O (Ж) C2H5OH(Ж), H0 = –44 кДж, выделяется ___ кДж теплоты.
|
а) 88 |
б) 66 |
в) 44 |
г) 22 |
2-57.
При взаимодействии 16 г серы и 11,2 л
водорода выделяется ___ кДж теплоты
(![]() ).
).
|
а) 21 |
б) 5,25 |
в) 42 |
г) 10,5 |
2-58. Если при разложении перхлората калия, согласно термохимическому уравнению KClO4(Т) KCl(Т) + 2O2(Г), H0 = 33 кДж, образовалось 10 моль кислорода, то количество затраченного тепла ____ кДж.
|
а) 66 |
б) 330 |
в) 165 |
г) 132 |
2-59. В соответствии с термохимическим уравнением
CH4(Г) + 2O2(Г) = CO2(Г) + 2H2O(Г), H0 = –802 кДж
для получения 500 кДж теплоты необходимо сжечь ____ л(н.у.) метана.
|
а) 28 л |
б) 42 л |
в) 14 л |
г) 56 л |
2-60. Для получения 1132 кДж тепла по реакции
2NO(Г) + O2(Г) 2NO2(Г), H0 = –566 кДж
необходимо затратить ___ литра(ов) кислорода.
|
а) 22,4 |
б) 11,2 |
в) 44,8 |
г) 56 |
2-61. В системе, находящейся при постоянных давлении и температуре, самопроизвольно могут протекать процессы, для которых
|
а) H > 0 |
б) G > 0 |
в) S < 0 |
г) G < 0 |
2-62. При переходе от кристаллического состояния вещества к газообразному его энтропия
|
а) возрастает |
в) изменяется хаотично |
|
б) уменьшается |
г) остается неизменной |
2-63. Для получения 17 г сероводорода по реакции
H2(Г) + S(Т) = H2S(Г) – 21 кДж требуется затратить ___ кДж теплоты.
|
а) 11,5 |
б) 32,5 |
в) 42 |
г) 21 |
2-64. Для получения 112 г оксида кальция по реакции
CaCO3(Т) = CaO(Т)+ CO2(Г) – 178,5 кДж требуется затратить ___ кДж теплоты.
|
а) 178,5 |
б) 268,8 |
в) 224 |
г) 357 |
2-65. Если энтальпия образования SO2 равна –297 кДж/моль, то количество теплоты, выделяемое при сгорании 16 г серы, равно ___ кДж
|
1) 74,25 |
2) 148,5 |
3) 297 |
4) 594 |
2-66. Термодинамическая функция, характеризующая степень упорядоченности состояния системы, называется
|
а) энтропией |
в) энтальпией |
|
б) теплоемкостью |
г) внутренней энергией |
2-67. Энтальпия образования H2S(Г) равна -21 кДж/моль. При взаимодействии 16 г серы и 11,2 л водорода выделяется ___ кДж теплоты.
|
а) 5,25 |
б) 21 |
в) 10,5 |
г) 42 |
2-68. В изолированной системе самопроизвольно могут протекать процессы, для которых
|
а) S < 0 |
б) S > 0 |
в) G > 0 |
г) H > 0 |
2-69. Для получения 22,4 л (н.у.) аммиака по реакции
N2(Г) + 3H2(Г) = 2NH3(Г) – 92,3 кДж требуется затратить ___ кДж теплоты.
|
а) 92,3 |
б) 139,8 |
в) 69,9 |
г) 46,6 |
