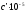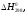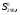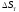- •Курсовая работа по основам физической химии на тему: « Термохимия и химическая термодинамика»
- •Теоретические сведения.
- •Основные понятия
- •Первый закон термодинамики
- •Второй закон термодинамики
- •Третий закон термодинамики
- •Закон Гесса
- •Закон Кирхгофа
- •Энтальпия
- •Энтропия
- •Термодинамические потенциалы. Свободная энергия Гиббса и Гельмгольца.
- •Константа равновесия
- •Расчетное задание
- •Результаты расчета
- •Расчет параметра .
Расчетное задание
Химическая Реакция: 2HJ=J2+H2
Исходное вещество: 2HJ; продукты реакции:H2иJ2.
Справочные данные:
|
Вещество |
Фазовое состояние |
а |
|
|
Дж/моль |
Дж/(моль*К) |
|
H2 |
Газ |
27,28 |
3,26 |
0,502 |
0 |
130,6 |
|
J2 |
Газ |
37,4 |
0,59 |
-0,71 |
62240 |
260,58 |
|
HJ |
Газ |
26,32 |
5,94 |
0,92 |
25940 |
206,3 |
Расчет
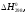
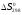 ,
,
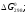

ΔH°298 = ΔH°298 (H2) + ΔH°298 (J2) – ΔH°298 (HJ) = 0 + 62240 – (2· 25940) = 10360 Дж/моль
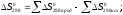
ΔS°298 = ΔS°298 (H2) + ΔS°298 (J2) – ΔS°298 (HJ) = 130,6 + 260,58 – 206,3 = -21,24 Дж/моль·К
ΔG°298=ΔH°298-TΔS°298= 10360 – 298 · (-21,24) = 16743,16 Дж/моль
Расчет
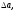
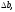
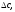
 :
:
Δa= 27,28 + 37,4 - 2·26,32= 12,04;
Δb= (3,26 + 0,59 – 2 · 5,94)10-3= -0,000803 = -0,803 * 10;
Δ’c= (0,502 – 0,71 - 2· 0,92)105= -204800;
ΔC°298=ΣCpпрод– ΣCpисх= Δa+ ΔbT+ Δc’T-2‑= 12,04 + 0,000803 ·298 – 204800/2982= 9,495
Расчет
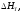
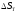 :
:
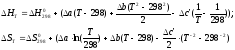
Результаты расчета
|
Термодина-мические параметры |
Размер-ность |
T, K | ||||||
|
298 |
400 |
600 |
700 |
800 |
900 |
1000 | ||
|
|
Дж/моль |
10360 |
11348,59 |
13505,63 |
14608,67 |
15751,526 |
16823,17 |
17928,132 |
|
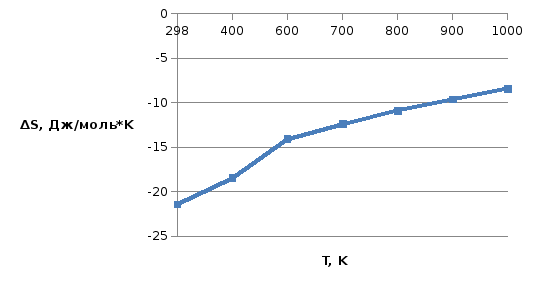
|
Дж/ (моль*К) |
-21,42 |
-18,471 |
-14,1051 |
-12,405 |
-10,926 |
-9,622 |
-8,458 |
|
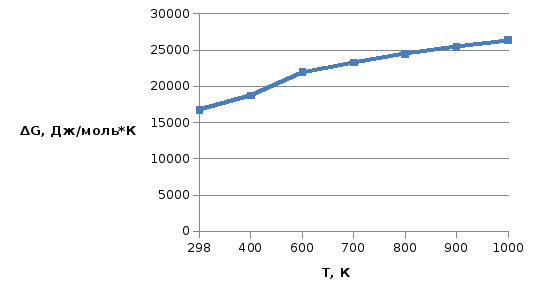
|
Дж/ (моль*К) |
16743,16 |
18736,904 |
21968,71 |
23292,12 |
24492,717 |
25483,21 |
26386,171 |
|
|
- |
-6,761 |
-5,637 |
-4,406 |
-4,004 |
-3,684 |
-3,407 |
-3,175 |
|
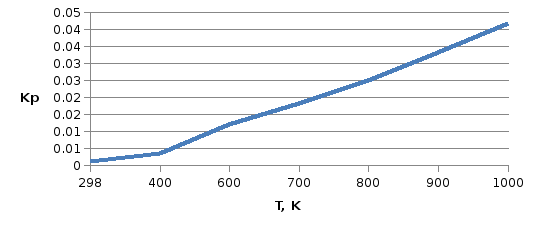
|
- |
1,16·10-3 |
3,56·10-3 |
12,203·10-3 |
18,24·10-3 |
25,12·10-3 |
33,13·10-3 |
41,78·10-3 |
Графики зависимостей:

Расчет параметра .
2HJ = H2 + J2
2(1*β)p (1- β)p (1- β)p
Kp = β2*p2/2(1- β)p = β2*p/2(1- β)= 0,0025117
При p= 1 атм и Т = 800К
β=
При β= 0,9
p =
При p = 5 атм
β=