
Методичка_Громов
.pdf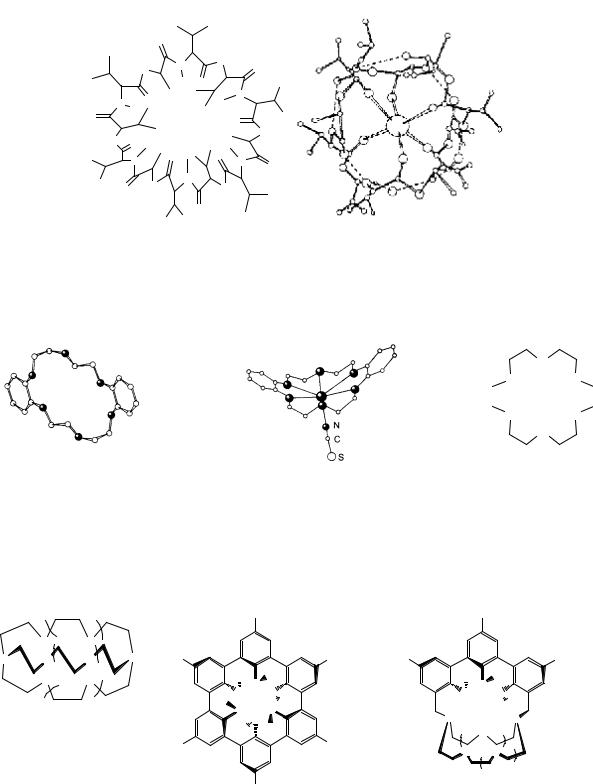
Среди лигандов для катионов можно выделить три класса:
1)природные макроциклы, обладающие свойствами антибиотиков (валиномицин или энниатины);
|
O |
|
|
|
|
|
O |
N |
O |
|
O |
|
|
|
|||
|
|
H |
O |
|
|
N |
H O |
|
H N |
|
|
O |
|
|
|
O |
|
|
|
|
|
O |
|
O |
O H |
|
H |
|
|
O H |
|
|
|||
|
N |
O |
N |
O |
|
|
|
|
|||
|
|
N |
|
|
|
O |
O |
O |
|
|
|
|
|
|
|||
|
|
|
O |
|
|
Рисунок 1 – Валиномицин и его комплекс с K+.
2)синтетические макроциклические полиэфиры, краун-эфиры и их многочисленные производные, а также сферанды;
|
|
|
|
O |
|
|
|
|
O |
O |
|
|
|
|
O |
|
|
|
|
|
O |
||
|
|
|
|
O |
|
дибензо-18-краун-6-эфир |
комплекс дибензо-18-краун-6-эфира с Rb+ |
18-краун-6-эфир |
|||
|
|
|
|
|
|
Рисунок 2 – Макроциклические полиэфиры.
3) синтетические макрополициклические лиганды, криптанды и криптосферанды.
|
|
|
|
|
Me |
|
|
|
Me |
|
|
|
O |
O |
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
N |
O |
O n |
N |
Me |
|
Me |
Me |
|
|
|
Me |
|
O |
O |
|
|
Me O |
Me |
|
|
Me O |
Me |
|
|
|
|
|
|
O |
O |
|
|
O |
O |
|
|
|
m |
|
|
Me |
O Me |
|
|
|
|
Me |
|
|
|
|
|
O |
|
N |
|
|
||
|
криптанд |
|
|
Me O Me |
|
O |
|
N |
|||
|
|
|
|
Me |
|
Me |
|
|
O |
O |
n |
|
|
|
|
|
|
|
|
|
m |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Me |
|
|
криптосферанд |
|||
|
|
|
|
|
|
|
|
||||
сферанд Рисунок 3 – Макрополициклические лиганды.
81
Сделав отступление, можно обратиться к номенклатуре лигандов. Наименования краун-эфиров относительно просты, но они недвусмысленны только тогда, когда имеется в виду использование исключительно этиленгликольных (–OCH2CH2O–) звеньев; в более сложных случаях название сопровождают изображением.
1.Первое число в названии краун-эфира означает число атомов в кольце (в англоязычной литературе обычно дается в квадратных скобках).
2.Второе число показывает число атомов кислорода (или другого донора).
3.Заместители обозначают префиксами: бензо- , дициклогексано- и т.д.
Например, дибензо-18-краун-6-эфир – это краун-эфир с 18-членным макроциклическим кольцом, содержащий 6 атомов кислорода и два бензольных заместителя.
Более обобщенная номенклатура для таких нейтральных органических лигандов была разработана Фегтле и Вебером (1979 г.), и позже модифицирована Крамом (1986 г.). По этой номенклатуре любую моноциклическую систему, в частности, краун-эфир, называют корандом (или коронандом), молекулы с разомкнутой цепью называют подандами; биили олигоциклические системы называют криптандами; жестким системам на основе пара-
метиланизола присвоено название сферанды. |
|
|
|
|
|
|
|
|
|
|||||
|
Открытая цепь |
Циклический лиганд |
Трехмерный лиганд |
|||||||||||
|
|
|
n |
|
D |
D |
|
|
|
D |
|
n |
||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
D |
|
D |
D |
|
|
|
B D |
B |
||||||
|
|
|
|
|
D |
|
|
|
||||||
|
|
|
|
|
|
n |
|
|
|
D |
n |
|||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
Поданд |
|
Коранд |
|
|
|
|
Криптанд |
|||||
|
D – донорный атом |
D = O, краун-эфир |
B – атом в голове мостика |
|||||||||||
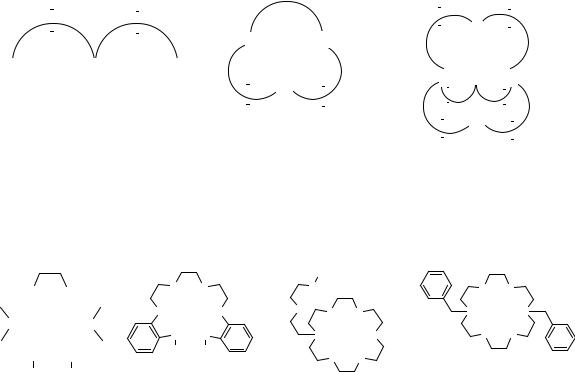
Рисунок 4 – Строение лигандов.
 O O
O O O O
O O
 O O
O O
Me Me
|
|
|
Me |
|
|
|
O |
O |
|
O |
|
O |
O |
O |
O |
O |
O |
O |
N |
N |
O |
O |
|
N |
O |
O |
O |
Me |
Me |
|
O |
O |
|
|
|
|
|
|
|
поданды |
лариат-эфир |
бибрахиальный лариат- |
|
|
эфир |
82
N |
O |
NH HN |
O |
O |
H |
|
|
|
|
O |
HN |
N |
O |
O N |
H |
|
NH HN |
|
|
N |
O |
|
O |
O |
|
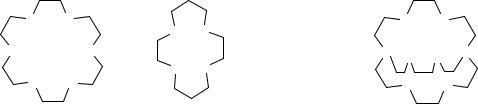
коранды |
[2.2.2]-криптанд |
||
Рисунок 5 – Примеры подандов, корандов и криптандов.
В целом, для чисто кислородных донорных лигандов исторически сложившаяся номенклатура краун-соединений сохранена, но если следовать новой номенклатуре, название «18-краун-6» превращается в «18(O626коранд-6)» или сокращенно «[18]-ан-O6», поскольку коранд рассматривают как большой замещенный циклоалкан. Аналогично будут называться соединения, включающие в состав атомы азота и серы. Для криптандов, имеющих скорее сферическую структуру, используют несколько другую номенклатуру. При этом в названии каждого хозяина указывают число донорных атомов в каждом из мостиков между атомами в головах этих мостиков (например, [2.2.2]-криптанд).
Поскольку номенклатура комплексов должна отличаться от номенклатуры свободных соединений, изначально было принято решение изменять окончание «анд» на окончание «ат» – подат, корат, криптат. Однако, в связи с тем, что суффикс «ат» используют для анионов (ацетат, сульфат), было принять решение заменить «ат» на «плекс» (получаем производное от слова «комплекс» – кораплекс, сфераплекс. В обозначение комплексов включают математический символ « », обозначающий принадлежность к системе.
Поскольку химия катионного комплексообразования положила начало целой области молекулярного распознавания, мы перейдем к обсуждению связывания катионов, и параллельно будем обращать внимание на геометрию лиганда. Основой молекулярного распознавания является сильное, но селективное связывание, то есть успешно подобранный хозяин проявляет сильное сродство именно к отдельно взятому гостю и гораздо меньшее сродство к другим катионам. Конструирование синтетического хозяина, высокоселективного к данному катиону, – очень сложная задача из-за того, что селективность определяется огромным количеством факторов, и самые важные из них – это:
-соответствие между размерами катиона и полости хозяина;
-электростатический заряд;
-растворитель (полярность, водородное связывание, способность к координации);
-степень предорганизации хозяина;
-энтальпийный и энтропийный вклады во взаимодействие катион-хозяин;
83
-свободные энергии сольватации катиона и хозяина;
-природа противоиона и его взаимодействие с растворителем и катионом;
-размер хелатного кольца (мы об этом говорили на прошлой лекции).
O
O O
 O O
O O
|
O |
|
|
K+ |
|
|
O |
|
O |
K+ |
O |
|
|
|
O |
|
O |
|
O |
|
lgK = 6.08
O
O 
N
 O
O
O
O
O
N
 K+
K+
O O

 O
O
O

 K+ N
K+ N
 N
N







 O
O
 O
O
lgK = 4.8
|
O |
|
O |
|
O |
O |
|
O |
|
O |
|
|
K+ |
|
|
O |
|
O |
K+ |
O |
|
|
|
O |
|
O |
|
O |
|
lgK = 5.30
O |
Me |
|
|
|
|
O |
|
|
O |
|
|
O |
|
|
K |
+ |
O |
|
|
|
|
|
O |
Me |
Me |
|
O |
|
Me |
O |
|
O |
K+ |
|
|
O |
|
O |
O |
|
|
N
H
O O
O |
H |
O |
|
|
|
|
N |
|
 K+
K+
NH
 O
O

 K+
K+


 O
O
O

 O
O
NH
lgK = 2.04
|
O |
O |
|
N |
O |
O |
N |
|
O |
O |
|
|
|
K+ |
|
|
O |
O |
|
N |
O K |
+ |
N |
O |
|||
|
O |
O |
|
lgK = 2.3 |
lgK = 10.0 |
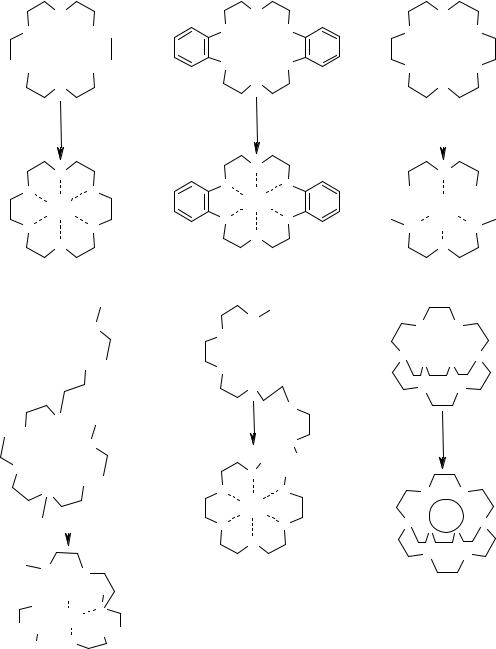
Рисунок 6 – Константы связывания катиона калия с различными лигандами в MeOH.
Обращая внимание на разницу в связывании между подандом и краун-эфиром, нужно учитывать, что ациклический полиэфир способен принимать вытянутую конформацию,
84
предоставляя максимально возможную площадь поверхности для взаимодействия с молекулами растворителя. Десольватация неподеленных электронных пар атомов кислорода
– процесс энергозатратный, и это вносит вклад в значение константы связывания. Способность макроциклов более селективно образовывать более устойчивые
комплексы, чем ациклические лиганды, была названа макроциклическим эффектом. И, несмотря на это, краун-эфиры являются достаточно гибкими макроциклами, поэтому в отношении связывания катионов у них возникает так называемое «плато селективности», поскольку краун-лиганды способны приспосабливаться к различным катионам до некоторой степени независимо от их ионного радиуса. Лариат-эфиры за счет боковой подандной цепи предназначены для придания некоторой трехмерности катионному комплексообразованию, при этом сохраняется высокая скорость комплексообразования, ожидаемая для гибких корандных систем. Таким образом, они сочетают свойства подандов, корандов и криптандов. Особенно интересны бибрахиальные лариат-эфиры с N-прикреплением, так как они способны более точно направить свою боковую цепь к гостю. (В гетеролигандах замена кислорода на донорные функциональные NH или S-группы меняет поведение лиганда, в частности, видно падение константы связывания с калием при введении двух атомов азота в макроцикл за счет уменьшения сродства к калию, в соответствии с теорией жестких и мягких кислот и оснований. Однако, в случае связывания с лариат-эфиром константа возрастает за счет дополнительного трехмерного связывания.)
Таблица 1 – Соотношение между стабильностью и стабилизирующим эффектом комплексов типа «гость-хозяин».
Тип комплекса |
K (MeOH) |
Эффект |
|
|
|
Подат |
102-104 |
Хелатный |
Корат |
104-106 |
Макроциклический |
Криптат |
106-109 |
Макробициклический |
Трехмерные криптанды проявляют предельно высокую селективность. Их макробициклические полости более жестки и ограничены, поэтому они не способны ни достаточно сжиматься для связывания с катионами, слишком малыми для такой полости, ни расширяться, приспосабливаясь к радиусам большим, чем требуется для оптимального связывания. Зато трехмерная полость криптанда гораздо более предорганизована для связывания, поскольку затраты на конформационную перестройку менее значительны. Скорость катионного обмена криптатов на несколько порядков ниже, чем макроциклических
85
комплексов, и обычно уменьшается по мере повышения устойчивости комплекса. Такое поведение лигандов называется криптатным или макробициклическим эффектом.
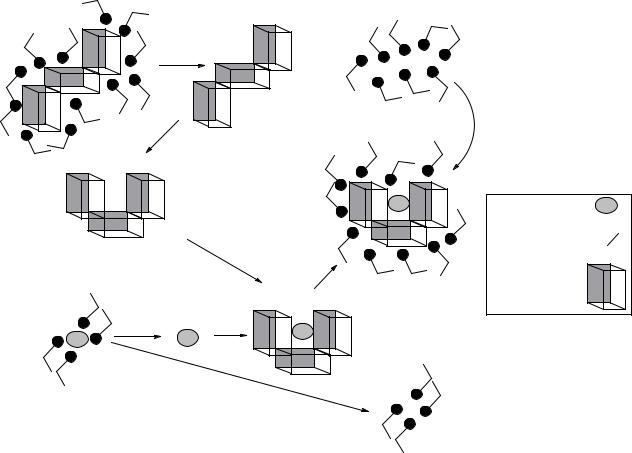
Для понимания роли растворителя при связывании обратимся к схематично представленому процессу комплексообразования гость-хозяин.
1. Сольватированный хозяин |
2. Десольватированный хозяин |
(гидрофобные и ван-дерваальсовы |
и свободный растворитель. |
взаимодействия). |
Энтальпийно затратный, |
|
энтропийно выгодный процесс. |
+
3. Конформационная перестройка хозяина.
Энтальпийно и энтропийно затратный процесс. Не
обязателен для предорганизованного хозяина.
6. Комплексообразование.
Энтальпийно очень выгодный процесс.
Взаимодействия между комплексом и растворителем могут включать как гидрофобные и ван-дер-ваальсовы взаимодействия, так и координационные эффекты.
Катион металла.
Молекула растворителя.  Полярная "головка", гидрофобный "хвост".
Полярная "головка", гидрофобный "хвост". 
Фрагмент хозяина.
7. Растворение комплекса. Энтальпийно выгодный, энтропийно затратный процесс.
4. Сольватированный гость |
5. Десольватация гостя. |
8. Остаточный растворитель |
|
(координационный комплекс) |
не включается во взаимодействие. |
||
Энтальпийно затратный, |
|||
|
Энтропия возрастает. |
||
|
энтропийно выгодный процесс. |
||
|
|
Рисунок 7 – Процесс комплексообразования гость-хозяин.
Часто взаимодействия между растворителем и гостем, а также между растворителем и хозяином имеют тот же тип, что и между гостем и хозяином. Для того, чтобы связать гостя, и хозяин, и гость должны лишиться своих сольватных оболочек. Таким образом, свободная энергия комплексообразования гость-хозяин включает энтальпийный и энтропийный приросты энергии, являющиеся результатом благоприятных взаимодействий между хозяином и гостем, в частности, благодаря высокой степени организации хозяина и ее отсутствию у растворителя. Исходя из свободных энергий связывания ряда хозяев с наиболее комплементарными гостями, семейства соединений в основном располагаются в следующем порядке (по степени уменьшения предорганизации): сферанды > криптасферанды >
86
криптанды > полусферанды > коранды > поданды > растворители. Сравнение кристаллических структур исследуемого сферанда и его очень стабильного сфераплекса с пикратом лития показало, что в обоих случаях хозяин имеет одну и ту же конформацию, то есть он полностью предорганизован к связыванию, и на комплексообразование не требуется никаких энтальпийных затрат.
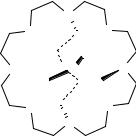
Селективное связывание тетраэдричесаких гостей требует создания молекул-хозяев с тэтраэдрическим центром распознавания. Достичь этой цели можно поместив соответствующие центры связывания в вершинах тэтраэдра и соединив их шестью мостиками. Именно такая структура была реализована в сферическом макроциклическом криптанде «футбольный мяч», в котором четыре атома азота расположены в вершинах тэтраэдра, а шесть атомов кислорода – в вершинах октаэдра (как показано на рис. 8). Этот макроцикл исключительно прочно и селективно (по сравнению со сферическим катионом калия) связывает тетраэдрический катион аммония, образуя криптат аммония. Этот комплекс представляет собой высокоструктурный образец комплементарности хозяина и гостя и их центров взаимодействия.
N
O 
 O
O
N OO
OO  N
N
O 
 O
O
N
Рисунок 8 – Макроциклический криптанд «футбольный мяч».
Ион аммония вписывается в полость рецептора тетраэдрическим «пучком» водородных связей с атомами азота и электростатическими взаимодействиями с шестью атомами кислорода. Прочное связывание в комплексе приводит к тому, что величина pKa для связанного катиона аммония превышает на 6 единиц значение для свободного катиона. Это значит, что депротонирование криптата в 1 млн раз менее вероятно, чем незакомплексованного катиона.
87

N
O H
 O
O

 N+
N+
N H 

 OO H N
OO H N
H
O 

 O
O
N
Рисунок 9 – Связывание катиона аммония криптандами.
Для сравнения можно привести другой макробицикл, который также связывает катион аммония, образуя криптат. Динамические свойства отражают степень комплементарности связывания: в случае соединения «футбольный мяч» катион аммония жестко фиксирован в полости, в этом случае он претерпевает внутреннее вращение.
Коранды, такие как 18-краун-6-эфир и его N-гетероаналоги связывают катионы аммония и алкиламмония с помощью трех водородных связей, давая комплекс типа «насест».
|
Me |
|
R O |
Me |
|
|
N |
H + H N |
|
Водородная |
|
O |
N |
O |
|
H |
|||
связь |
|
|||
|
|
|
N |
|
Me Ион-дипольное
взаимодействие
Рисунок 10 – Связывание катиона аммония гетероаналогом краун-эфира.
Указанный триазакоранд показывает селективность к ионам алкиламмония по сравнению с катионом калия.
При введении в молекулу 18-краун-6-эфира отрицательно заряженных групп, например карбоксигрупп, связывание катиона алкиламмония усиливается за счет укрепления сетки водородных связей электростатическим притяжением между между аммонийным NH3+ и анионным CO2- фрагментом. Такие рецепторы сильно связываются с первичными солями аммония и более селективны к ним по сравнению со вторичными и третичными солями. Это явление называют центральным распознаванием, так как оно включает селективность, возникающую благодаря центральному ядру корандного макроцикла, и позволяет
88
распознавать биологически важные первичные соли аммония, например норадреналин и норэфедрин на фоне их N-метильных аналогов.
Латеральное распознавание
X |
R |
|
X |
|
|
|
|
O |
O |
O |
|
N+ |
Центральное |
||
H |
H |
|
|
O |
H |
O |
распознававние |
|
O |
|
|
X |
|
|
X |
|
|
|
Рисунок 11 – Центральное и латеральное распознавание.
Изменение боковых цепей Х приводит к появлению ряда рецепторов, которые могут быть настроены на селективное связывание именно первичных ионов аммония благодаря специфическим взаимодействиям с заместителем R. Этот вид связывания называют латеральным распознаванием, которое в хорошо сконструированном хозяине комплементарно центральному распознаванию. Увеличение размера рецептора способствует комплексообразованию больших катионов аммония, например ионов гуанидиния.
Для линейного распознавания длины молекул используются дитопные рецепторы – это хозяева, обладающие двумя центрами связывания гостей. По идее, сродство дитопного (или политопного) хозяина к бифункциональному гостю должно быть больше (по крайней мере, в 2 раза), чем сродство монотопного аналога, поскольку происходят два или более случаев распознавания. Кроме того, эффективность селективного молекулярного распознавания можно сильно увеличить за счет размещения и разнесения центров связывания рецептора. При этом дитопные рецепторы могут проявлять макрохелатный эффект, при котором многоточечное (например, макроциклическое) связывание более чем на одном участке больше суммы отдельных взаимодействий.
89

|
N H |
O |
|
|
|
N+H |
O |
R равно: |
|
|
O |
H |
N |
|
|
|
O |
|
|
R |
[CH2]n |
|
|
|
|
|
|
||
|
|
|
|
R |
|
N |
O |
O |
|
|
N+ |
|
||
|
H |
H |
|
|
|
O |
H |
N |
|
|
|
O |
|
|
Рисунок 12 – Линейное молекулярное распознавание.
В 1980 г. Лен синтезировал дитопные хозяева, способные к молекулярному распознаванию катионов диаммония в соответствии с длинной спейсерной группы гостя. Исследования методом ПМР показали, что меньший хозяин (а) проявляет меньшую селективность к гостям. Однако, при связывании гостей с длиной цепи соответственно n = 5, 7 и 10 хозяева (б), (в) и (г) вызывают максимальные изменения химического сдвига протонов цепи гостя по сравнению с аналогами, имеющими как более длинные, так и более короткие цепи. (При нахождении гостя внутри молекулярной полости происходят большие изменения, так как алифатическая цепь гостя попадает в область экранирования кольцевых токов ароматических спейсерных групп.) Интересные результаты были получены при измерении времен релаксации хозяина и гостя. Было показано, что у стерически комплементарных пар гость-хозяин очень сходные движения молекул в растворе, и они значительно более медленные, чем у свободных молекул. Как только соответствие хозяин-гость нарушается, движения становятся анизодинамическими. Это объясняется образованием комплексов другой стехиометрии со связыванием, внешним по отношению к одному из корандных колец.
Поскольку при различных заместителях в тетраэдре соединение становится хиральным, возникает вопрос о селективном хиральном распознавании субстратов. Энантиоспецифическое связывание рецептор-субстрат является крайне важным в биохимических системах. Первый синтетический хиральный коранд был получен в 1978 г.
90
