
Методичка_Громов
.pdf
C |
Th

 C
C
Рисунок 14 – Комплекс Th(0) с циклооктатетраеном, координация π-связями.
Для характеристики способа присоединения так называемого π-лиганда к центральному атому применяется понятие гаптичность. Как и дентатность, оно определяется числом атомов лиганда, непосредственно связанных с центральным атомом. Лиганды, присоединяющиеся одной двойной связью (т.е. двумя атомами, например, этилен), определяют как дигапто-лиганды. Циклооктатетраен – октагапто-лиганд.
Современные методы расчета энергии взаимодействия атомов в молекулах, следовательно, и все характеристики пространственного строения соединений (длины связей, валентные и двугранные углы) основаны на квантовой механике. Общим решением задачи о пространственном строении вещества является вычисление потенциальной поверхности как функции внутренних координат. Но до становления квантовохимических методов для оценки свойств координационных соединений применялись методы, основанные на законах классической физики, в которой электроны, атомы и молекулы рассматривались как тела, движущиеся по законам Ньютона и взаимодействующие между собой по закону Кулона (т.е. основными считались электростатические взаимодействия).
При всем несовершенстве подхода, конструктивной являлясь идея о влиянии соотношения размеров центрального атома и лигандов на состав и относительную устойчивость координационной сферы. Усилиями исследователей В. Косселя, А. Магнуса и Е. Лемберта удалось прийти к понятию критического соотношения радиусов центрального атома и лиганда: ρ =rM:rL. Стабильной координационная сфера может быть лишь при значениях этой величины, находящихся в определенных пределах.
a |
б |
в |
г |
Рисунок 15 – Пространственное расположение лигандов при разных значениях ρ.
31
Наиболее устойчивы соединения, в которых соприкасаются только ионы противоположного знака (а). Структура (б) с меньшим значением ρ менее устойчива из-за более близкого расположения одинаково заряженных лигандов. Структура (в) неустойчива, центральный атом может перемещаться в полости, образованной лигандами, что приведет к образованию более устойчивого комплекса с меньшим к.ч. (г).
Таблица 3 – Интервалы критических соотношений радиусов ионов.
К.ч. |
r = rM : rL |
Геометрическое расположение |
|
|
|
||
|
|
координированных групп |
|
2 |
r < 0,15 |
Прямая линия |
|
3 |
0,15 < r < 0,22 |
Равносторонний треугольник |
|
4 |
0,22 < r < 0,41 |
Тетраэдр |
|
6 |
0,41 < r < 0,73 |
Октаэдр |
|
8 |
0,73 < r < 1,37 |
Куб |
|
|
|
|
Были оценены интервалы значений ρ, допускающие существование комплексов с данным к.ч. Действительно, известно, что в кристаллических галогенидах щелочных металлов литию свойственно к.ч 4 в хлоридах, бромидах и иодидах, а хлоридам, бромидам и иодидам натрия свойственно к.ч. равное 6, и т.д. В таблице приведены значения этих интервалов. Таким образом, простые геометрические соотношения оказались полезными для обобщения большого числа экспериментальных данных по строению кристаллов и молекул координационных соединений.
Таблица 4 – Наиболее стабильные координационные полиэдры.
К.ч. |
|
Координационный полиэдр |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
2 |
гантель |
|
|
|
|
|
|
|
3 |
равносторонний треугольник |
|
|
|
|
|
|
|
4 |
тетраэдр |
|
|
|
|
|
|
|
5 |
тригональная бипирамида |
|
|
|
|
|
|
|
6 |
октаэдр |
|
|
|
|
|
|
|
7 |
одношапочный |
|
одношапочная |
|
пентагональная |
|
||
|
октаэдр |
³ |
тригональная призма |
³ |
бипирамида |
|
||
8 |
квадратная (Архимедова) призма |
> |
Тригональный додекаэдр |
> |
куб |
|||
9 |
трехшапочная тригональная призма |
³ |
одношапочная квадратная антипризма |
|
||||
10 |
двухшапочная |
квадратная |
сфенокорона |
четырехшапочная |
|
|
||
|
антипризма |
|
³ |
³ |
тригональная призма |
|
||
12 |
икосаэдр |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
32
Попытки усовершенствования ионной модели строения комплексов связаны с более точным учетом межлигандных взаимодействий с использованием разных формул типа B/rn, где показатель степени n и константу B выбирали эмпирически. Так определили самые стабильные координационные полиэдры.
Для понимания возможных координационных чисел и координационных полиэдров, образуемых центральным атомом разных групп или центральным атомом в разных степенях окисления используют подход Гиллеспи-Найхолма. Различают связевые и неподеленные электронные пары, взаимное расположение атомов в молекуле определяется количеством образуемых атомом связей и количеством оставшихся неподеленных электронных связей на каждом атоме. Однако, этот подход не применим для комплексов переходных металлов, где центральный атом может содержать как неподеленные пары, так и неспаренные электроны, что не описывается имеющимися структурными типами.
Вообще широкое применение органических лигандов в современной координационной химии стимулирует использование известных концепций органической химии для понимания термодинамики и кинетики реакций комплексообразования. Одна из таких концепций – представление о влиянии пространственных затруднений на протекание реакций и стабильность соединений. Экспериментально установлено, что лиганды с одинаковыми донорными атомами и одинаковым способом координации, но значительно отличающиеся по размерам, могут существенно отличаться по способности образовывать комплексы. Другая концепция – влияние конформационных равновесий органических лигандов. В комплексе лиганд может находиться не в самой выгодной конформации. Образование координационных связей центрального атома с донорными атомами лиганда может потребовать существенной пространственной перестройки лиганда. Энергия комплексообразования при этом уменьшается на величину разности энергий свободного и координированного лиганда. Это может влиять на устойчивость комплексов и их пространственное строение.
Конец двадцатого века ознаменовался принципиально новыми технологическими решениями, и ясной перспективой становится переход к техническим элементам молекулярных размеров. Химические соединения и материалы стали рассматриваться не просто как сырьё, из которого механическими методами изготавливают нужные детали. Химическое соединение становится самостоятельным техническим изделием – магнитом, ячейкой памяти, диодом, транзистором, но в отличие от привычных изделий имеет молекулярные размеры. Координационные соединения находят своё применение в роли таких изделий.
33
|
hν1 |
|
|
|
N |
N |
R |
N |
N |
N Ru2+ N |
N |
Os3+ N |
||
N |
N |
R |
N |
N |
|
|
|
|
|
|
|
R = n-C6H13 |
|
|
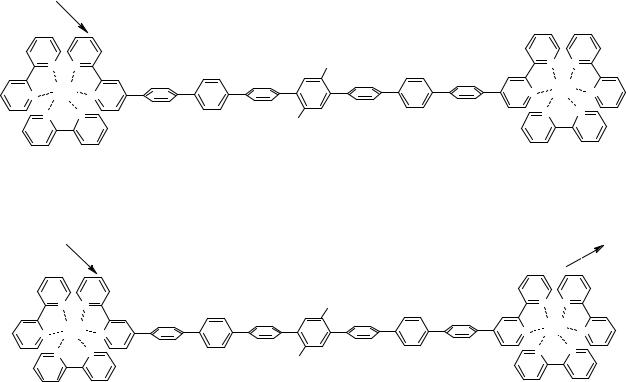
Рисунок 16 – Супрамолекулярная система, выполняющая функцию переносчика электрона.
|
hν1 |
|
|
hν2 |
N |
N |
R |
N |
N |
N Ru2+ N |
N |
Os2+ N |
||
N |
N |
R |
N |
N |
|
|
|
|
|
Рисунок 17 – Супрамолекулярная система, выполняющая функцию переносчика энергии.
Одна из актуальных проблем – эффективное использование солнечной энергии. Вопервых, световая энергия может быть использована (кроме тривиального освещения) для преобразования ее в излучение с нужной частотой. Во-вторых, ее можно преобразовать в электрическую или энергию химических связей.
СПИСОК ЛИТЕРАТУРЫ 1. Илиел, Э. Основы стереохимии / Э. Илиел - М.: Мир - 1971.
2.Скопенко, В.В. Координационная химия / В.В. Скопенко, А.Ю. Цивадзе, Л.И. Савранский, А.Д. Гарновский - М.: ИКЦ «Академкнига» - 2007.
3.Харгиттаи, И. Симметрия глазами химика / И. Харгиттаи, M. Харгиттаи – М.: Мир -
1989.
4. Photochemistry and Photophysics of Coordination Compounds Volume I, II / edited by V. Balzani and S. Campagna - Springer-Verlag Berlin Heidelberg - 2007.
34
Г Л А В А 3. ОСНОВНЫЕ КЛАССЫ ФОТОХРОМНЫХ СОЕДИНЕНИЙ
Под фотохромизмом понимают переход между двумя химическими соединениями A и B с различным поглощением или испусканием при длинах волн λ1 и λ2, который индуцируется действие электромагнитного излучения по крайней мере в одном направлении.
D |
|
λсч(λB) |
|
|
|
A |
λзап(λA) |
|
|
|
hν |
|
A |
B |
|
|
B |
|
|
λ/нм |
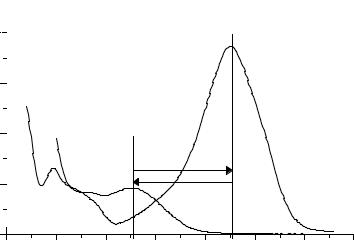
Рисунок 1 – Фотохромная система.
Фотохромные системы характеризуют спектрами поглощения А и В, квантовым выходом перехода А→В (т.наз. светочувствительностью f), временем темновой релаксации τ
(самопроизвольного перехода В→А в отсутствие освещения), квантовым выходом фоторазложения (ϕфр). На рисунке представлен спектр типичного фотохромного соединения: спектр термически стабильной A и фотоиндуцированной B форм. В полосе формы А записывают, а в полосе формы B считывают и стирают информацию. Если соединения А и В поглощают только в УФ-области спектра, то такую разновидность фотохромии называю фототропией.
В может представлять собой одно или несколько термодинамически метастабильных или нестабильных соединений. При переходе А→В изменяется электронная структура хромофора и, соответственно, спектр поглощения соединения, а также другие важные свойства вещества, включая оптические (коэффициет преломления), электрические (проводимость, фотопроводимость), термодинамические (энтальпия образования, температура плавления) и другие характеристики.
Хромофо́ры (греч. chromos – цвет и foreo – несу) – ненасыщенные группы атомов, обуславливающие цвет химического соединения. Хромофорная теория возникновения
35
окраски была предложена в 1878 г. немецким ученым Виттом. К хромофорам относят азогруппу –N=N–, нитрогруппу –NO2, нитрозогруппу –N=O, карбонильную группу =С=О, сопряженные системы двойных связей, хиноидные группировки и др.
Введение других групп, называемых ауксохромами (от греч. auxo – увеличиваю) (– ОН, –NH2 и др.), способствует углублению окраски.)
По способности к обратимости различают:
-фотообратимые системы, когда окрашенная форма В переходит при облучении светом в своей длинноволновой полосе поглощения обратно в бесцветную форму А в результате так называемого оптического отбеливания.
-термообратимые системы, которые спонтанно при комнатной температуре или при нагревании переходят в исходную форму А (т.н. термическое отбеливание).
Часто фотохромные системы могут быть не только фото-, но и термообратимыми, т.е. термотропными.
Dсч
Фотостационарное
состояние
hν |
B ¾¾® A |
A ¾¾® B |
t0 |
|
|
|
|
t1 |
|
|
|
t |
|
|
Экспонирование |
Термическое |
|
|||||||
|
|
|
|
|
||||||
|
|
|
|
|
|
тушение |
|
|
||
Процесс записи |
|
|
|
|||||||
|
|
|
|
|
|
|||||
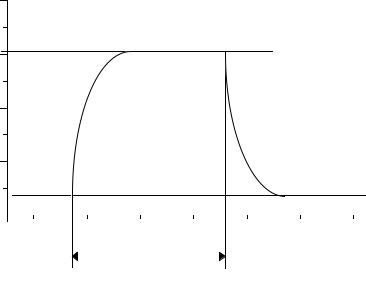
Рисунок 2 – Спектральные изменения фотохромной термообратимой системы.
Если исходная термодинамически стабильная форма A фотохромного соединения поглощает свет в более длинноволновой области спектра, а при облучении или нагревании обратимо переходит в форму В, поглощающую в более коротковолновой области, то такую фотохромию называют инверсионной или обратной. В случае, когда более чем две формы обратимо превращаются друг в друга в результате фотоиндуцированных реакций, говорят о мультифотохромности. Теоретически прямую и обратную реакции можно повторять любое число раз (достигнутое число циклов составляет 106), но на практике многие фотохромные
36
реакции сопровождаются побочными и необратимыми реакциями, в результате чего фотохромное соединение разрушается и говорят, что система «устает».
Фотохромизм можно наблюдать в жидких и твердых растворах, а также в кристаллах разных классов органических и неорганических веществ. При этом природа фотохромных эффектов может быть различной. Наиболее изучены системы, в которых изменение свойств происходит в ходе фотохимической реакции органического соединения. Затем идут системы, которые проявляют фотохромию вследствие триплет-триплетных переходов, затем системы, которые обесцвечиваются высокоинтенсивным лазерным лучом благодаря инверсионной заселенности.
Рассмотрим механизмы, которые лежат в основе превращений наиболее известных фотохромных органических соединений.
Примером процесса с гомолитическим разрывом связи может служить фотолиз гексафенилбисимидазолила, который реагирует по схеме. С относительно высокими квантовыми выходами возникают глубоко окрашенные радикалы А, которые могут
термически рекомбинировать с образованием исходных веществ. |
|
|
||||||||
1. Гомолитический разрыв связи |
|
2. Гетеролитический разрыв связи |
|
|||||||
|
|
A2 |
hν |
2A. |
|
AB |
|
hν |
A+ + B- |
|
|
Ar |
Ar |
|
Ar |
|
Ar3CX |
hν |
Ar3C+ + X- |
|
|
|
ArN |
|
N |
|
|
|||||
N |
N |
|
hν |
2 |
. |
Ar |
|
|
|
|
Ar |
N |
Ar |
|
Ar |
N |
|
|
|
|
|
|
Ar |
|
|
|
|
|
|
|
hν |
|
|
|
Бисимидазолил |
|
|
|
|
+ |
|
||
|
|
|
N O |
NO2 |
|
N O- |
NO2 |
|||
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|
|
|
|
|
|
|
бесцветный |
|
|
голубой |
|
Рисунок 3 – Примеры реакций фотодиссоциации.
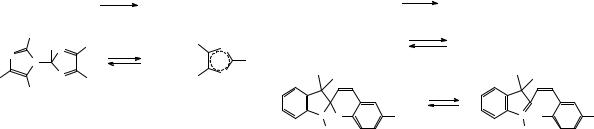
Гетеролитический разрыв связей характерен для соединений типа AB, например, для лейкосоединений триарилметановых красителей Ar3CX (X = CN, OH, SO3H), которые реагируют фото- и термообратимо. Катионы Ar3C+ имеют очень большие коэффициенты экстинкции и полосы поглощения в более длинноволновой области спектра, чем исходные молекулы. Фотохромизм многих производных спиропирана также обусловлен гетеролитическим расщеплением связи С-О. Фотореакция заключается во внутримолекулярном раскрытии гетеролитического кольца.
37
R |
R |
hν1 |
R |
|
R |
+ |
|
N |
+ e- |
||||||
N |
N |
hν2, |
N |
|
|||
R |
R |
R |
|
R |
|
||
|
|
|
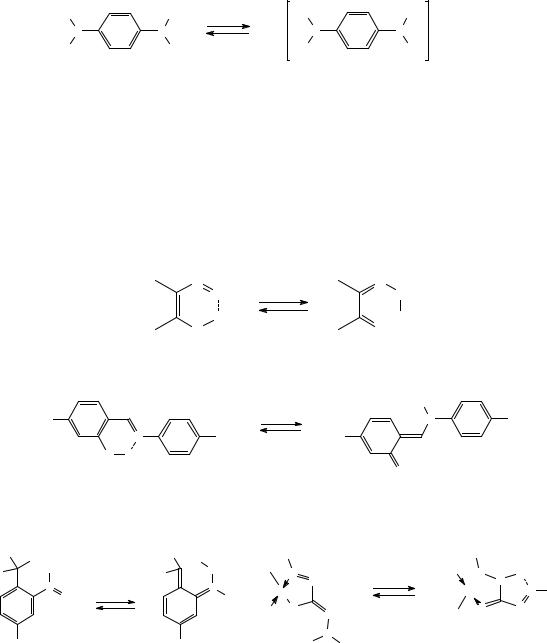
Рисунок 4 – Реакция фотоионизации.
Обратимое изменение цвета может также происходить в результате фотоиндуцированных окислительно-восстановительных (редокс-) реакций. Особый случай редокс-фотохромии – обратимая фотоионизация. Таким образом, из n-фенилендиаминов возникают известные глубоко окрашенные красители типа Вюрстера.
Y |
Z |
hν1 |
Y Z |
|
X |
H |
hν2, |
H |
|
|
|
X |
|
|
X = O, CHR; Y = CH, CR, NO, N; Z = O, N |
|
|||
R1 |
|
hν1 |
H |
|
|
N |
R2 |
||
N |
R2 |
hν2 |
R1 |
|
O H |
|
|
|
|
|
|
|
O |
|
енольная форма |
|
|
кетоформа |
|
кето-енольная
R2 |
R2 |
|
Ar 1 |
|
|
|
Ar 1 |
|
||
1 |
H O- |
1 |
H |
O |
N |
N |
|
|
N N |
H |
R |
N +O |
R |
|
N +O- |
|
hν |
||||
|
|
|
|
|
|
|
||||
|
hν |
|
Hg |
|
|
Hg |
N Ar 2 |
|||
|
|
|
|
|
S |
|
N |
|
S |
N |
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
|
NO2 |
|
|
H |
N |
Ar 2 |
|
|
|
нитро-аци-нитро |
|
|
|
|
|
комплексов металлов |
|
||
Рисунок 5 – Фототаутомерные перегруппировки.
Фотохромизм ряда соединений связан с индуцированным светом перемещением атома водорода – фототаутомерией. Наиболее важные случаи фототаутомерии – кето-енольная, нитро-аци-нитро- и фототаутомерия некоторых комплексов металлов. В первых двух случаях внутримолекулярный сдвиг атома водорода происходит в шестичленном переходном состоянии. Термически стабильны орто-замещенные ароматические соединения, которые в результате облучения дают глубоко окрашенные таутомеры, имеющие хиноидную структуру.
38
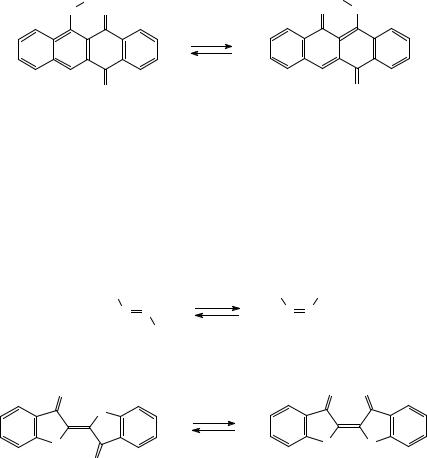
Широко известна фототаутомерия легко доступных анилов ароматических о- гидроксиальдегидов, а также о-нитробензильных производных.
Комбинация фототаутомерии и изомеризации обуславливает фотохромизм дитизонатов Hg(II), Cu(II), Pd(II), Ni(II), Zn(II), Ag(II). Реакция протекает не только в растворах, но и в полимерных пленках при комнатной температуре. Окраска изменяется при этом очень сильно – от желтой до синей. Центральный атом металла определяет фотохимическую стабильность, скорость обратной реакции и цвет комплексов.
O Ar O |
O Ar O |
|
hν1 |
|
hν2 |
O |
O |
Рисунок 6 – Фотоперегруппировки. Фотозамещение.
Интересный тип фотохромии (внутримолекулярное обратимое ароматическое фотозамещение) обнаружен у 6-арилокси-5,12-нафтаценхинона и некоторых аналогичных конденсированных ароматических систем.
R1 |
hν1 |
R1 |
R2 |
|
X Y |
X |
Y |
|
|
hν2 |
|
|||
R2 |
|
|
|
|
транс-изомер |
|
цис-изомер |
|
|
O |
|
|
O |
O |
S |
hν1 |
|
|
|
S |
hν2, |
|
S |
S |
|
|
|||
O |
|
|
|
|
транс-Тиоиндиго |
|
цис-Тиоиндиго |
||
Рисунок 7 – Фотоперегруппировки. Фотоизомеризация.
Фотохимическая транс-цис-изомеризация обусловлена затрудненным вращением вокруг двойной связи и является причиной фотохромных изменений в целом ряде органических соединений. В силу малого отличия электронных структур исходных и конечных продуктов, спектральные изменения в этом случае менее значительны. Обычно транс-форма термодинамически более стабильна.
39
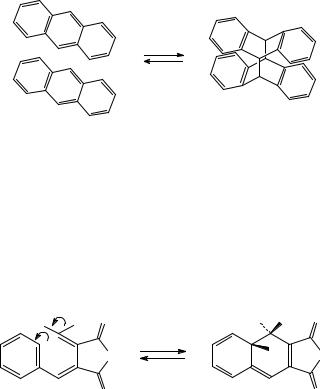
При X=Y=N общая формула соответствует фотохромным азасоединениям, триазенам и некоторым другим группам соединений. При X=CR и Y=N – анилам и азометинам, азинам, формазанам и некоторым другим фотохромным красителям. При X=Y=CR формула соответствует фотохромным этиленам, стильбенам, стириловым красителям, индигоидным красителям.
Перициклическими называют синхронные реакции, переходное состояние которых может быть представлено в виде цикла. К этой категории относят следующие типы реакций:
1.Реакции циклоприсоединения, приводящие к образованию циклических молекул из двух независимых непредельных (в том числе сопряженных) π-электронных систем путем образования двух новых σ-связей между их концевыми атомами. Обратные реакции этого типа называют циклораспадом.
hν1
hν2
Рисунок 8 – Циклоприсоединение антрацена.
2.Электроциклические реакции, включающие образование новой σ-связи между концевыми атомами нециклической сопряженной π-электронной системы в результате участия двух её р-электронов (или обратные процессы раскрытия цикла).
R R' O |
|
R R' O |
|
O |
hν1 |
H |
O |
|
|||
hν2 |
|
||
|
|
|
|
O |
|
|
O |
Рисунок 9 – Электроциклическая реакция фульгида.
3.Сигматропные сдвиги, представляющие собой перегруппировки сопряженных нециклических π-электронных систем, которые происходят путем внутримолекулярного перемещения одной из имеющихся σ-связей от одного из концевых атомов молекулы к другому её концевому атому.
40
