
Методичка_Громов
.pdf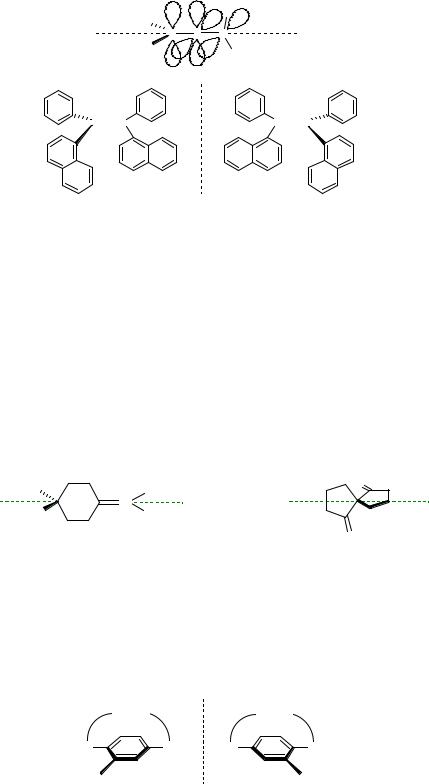
B |
A |
|
C C |
||
C |
||
A |
Ось хиральности |
|
B |
||
|
C=C=C |
C=C=C |
Зеркало
Рисунок 6 – Энантиомеры 1,3-ди(1-нафтил)-1,3-дифенилаллена.
Примерами таких молекул являются 1,2-диеновые углеводороды – в них соседние π- связи располагаются во взаимно перпендикулярных плоскостях. Асимметрия в молекулах алленов возникает тогда, когда по разные стороны оси хиральности располагаются разные группировки атомов.
Осевой хиральностью обладают также производные циклоалканов, имеющих экзоциклическую двойную связь, и производные спироуглеводородов.
H |
COOH |
O |
H3C |
C |
|
H |
|
O
4-метилциклогексилиденуксусная кислота
(+)-спиро[4,4]нонандион-1,6
Рисунок 7 – Соединения с осевой хиральностью.
2) Макроциклические эфиры гидрохинона – анса-соединения (от франц. аnse – петля) –
пример соединений с планарной хиральностью.
|
(CH2)8 |
|
(CH2)8 |
O |
O |
O |
O |
H3C |
|
|
CH |
|
|
|
3 |
Зеркало
Рисунок 8 – Анса-соединения.
Хиральность молекул анса-соединений обусловлена тем, что в них затруднен или вообще невозможен поворот бензольного кольца вокруг находящихся в пара-положении относительно друг друга σ-связей макроцикла.
11
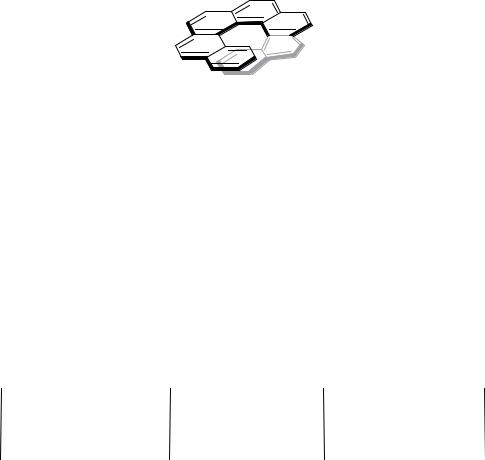
3) Гептагелицен служит примером соединения со спиральной хиральностью. В молекулах этого соединения конденсорованные бензольные кольца не могут расположиться в одной плоскости и образуют витки левоили правозакрученной спирали.
Рисунок 9 – Гептагелицен.
Гелицены имеют удивительно большое удельное вращение, что обусловлено хиральным хромофором – сопряженной системой из конденсированных бензольных колец.
Переходя к диастереомерам, следует отметить, что различают σ- и π-диастереомеры.
В виде σ-диастереомеров могут существовать соединения, молекулы которых имеют два или более центров хиральности. С увеличением числа асимметрических атомов углерода число стереоизомеров удваивается с появлением каждого нового центра хиральности и может быть вычислено по формуле N = 2n, где N – число стереоизомеров, n – число центров хиральности.
|
COOH |
|
|
COOH |
|
|
COOH |
|
|
COOH |
||||||||
H |
|
|
OH |
HO |
|
|
H |
H |
|
|
OH |
HO |
|
|
|
H |
||
|
|
|
|
|
|
|||||||||||||
H |
|
|
Cl |
Cl |
|
|
|
H |
Cl |
|
|
|
H |
H |
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
||||||||||
|
COOH |
|
|
COOH |
|
|
COOH |
|
|
COOH |
||||||||
|
|
|
|
|||||||||||||||
(2S,3S)-, эритро-форма |
(2R,3R)-, эритро-форма |
(2S,3R)-, трео-форма |
(2R,3S)-, трео-форма |
|||||||||||||||
|
|
|
|
|||||||||||||||
[α]D20 –31,3°, т.пл. 173°С |
[α]D20 +31,3°, т.пл. 173°С |
[α]D20 +9,4°, т.пл. 167°С |
[α]D20 -9,4°, т.пл. 167°С |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рисунок 10 – Изомеры 2-гидрокси-3-хлорбутандиовой кислоты.
Если в проекционных формах одинаковые заместители (атомы водорода) находятся по одну сторону вертикальной линии проекции Фишера, такие стереоизомеры называют эритро-формами, а если по разные – трео-формами.
Диастереомеры отличаются температурами плавления и кипения, имеют разную плотность, показатели преломления, растворимость, дипольные моменты. Оптическая активность диастереомеров отличается по знаку и величине угла. Из диастереомеров могут образовываться разные по стороению вещества.
12
|
1CH OH |
|
|
1CH OH |
|
1CH OH |
|
|
1CH OH |
|
||||||||
|
|
2 |
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
2 |
|
|
HO |
2 |
|
|
H |
H |
|
2 |
|
|
OH |
H |
2 |
OH |
H |
|
2 |
OH |
|
3 |
|
|
|
3 |
|
|
3 s |
|
3 r |
s |
||||||||
H |
|
|
|
OH |
HO |
|
|
|
H |
H |
|
OH |
HO |
|
H |
|
||
4 |
|
|
4 |
|
|
4 |
4 |
|
||||||||||
H |
|
|
OH |
HO |
|
|
H |
H |
OH |
H |
OH |
|
||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
5CH OH |
|
|
5CH OH |
|
5CH OH |
|
|
5CH OH |
|
||||||||
|
|
2 |
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
2 |
|
|
|
|
|
|
Зеркало |
L-арабит |
|
рибит |
|
|
|
ксилит |
|
|
|||||
|
D-арабит |
|
|
|
|
|
|
|
|
|||||||||
Рисунок 11 – Образование разных веществ из диастереомеров (рибит и ксилит – мезо- формы).
Если асимметрические атомы углерода имеют одинаковое окружение, то число изомеров становится меньше чем 2n, так как возникает плоскость симметрии, и соединение становится оптически неактивным. Такие соединения называют мезо-формами.
В виде π-диастереомеров могут существовать алкены и их производные с общей формулой ABC=CDE, где возникают условия неидентичности лигандов, то есть A ¹ B, D ¹ E.
B
A 


 A
A 



 A
A
C C 
 C
C  C
C
B B B
A
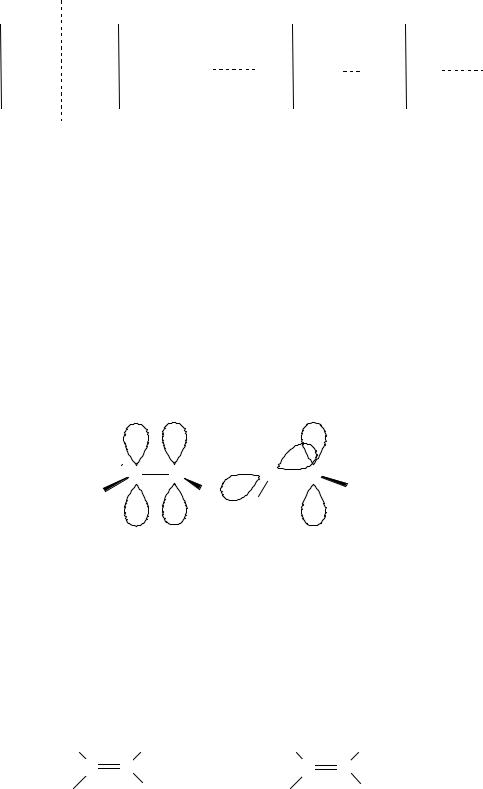
Рисунок 12 – p-Диастереомеры.
Эти изомеры отличаются друг от друга различным расположением лигандов относительно плоскости p-связи и существуют потому, что свободного вращения вокруг двойной связи не происходит, иначе нарушилась бы p-связь. Для их обозначения используют префиксы цис- и транс-.
H |
H |
H |
C2H5 |
C |
C |
C |
C |
H5C2 |
C2H5 |
H5C2 |
H |
цис-гексен-3, т.пл. –138 °С, |
транс-гексен-3, т.пл. –114 °С, |
т.кип. 66.4 °С |
т.кип. 67.1 °С |
Рисунок 13 – Сравнение цис- и транс-изомеров гексена.
13
У цис-изомеров одинаковые заместители расположены по одну сторону плоскости симметрии, у транс-изомеров – по разные стороны. Молекулы π-диастереомеров ахиральны
(есть как минимум одна плоскость симметрии, в которой лежат σ-связи атомов углерода).
H3C |
COOH |
Br |
C |
C |
C |
C |
H3CH2C |
H |
Cl |
|
Cl
CH2CH2CH3
(E)-3-метилпентен-2-овая кислота (Z)-1-бромо-1,2-дихлорпентен-1 Рисунок 14 – Примеры E- и Z-изомеров.
Если заместители разные, то для обозначения используют E,Z-систему согласно принципу старшинства заместителей (от нем. zusammen – вместе, entgegen – напротив).
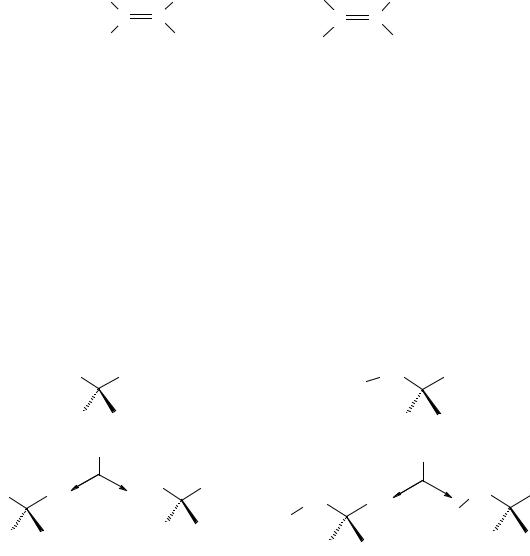
Важной характеристикой лигандов является топизм. Topos в переводе с греческого значит «место». Мы говорим о «дитопных» лигандах, в которых есть два места связывания, об удачной топологии. Кроме этого, два одинаковых заместителя в молекуле могут быть гомотопными (если реакция по любому из них приводит к одному и тому же веществу),
энантиотопными (если образуются энантиомеры) и диастереотопными.
|
H3C |
|
CH3 |
|
|
H3C |
H2C |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
H |
a |
Hb |
|
|
|
Ha |
H |
|
|
|
|
|
|
|
b |
|
||
|
|
пропан |
|
|
|
бутан |
|
||
|
|
|
|
|
|
|
|
||
H3C |
CH3 |
|
H3C |
CH3 |
H2C |
|
CH3 |
H2C |
CH3 |
|
|
|
|
||||||
|
|
|
|
|
|
H3C |
|
||
|
|
|
|
|
H C |
|
|
|
|
|
|
|
Ha |
Br |
3 |
|
|
|
|
Br |
Hb |
|
|
|
|
Ha |
OH |
||
|
|
|
HO |
|
Hr |
||||
|
|
|
|
|
|
|
|
||
идентичные структуры 2-бромпропана |
(S)-бутанол-2 и (R)-бутанол-2 |
|
|
Рисунок 15 – Установление характера топических отношений в молекуле. |
|
Диастереотопные протоны имеют разные сигналы в спектрах ПМР. Еще говорят, что эти протоны неэквивалентны.
Аналогичные топические взаимоотношения можно проследить в плоских молекулах.
14
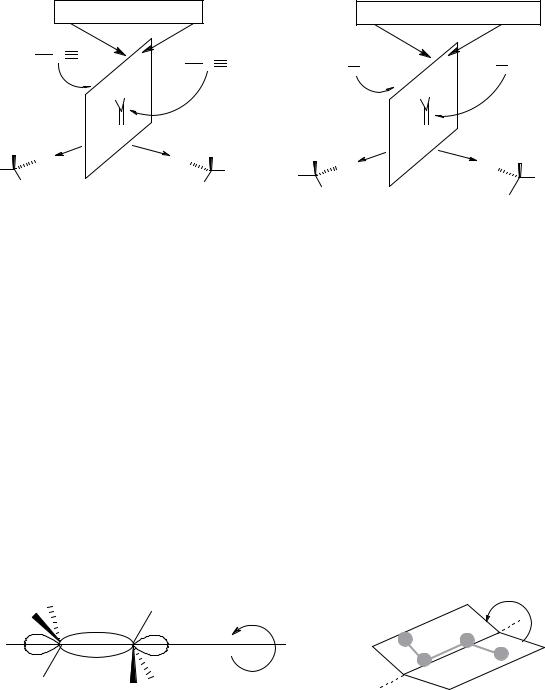
|
Гомотопные поверхности |
|
|
Энантиотопные поверхности |
|||
H C N |
|
|
|
re-сторона |
|
si-сторона |
|
H C |
N |
|
Br Br |
Br |
Br |
||
|
|
|
|||||
|
H C |
CH |
|
|
H CH |
|
|
|
3 |
|
|
3 |
|
|
|
|
3 |
|
|
|
|
|
|
|
|
O |
|
|
CH2 |
|
|
CH3 |
CH3 |
CH |
|
H |
|
H |
|
CN |
H C |
3 |
|
H C |
|||
|
3 |
NC |
Br |
CH3 |
Br |
||
OH |
HO |
CH2Br |
3 |
||||
|
|
BrCH |
|||||
идентичные 2-гидрокси-2- |
|
|
|
|
2 |
||
|
(R)-1,2-дибромопропан |
(S)-1,2-дибромопропан |
|||||
|
метилпропанонитрилы |
|
|
энантиомеры |
|
||
Рисунок 16 – Топические взаимоотношения в плоских молекулах.
Соответственно получаемым в реакциях соединениям, различают гомотопные (при воздействии реагента с разных сторон плоскости получают идентичные соединения), энантио- и диастереотопные поверхности.
Конформация определяется как любое относительное положение атомных ядер в молекуле, при котором сохраняется ее целостность, то есть конфигурация. Конформационные изомеры неотделимы друг от друга и сосуществуют в едином множестве геометрических форм, возникающих в результате перемещения ядер атомов в молекуле относительно друг друга.
Ось симметрии |
ϕ |
s-связи |
|
Ось вращения
Рисунок 17 – Возникновение конформаций.
Одной из причин возникновения конформаций является вращение вокруг одинарных осей. σ-Связь симметрична относительно оси, проходящей через ядра связанных атомов, поэтому при повороте одного фрагмента относительно другого связь не нарушается. Характеристикой конформации является торсионный угол.
Конформации ациклических систем. Простейшая молекула, для которой возможно существование конформаций – этан. В результате поворота возникает бесконечное множество конформаций, шесть из них с торсионными углами, кратными 60°.
15
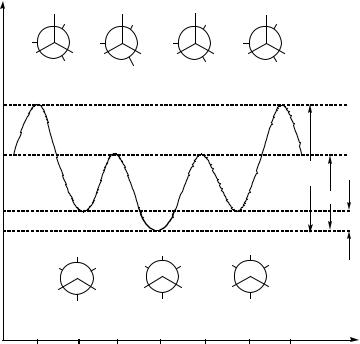
Три заслоненных (они соответствуют максимумам на энергетической кривой и неустойчивы из-за отталкивания электронных оболочек противостоящих связей – торсионного напряжения) конформации и три заторможенных – соответствуют минимумам на энергетической кривой. Конформации с равной потенциальной энергией называются вырожденными. Отдельные относительно устойчивые конформации называют
конформерами.
Е, кДж/моль |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
CH3 |
|
|
CH3 |
|
CH3 |
|
|
CH3 |
|
H |
|
|
H |
|
CH3 |
|
H |
|
H |
|
H3C |
|
|
H |
|
|
H |
H |
H |
H |
H |
|
H |
H |
H |
|
|
H |
|
CH3 |
|
|
H |
|
H |
|
синперипланарная |
|
|
|
синперипланарная |
|||||
антиклинальные |
|||||||||
|
|
|
|
|
|
|
|
|
25,5 |
|
|
|
|
|
|
|
|
|
14,5 |
|
|
|
|
|
|
|
|
|
3,5 |
|
CH3 |
|
|
CH3 |
|
|
CH3 |
|
|
|
H |
CH3 |
H |
|
H |
CH3 |
H |
|
|
|
H |
H |
H |
|
H |
|
H |
H |
|
|
H |
|
|
CH3 |
|
|
H |
|
|
синклинальная |
антиперипланарная |
синклинальная |
|
||||||
0 |
60 |
120 |
180 |
|
240 |
300 |
360 |
ϕ, град |
|
|
|
||||||||
Рисунок 18 – Изменение потенциальной энергии в процессе конформационных превращений бутана.
Например, для бутана наиболее энергетически выгодной является антиперипланарная конформация, где метильные группы максимально удалены друг от друга. В синклинальной (скошенной, гош-) конформации отсутствует торсионное напряжение, но сохраняется ван- дер-ваальсово.
Конформации циклических систем. Циклы, построенные только из тетраэдрических атомов углерода или содержащие гетероатомы (за исключением трехчленных) – неплоские, и существуют в виде разнообразных конформаций. Своеобразие этих переходов в том, что они протекают синхронно и согласованно.
16
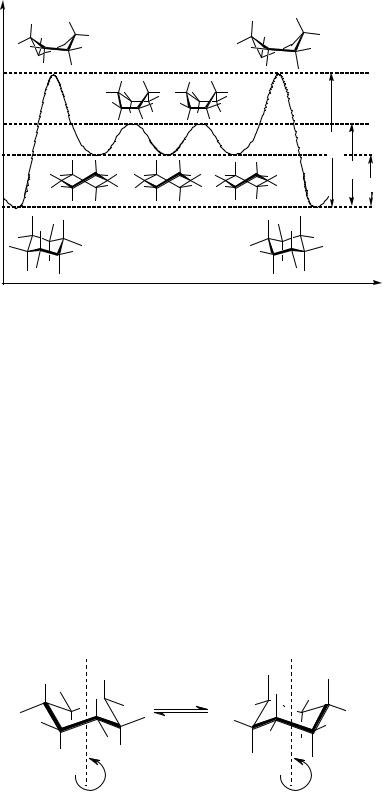
Е, кДж/моль |
46,0 |
23,0 |
19,9 |
Координата реакции |
Рисунок 19 – Энергетическая характеристика конформаций циклогексана.
Наиболее полно исследованы конформационные переходы циклогексана, рассмотрим их подробнее. Наиболее устойчивой конформацией является «кресло» (это было установлено в начале прошлого века методом РСА), минимуму на энергетической кривой также соответствует конформация искаженной ванны (или «твист»), конформации «ванна» и «полукресло» соответствуют максимумам на кривой, и их следует рассматривать как переходные состояния между более устойчивыми конформациями.
Конформация кресла наиболее симметричная, каждый атом углерода имеет по две неэквивалентные связи С–Н. Связи, расположенные параллельно вертикальной оси симметрии третьего порядка, называют аксиальными (а), а ориентированные по углом 109.5° к этой оси называют экваториальными (е).
Ha |
Ha |
|
|
|
|
|
Ha |
|
He |
He |
|
|
|
He |
He |
He |
|
|
|
|
|||
Ha |
|
|
|
||
|
|
He |
|
||
Ha |
|
|
|
||
Ha |
|
|
|
|
|
|
C3 |
|
|
C3 |
|
Рисунок 20 – Инверсия цикла.
В процессе конформационных превращений аксиальные заместители становятся экваториальными и наоборот – это называется инверсией. Конформации замещенных
17
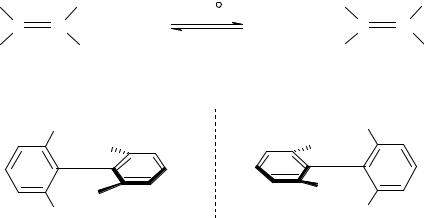
циклогексанов энергетически неэквивалентны – термодинамически более выгоден экваториальный конформер. Причина этому – взаимное отталкивание объемистых заместителей, находящихся в пространственно сближенных положениях.
Следует отметить, что деление стереоизомеров на конфигурационные и конформационные весьма условно. В одних условиях соединение может быть конфигурационно устойчивым, а в другом температурном интервале оно быстро превращается в другой стереоизомер, и эту пару изомеров уже следует считать конформерами.
H3C |
COOH |
200 |
C |
HOOC |
COOH |
|
C |
C |
C |
C |
|||
|
|
|||||
HOOC |
H |
|
|
H |
H |
|
фумаровая кислота (транс-изомер) |
|
|
малеиновая кислота (цис-изомер) |
|||
|
COOH |
|
|
HOOC |
|
|
|
HOOC |
|
|
COOH |
|
|
|
O2N |
|
|
NO2 |
|
|
|
COOH |
|
|
O2N |
|
|
Зеркало
энантиомеры 6,6’-динитробифенил-2,2’-дикарбоновой кислоты Рисунок 21 – Устойчивые стереоизомеры.
Однако, существуют конфигурационно устойчивые стереоизомеры, которые в традиционном понимании следовало бы считать конформерами. Например, π-диастереомеры малеиновая и фумаровая кислота; атропоизомеры (в которых конфигурационная стереоизомерия обусловлена торможением внутреннего вращения вокруг σ-связи), и уже упоминавшиеся анса-соединения (в которых устойчивость зависит от размера макроцикла, т.е. 10 и более атомов углерода в полиметиновой цепи – это уже конформеры, т.к. бензольное кольцо с заместителем свободно прокручивается через макроцикл).
Одно из интересных направлений – это создание хиральных поверхностей. Энантиоселективные химические технологии требуют присутствия хиральной среды.
18

Рисунок 22 – СТМ-изображение двумерных повержностей R,R- (слева) и S,S-битартрата (справа), адсорбированных на поверхности меди.
Учитывая важную роль, которую поверхности играют во многих химических процессах (адсорбция, катализ, кристаллизация и т.д.), есть весомая причина разрабатывать такие поверхности и изучать их энантиоселективность. Недавно было показано, что хиральные шаблоны, созданные с помощью адсорбции, могут удерживаться межмолекулярными водородными связями. Разработка этого направления ведет к созданию высокоорганизованных димерных поверхностей с предсказуемой точностью.
СПИСОК ЛИТЕРАТУРЫ
1.Органическая химия. Основной курс. / под ред. Н.А. Тюкавкиной – М.: Дрофа - 2002.
2.Реутов, О.А. Органическая химия / О.А. Реутов, А.Л. Курц, К.П. Бутин - М.: Бином - 2005.
ГЛ А В А 2. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ СОЕДИНЕНИЙ АЗОТА И
КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ
Для продолжения изучения пространственного строения соединений вспомним названия некоторых функциональных групп и соответствующих им органических соединений.
19
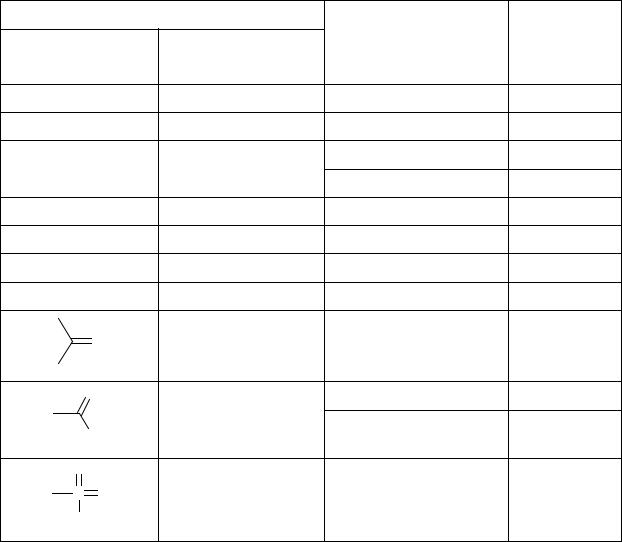
Таблица 1 – Некоторые функциональные группы и соответствующие классы органических |
||||
соединений. |
|
|
|
|
Функциональная группа |
Название класса |
Общая |
||
Формула |
Название |
|
формула |
|
|
|
|
|
класса |
___ |
|
___ |
Углеводороды |
R-H |
-F, -Cl, -Br, -I (-Hal) |
Галогены |
Галогенопроизводные |
R-Hal |
|
|
|
|
Спирты |
R-OH |
-OH |
|
Гидроксильная |
Фенолы |
Ar-OH |
-O- |
|
Окси |
Простые эфиры |
R-O-R’ |
-SH |
|
Меркапто |
Тиолы |
R-SH |
-NH2 |
|
Амино |
Амины (первичные) |
R-NH2 |
-NO2 |
|
Нитро |
Нитросоединения |
R-NO2 |
O |
Карбонильная |
Альдегиды |
R-CH=O |
|
|
|
|||
O |
|
|
Кетоны |
R-CO-R’ |
OH |
Карбоксильная |
Карбоновые кислоты |
R-COOH |
|
|
|
|
||
O |
|
|
|
|
S |
O |
Сульфо |
Сульфоновые кислоты |
R-SO3H |
OH |
|
|
** |
|
*Аr – ароматический заместитель. |
|
|
||
**то же, что и сульфокислоты. |
|
|
||
Согласно концепции гибридизации, sp3-гибридизованные орбитали придают молекуле тетраэдрическую конфигурацию, sp2-гибридизованные – плоскую форму, а spгибридизованные орбитали, называемые «диагональными» - линейную форму.
Кроме углерода, существуют и другие элементы, образующие соединения со структурой Xabcd, которые могут быть получены в оптически активной форме.
20
