- •Алициклические углеводороды
- •Моноциклические насыщенные углеводороды (циклопарафины, циклоалканы, полиметиленовые углеводороды)
- •Номенклатура циклопарафинов
- •Изомерия циклопарафинов
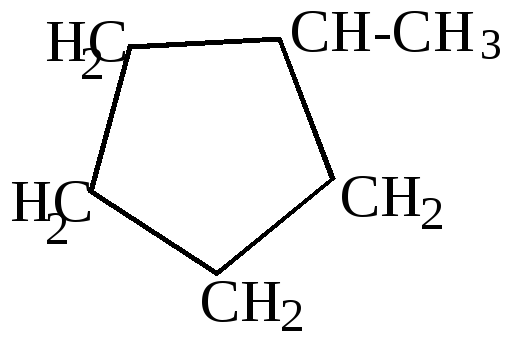
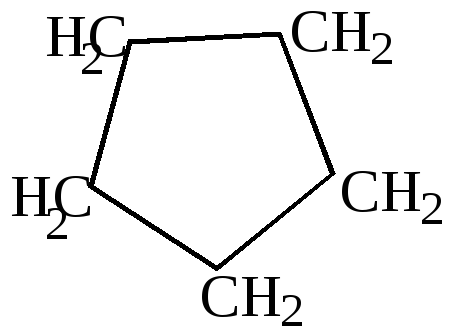
- •Соединения с четырех- и пятичленными кольцами
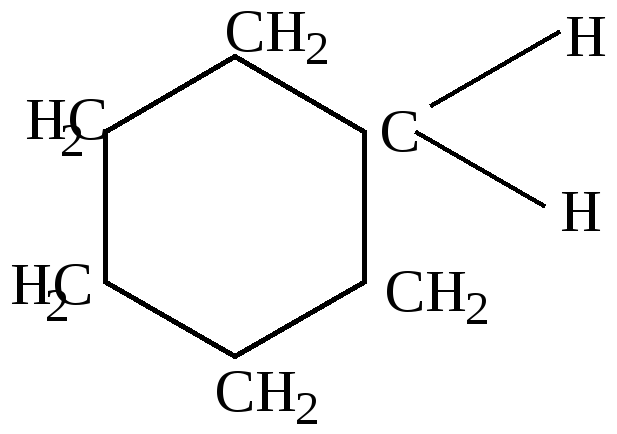
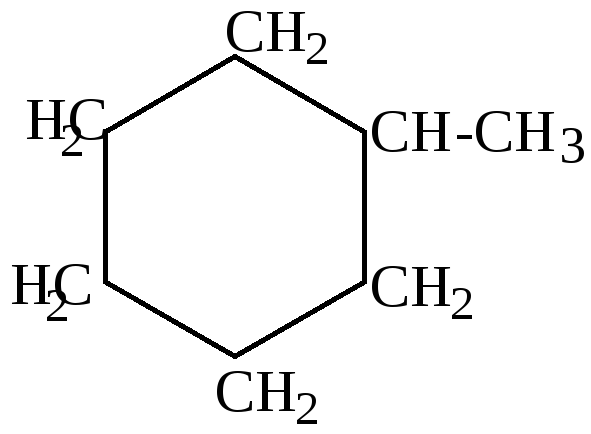
- •Соединения ряда циклогексана
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Химические свойства соединений с трехчленными циклами
- •1.Реакции присоединения
- •2.Реакции окисления
- •3.Реакции конденсации с ароматическими углеводородами
- •Химические свойства циклобутана и его гомологов
- •2.Окисление
- •3.Реакции термического разложения
- •4.Реакции присоединения
- •Взаимные превращения циклов
2.Реакции окисления
|
|
+[O]
HNO3 -H2O KMnO4 конц. |
|
При нагревании с концентрированным KMnO4 или другими сильными окислителями (HNO3, кислород в присутствии катализаторов) происходит разрыв кольца и окисление до двухосновных кислот.
3.Реакции конденсации с ароматическими углеводородами
|
|
+ |
|
AlCl3безв.
|
|
|
|
|
|
|
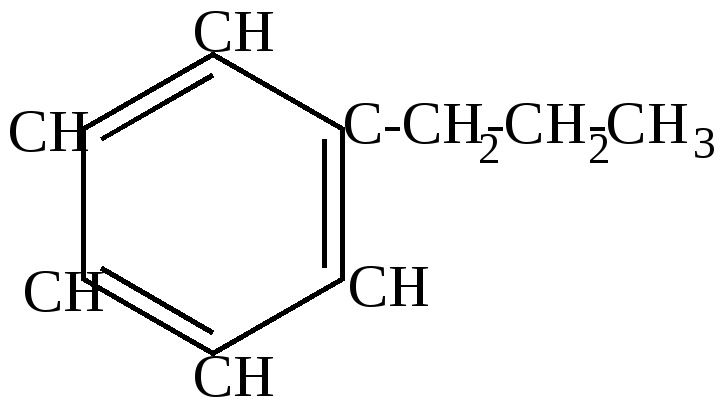
пропилбензол |
Алкилирование ароматических углеводородов циклопропаном позволяет ввести боковую цепь нормального строения (к реакции полимеризации трехчленные циклы не способны).
4.Изомеризация с образованием олефинов происходит при пропускании углеводорода через раскаленные трубки. В присутствии катализаторов температура реакции снижается до 50-1000С.
|
|
Al2O3, 1000C
Fe, Pt, 50-700С |
|
(1) |
|
|
|
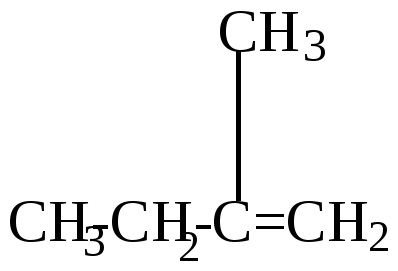
СH3-CH2-CH2-CH=CH2 (2) |
|
CH3-CH2-CH=CH-CH3 (3) |
Химические свойства циклобутана и его гомологов
Соединения с четырехчленными циклами отличаются от соединений ряда циклопропана меньшей склонностью к раскрытию цикла и большей активностью в реакциях замещения. Реакции присоединения Br2,HBr,HJ,H2, а также реакции окисления протекают при температурах более высоких, чем у циклопропана. Так, реакция гидрирования требует нагревания до 2000С (вместо 800С у циклопропана).
|
|
2000C 2 |
CH3-CH2-CH2-CH2-CH3 |
|
|
При этом разрыв кольца идет с одинаковой скоростью по любой связи цикла.
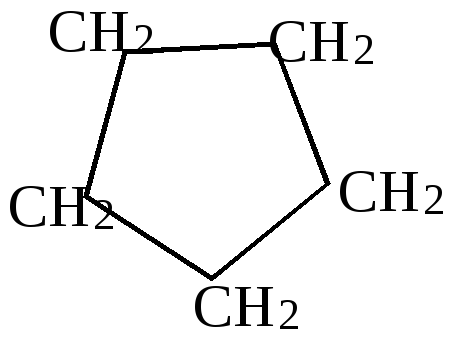
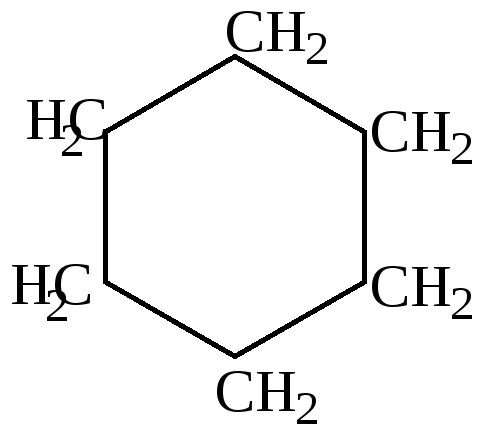
Химические свойства циклопарафинов с пяти- и шестичленными циклами
Химические поведение циклопентановых и цилогексановых сходно с поведением предельных углеводородов.
1.Наиболее типичными для них реакциями являются реакции замещенияводорода, протекающие преимущественно по свободно-радикальному механизму.
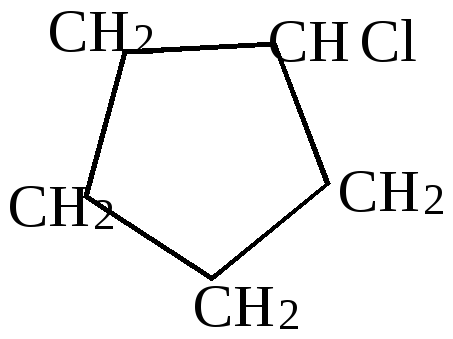
а) галоидирование;
|
|
рассеянный свет +Cl2
- HCl |
|
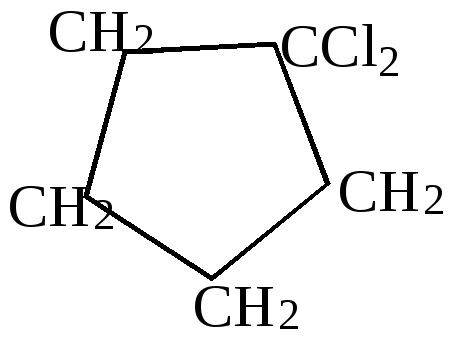
+ Cl2
- HCl |
|
+ Cl2
- HCl |
б) нитрование.
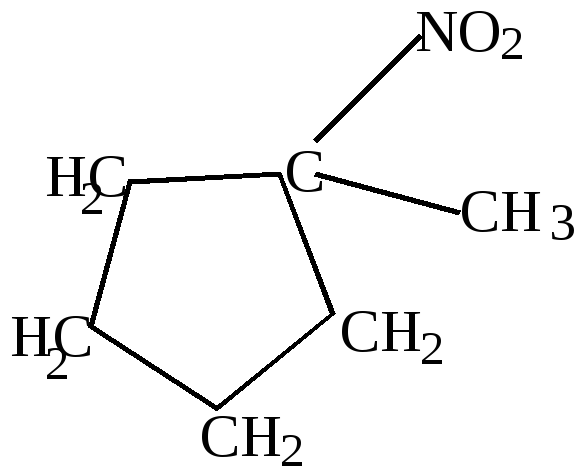
Проводится в условиях реакции Коновалова под действием разбавленной азотной кислоты при повышенной температуре. Нитруются легче, чем парафины и дают лучшие выходы нитросоединения. Особенно легко реагируют углеводороды с третичным атомом углерода в цикле.
|
|
t +
HO-NO2
разб. |
|
|
|
|
1-нитро-1-метициклопентан |
2.Окисление
Пяти- и шестичленные циклы к окислению устойчивы и могут окисляться лишь сильными окислителями при нагревании. В качестве окислителя чаще всего используются концентрированная азотная кислота.
2 HNO3
![]() 2 NO2
+ H2O
+ O
2 NO2
+ H2O
+ O
|
|
+О |
|
+О
-Н2О |
|
+3О
|
|
|
|
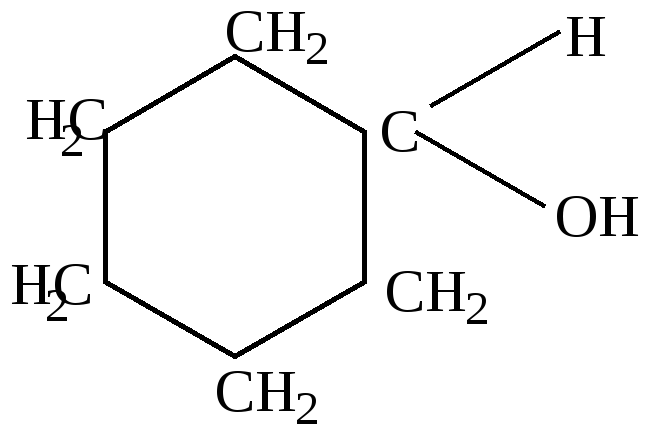
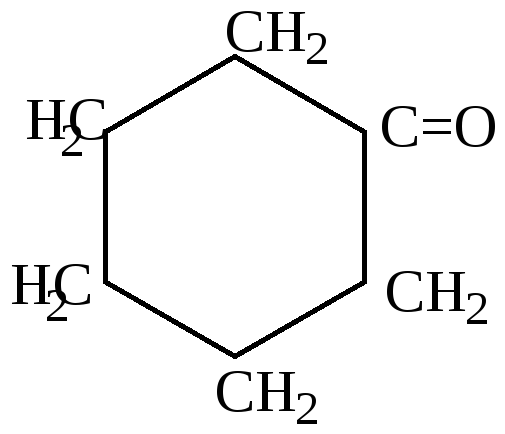
циклогексанол |
|
циклогексанон |
|
|
+3О
|
|
|
|
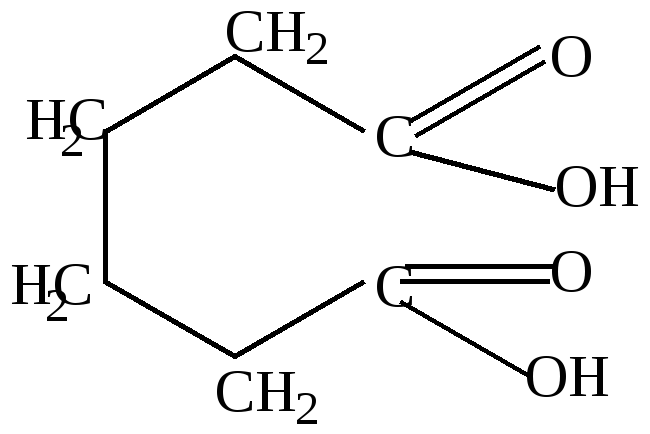
адипиновая кислота |
В зависимости от условий окисления, можно получить любой из этих продуктов.
3.Реакции термического разложения
Под действием высоких температур без доступа воздуха проходят процессы крекинга или дегидрогенизации.
|
|
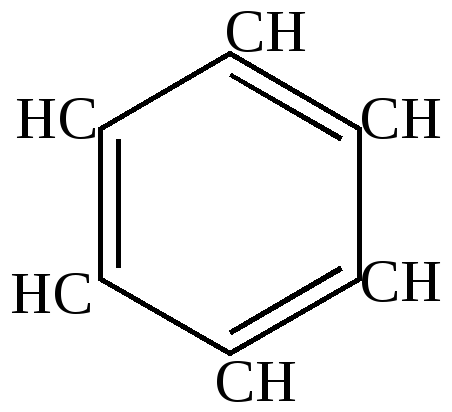
>6000С
Pt3000C |
|
|
|
|
бензол |
|
|
4500С
|
|
|
|
|
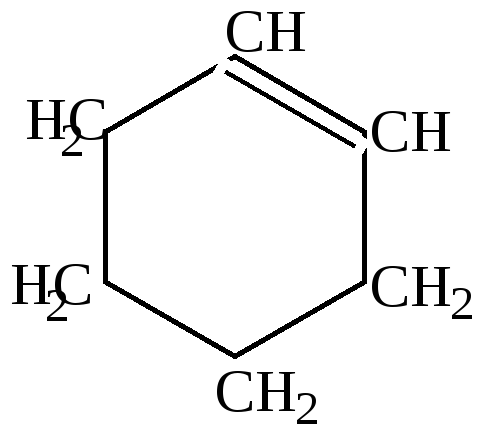
циклогексен |
|
|
>6000С
|
|
|
|
|
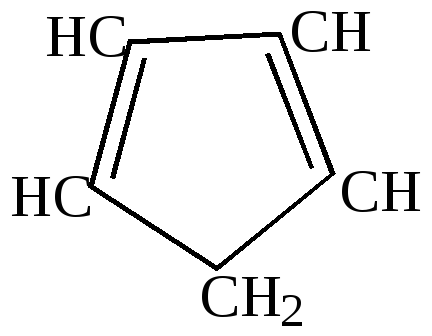
циклопентадиен |

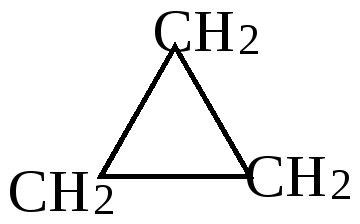
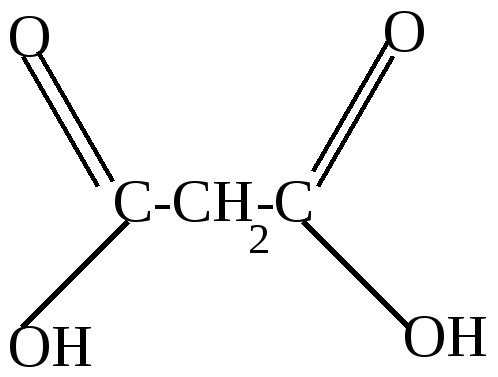
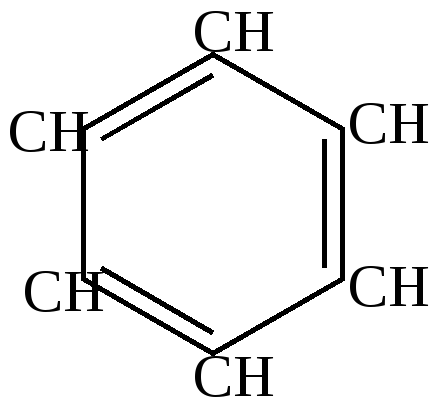
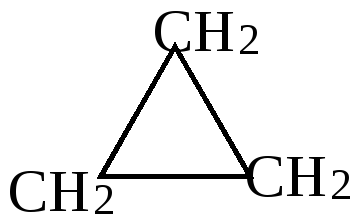
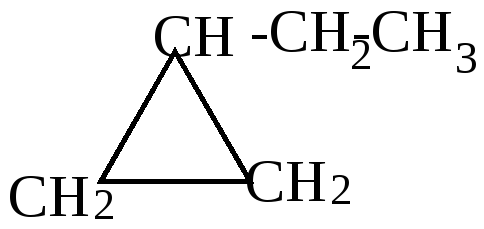
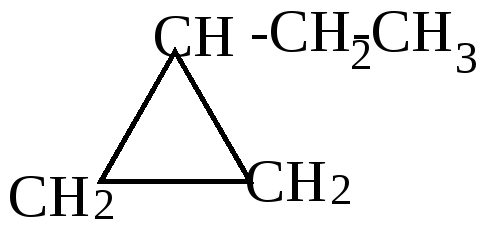




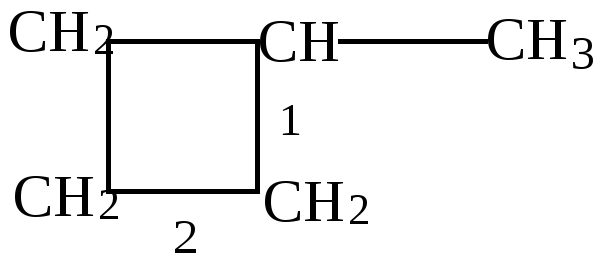

 Ni
1
Ni
1
 +H2
+H2