- •Циклические ненасыщенные углеводороды
- •Ароматические соединения
- •Основные признаки ароматичности
- •4.6.1.Ароматические соединения
- •1 Группа – ароматические соединения бензоидного строения (ароматические углеводороды)
- •Отличительные особенности химического поведения ароматических углеводородов
- •Гомологический ряд, изомерия и номенклатура ароматических углеводородов
- •Названия ароматических радикалов
|
|
AlBr3,T
комнатная температура |
|
|
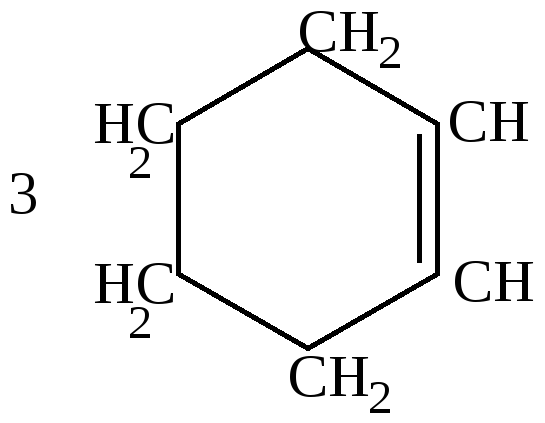
75% |
|
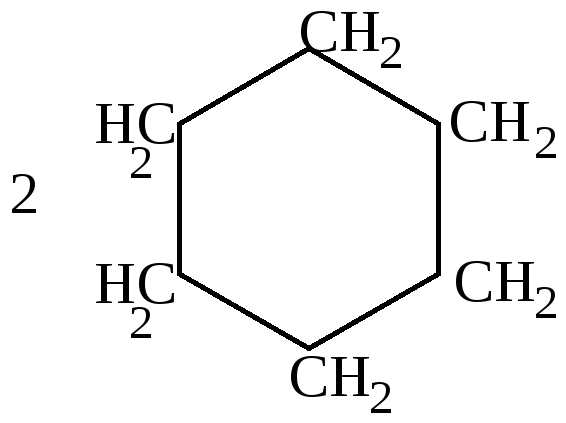
25% |
|
|
AlCl3
|
|
|
|
|
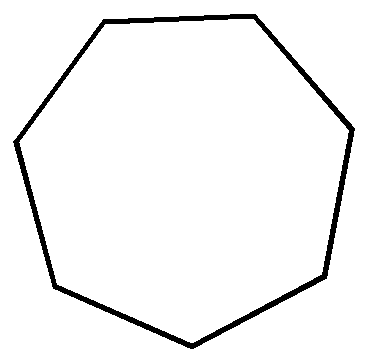
циклогептан |
|
97% |
|
3% |
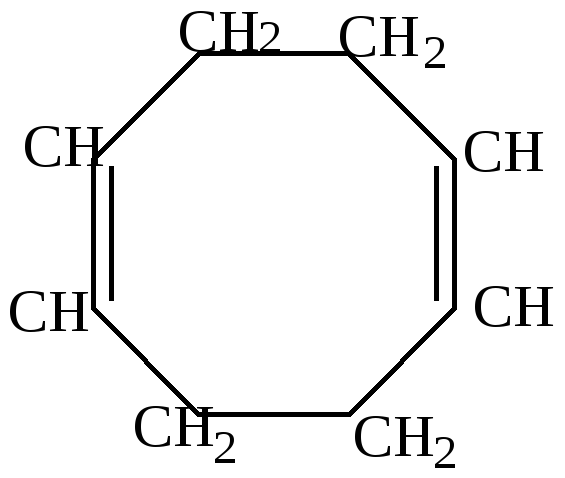
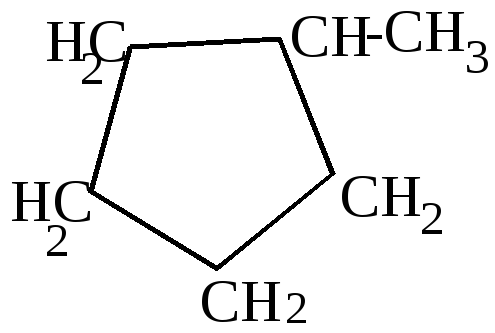
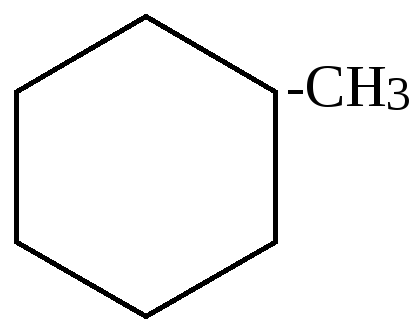
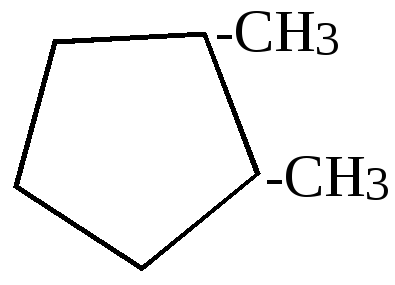
Как видно из приведенных цифровых данных, изомеризация при обычной температуре приводит к преимущественному образованию наиболее стойких шестичленных циклов.
2.Изомеризация при химических реакциях.
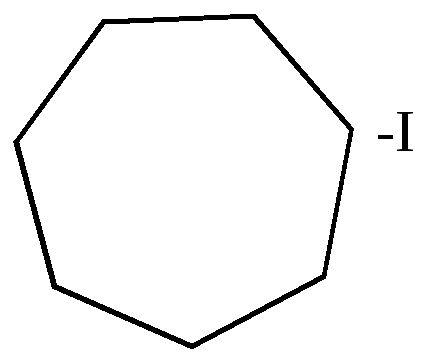
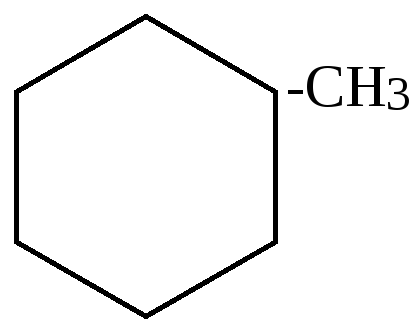
а) превращения йодпроизводных, работы Марковникова и Зелинского
|
|
+HI
|
|
|
иодциклогептан |
|
|
наблюдается сужение цикла
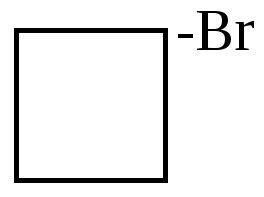
б) превращение спиртов, работы Демьянова и Кижнера
|
|
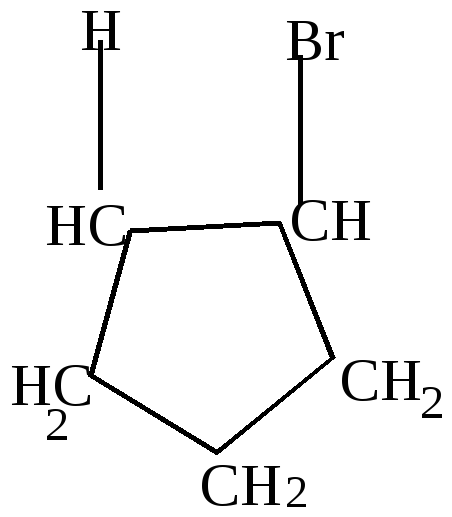
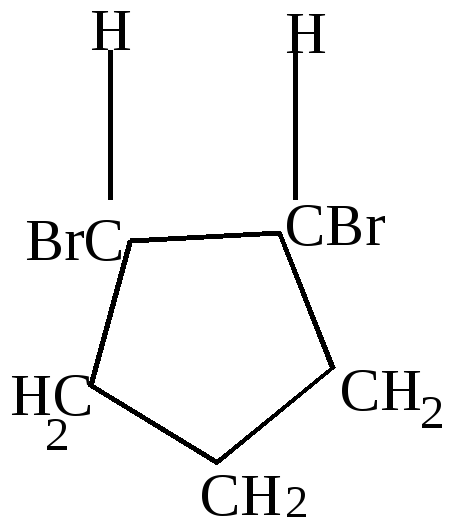
+HBr
|
|
|
циклопропилкарбинол |
|
бромциклобутан |
В большинстве таких превращений образуются соединения с менее напряженными циклами.
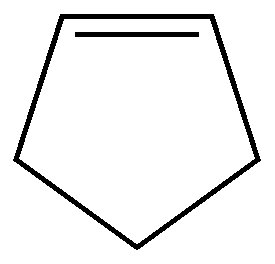
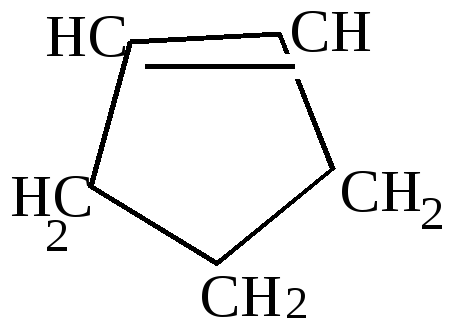
Циклические ненасыщенные углеводороды
|
Циклоалкены | |||||
|
|
|
|
| ||
|
циклопропен |
циклобутен |
циклопентен |
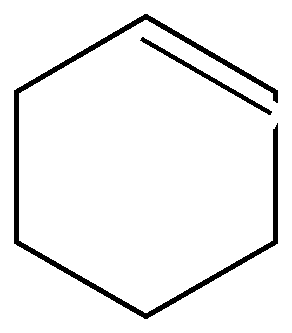
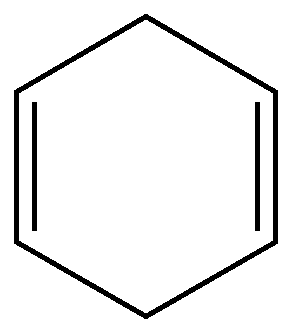
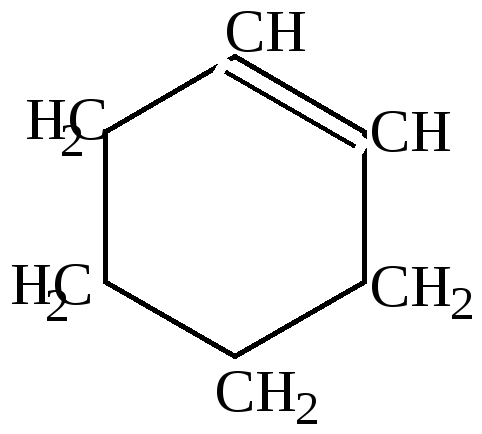
Циклогексен | ||
|
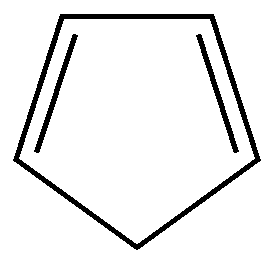
Циклоалкадиены | |||||
|
|
|
| |||
|
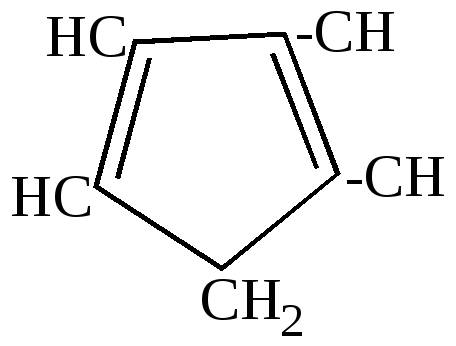
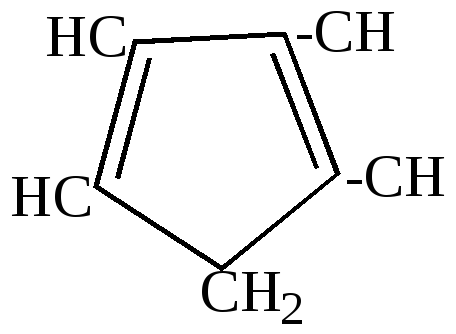
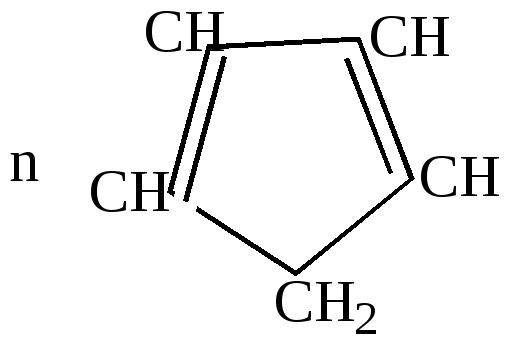
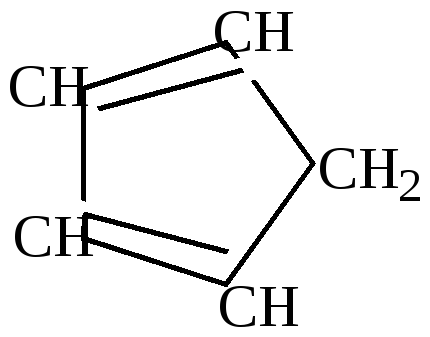
циклопентадиен |
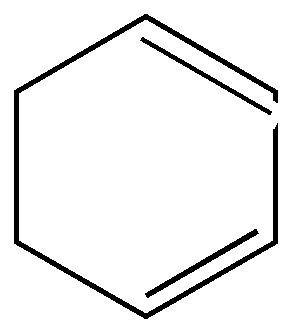
1,3-циклогексадиен |
1,4-циклогексадиен | |||
|
Циклоалкаполиены | |||||
|
|
| ||||
|
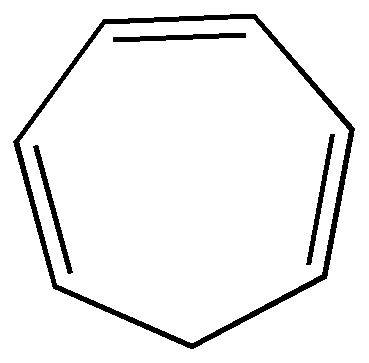
циклогептатриен |
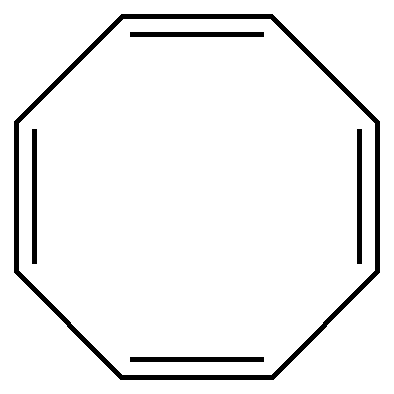
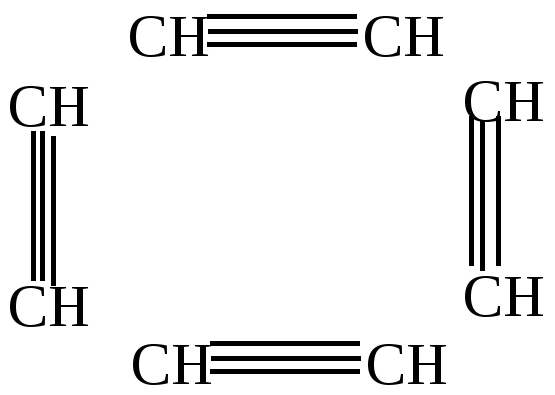
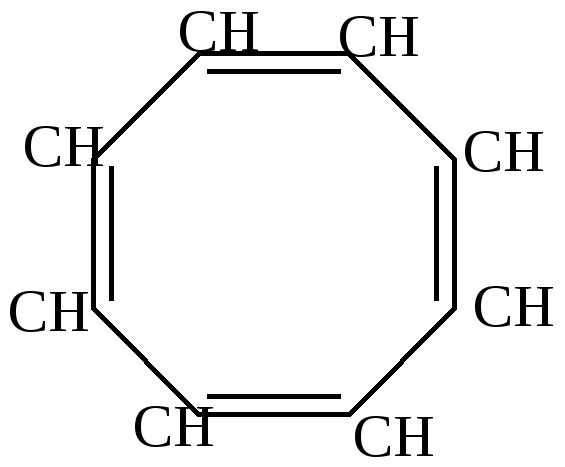
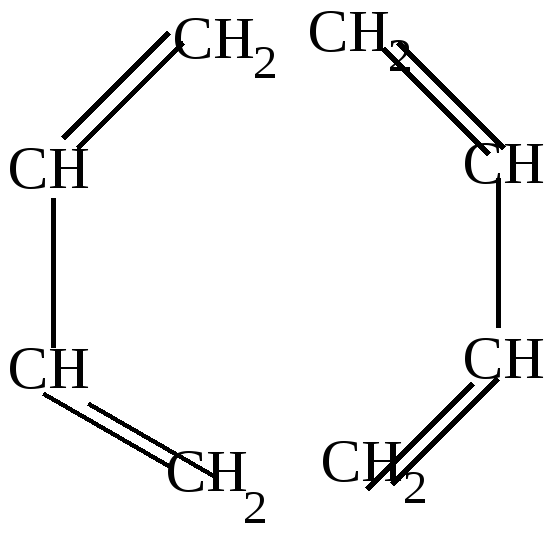
циклооктатетраен | ||||
Способы получения
1.Отщепление галогеноводорода от галогенопроизводных циклоалканов
|
|
+KOH
-KBr -HOH |
|
+Br2
|
|
+2KOH
-2KBr -2HOH |
|
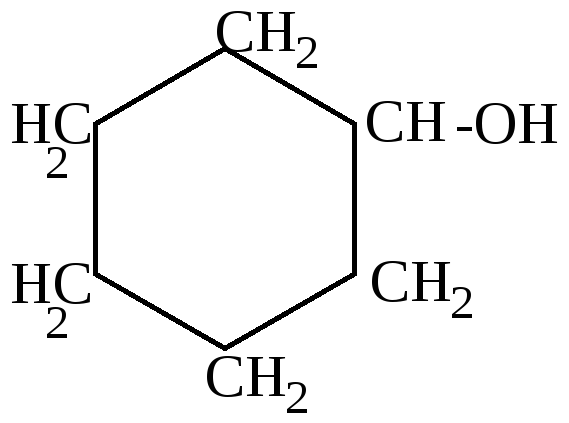
2.Дегидратация циклоалканолов
|
|
(H3PO4), t
-H2O |
|
3.Крекинг и пиролиз циклопарафинов (см. свойства последних)
4.Диеновый синтез – применяется для получения соединений ряда циклогексена
5.Реакция полимеризации непредельных углеводородов
|
|
t, p
[Ni(NH3)4](CN)2 |
|
|
|
Al(C2H5)3. TiCl3
|
|
Химические свойства
Проявляют типичные свойства непредельных углеводородов. Могут присоединять за счет разрыва двойных связей галогены, галогеноводороды, водород, серную кислоту и т.д. Быстро окисляются по двойной связи, что приводит к разрыву кольца, могут полимеризоваться. Наличие двойных связей в циклах обнаруживается с помощью качественных реакций (обесцвечивание бромной воды и разбавленного раствора KMnO4).
Отличительные реакции
1.Реакция необратимого катализа Зелинского
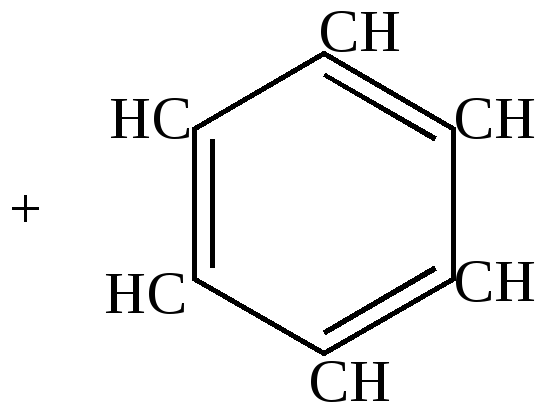
Характерна для ненасыщенных циклических соединений с шестичленным кольцом. При нагревании последних в присутствии платины происходит перераспределение водорода, при этом часть молекул превращается в бензол, часть – в циклогексан.
|
|
Pt
800C |
|
|
Эта реакция разработана Зелинским и названа им реакцией необратимого катализа, так как она никогда не идет в обратном направлении.
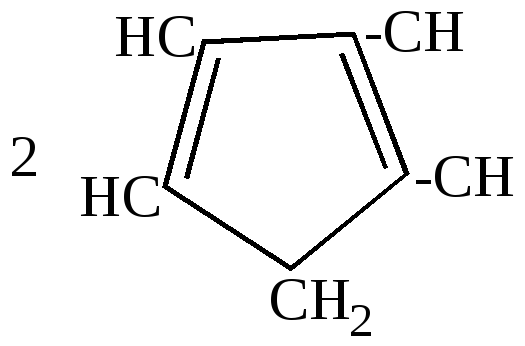
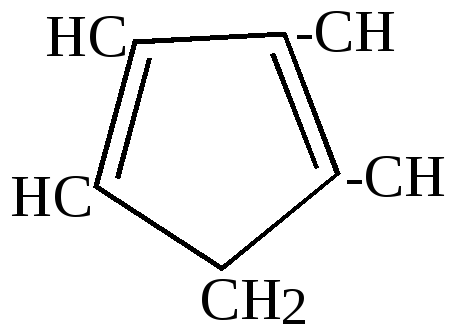
2.Отличительные особенности химических свойств циклопентадиена.
а) большая подвижность атома водорода в метиленовой группе, благодаря чему он может вступать в реакцию замещения водорода металлом:
|
|
+2Na
|
|
циклопентадиенил-натрий
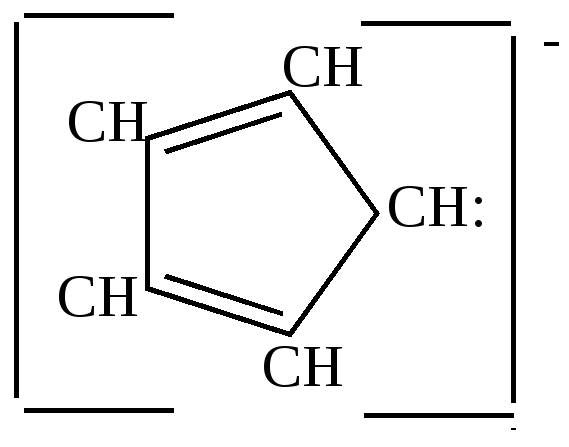
Связь углерода с металлом в этом соединении близка ионной.
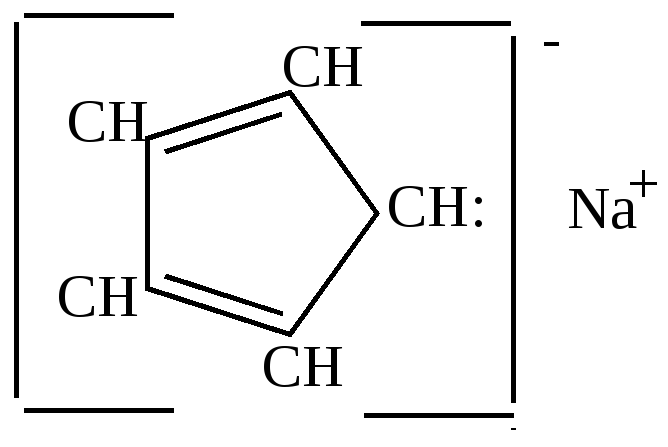
Остающаяся у углерода неподеленная
пара электронов вступает в сопряжение
с
![]() электронами
ядра, образуя единое сопряженное облако
из шести электронов. В результате
отрицательный заряд равномерно
распределяется по всему кольцу, что
приводит к повышению устойчивости
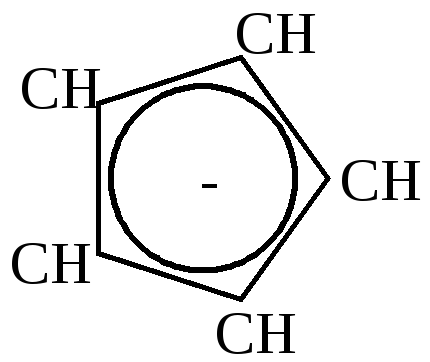
карбаниона. Равномерность распределения
электронной плотности подтверждается
полным выравниванием длин связей.
электронами
ядра, образуя единое сопряженное облако
из шести электронов. В результате
отрицательный заряд равномерно
распределяется по всему кольцу, что
приводит к повышению устойчивости
карбаниона. Равномерность распределения
электронной плотности подтверждается
полным выравниванием длин связей.
|
|
|
|
Такие металлорганические соединения циклопентадиен образует со многими металлами: Fe, Ni, Zn и др. Соединения с многовалентными металлами имеют строение бутерброда, в котором ион металла расположен между плоскими кольцами циклопентадиенил-анионов. Подобные соединения получили название ферроценов или сэндвич-соединений.
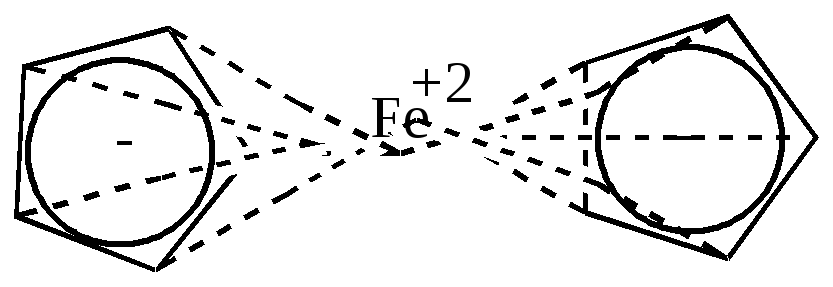
Металл в этих соединениях образует со всеми атомами углерода равноценные частично-ионные связи.
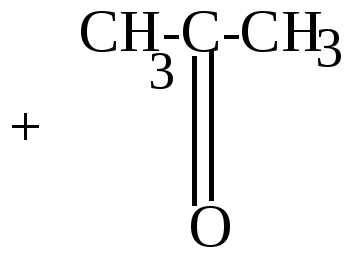
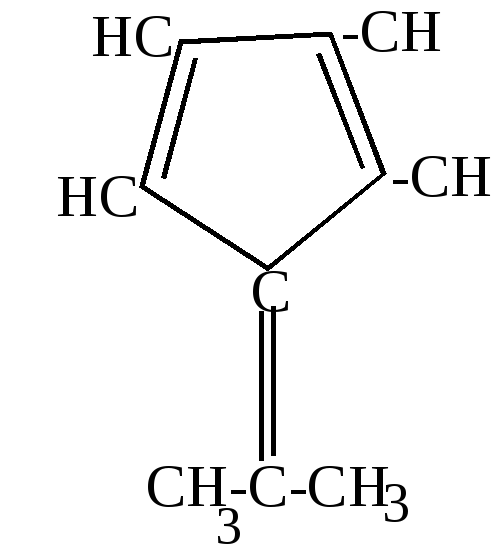
б) конденсация с альдегидами и кетонами.
Циклопентадиен вступает с альдегидами и кетонами в реакцию конденсации по типу кротоновой, играя роль метиленовой компоненты.
|
|
|
|
|
|
|
|
|
Диметилфульвен (оранж.) |
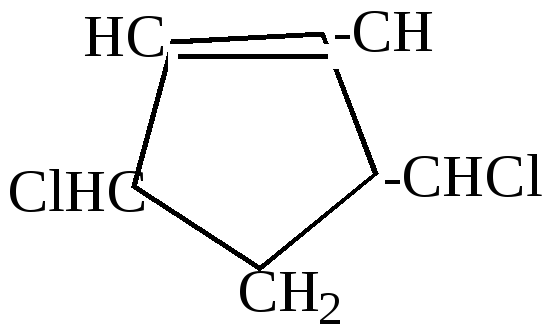
1.Реакции присоединения по концам цепи сопряжения.
|
|
+ Cl2
|
|
2.Реакции полимеризации
|
|
|
|
полициклопентадиенангидрид
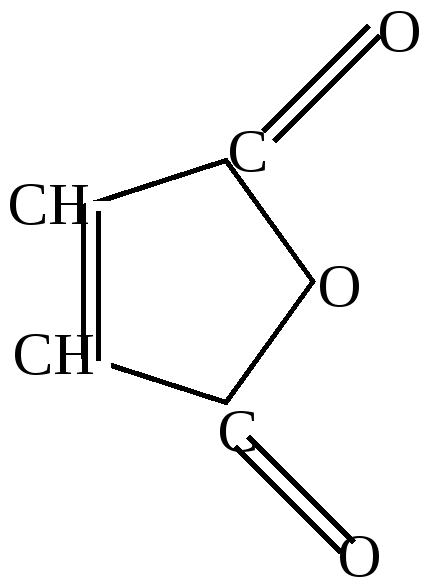
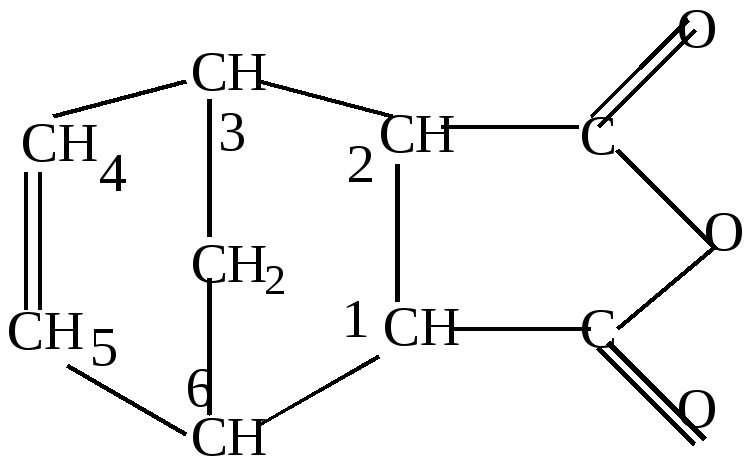
3.Реакции диенового синтеза.
|
|
+ |
|
|
|
|
|
|
|
|
3,6-экзометилен-1,2,3,6-тетрагидрофталевой кислоты |
Аналогичными с пентадиеном свойствами обладает бициклический углеводород – инден, который также находит применение в получении ферроценов, в получении полимерных соединений (инден – кумаровые смолы), применяемых в качестве мягчителей резиновых смесей.
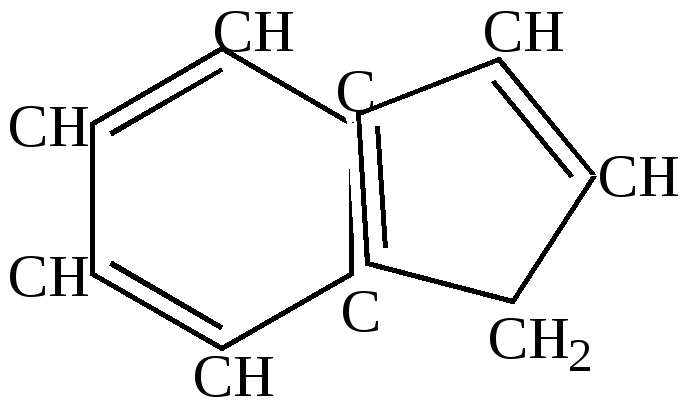

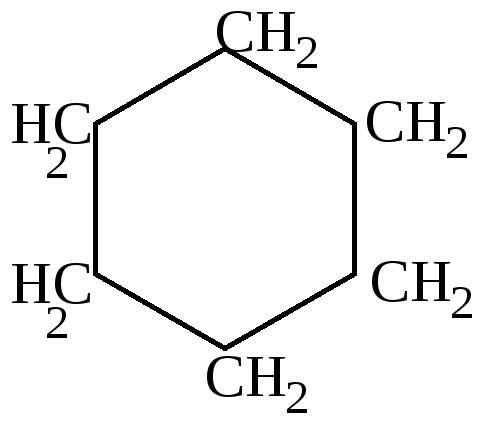
 +H2O
+H2O