
Салициловая кислота
.docСодержание.
-
Общие сведения 3
-
Получение 4
-
Качественный анализ 5
-
Аналитические реакции салицилат-иона 5
-
-
Количественный анализ 6
-
Кислотно-основное титрование в водных растворах 6
-
-
Инструментальный анализ 7
5.1. Фотоколориметрия 7
-
Применение 9
-
Список использованной литературы 10
2
-
 Общие сведения.
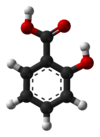
Общие сведения.
Салициловая кислота (2-гидроксибензойная кислота), С6Н4(ОН)СООН; бесцветные кристаллы, хорошо растворима в этаноле, диэтиловом эфире и других полярных органических растворителях, плохо растворима в воде (1.8 г/л при 20 °C).
Выделена из ивовой коры итальянским химиком Рафаэлем Пириа и затем синтезирована им же.
В природе встречается в растениях в виде производных — главным образом в виде гликозида метилового эфира (в частности, салициловая кислота была впервые выделена из коры ивы Salix L., откуда и происходит название), свободная салициловая кислота наряду с салициловым альдегидом в небольших количествах содержится в эфирном масле, выделяемых из цветов некоторых видов спиреи (Spiraea ulmaria, Spiraea Digitata).
Систематическое название: 2-гидроксибензойная кислота
Традиционные названия: Салициловая кислота
Химическая формула: С7Н6О3
Молярная масса: 138,12 г/моль
Физические свойства:
Плотность: 1,44 г/см3
Термические свойства:
Температура плавления: 159 °C
Температура кипения: 211 °C
Химические свойства:
Растворимость в воде: 0.2 г/100 мл
|
|
-
Получение.
-
Синтез бензойной и салициловой кислот осуществляют, используя общие методы синтеза ароматических кислот. В промышленности бензойную кислоту получают жидкофазным окислением толуола воздухом при 130 — 160 °С и давлении 308 — 790 кПа (катализаторы — бензоаты кобальта и марганца, промотированные соединениями брома). Бензойную кислоту получают окислением толуола кислородом воздуха в присутствии катализатора (соединений Со, Mn, V)
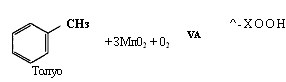
-
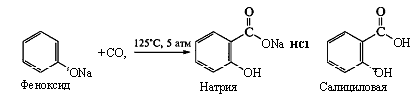
В химической промышленности салициловую кислоту получают карбокси-лированием твердого фенолята натрия (реакция Кольбе —Шмитта):
-
Получение ацетилсалициловой кислоты проводят ацилированием гидроксильной группы салициловой кислоты уксусным ангидридом:
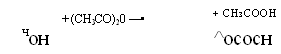
-
Рассмотрим основные этапы контроля качества ароматических кислот и их производных (определение подлинности, испытания на чистоту, количественное определение) в соответствии с их общими химическими свойствами, которые обусловлены присутствием фенольного гидроксида (в молекуле салициловой кислоты), карбоксильной группы (в молекулах бензойной, салициловой, ацетилсалициловой кислот), сложноэфирной группы (в молекулах фенилсалици-лата, ацетилсалициловой кислоты), амидной группы (в молекулах салицила-мида, оксафенамида).
4
-
Качественный анализ.
-
Аналитические реакции на салицилат-ион.
-
-
С хлоридом железа (III), с образованием окрашенного комплексного соединения:
-
С Сульфатом меди (II) с образованием растворимой в воде медной соли зелёного цвета:
5
-
Количественный анализ.
-
Кислотно-основное титрование в водных растворах.
-
Определение массовой доли салициловой кислоты в образце алкалиметрическим методом (вариант прямого титрования).
C6H4(OH)COOH + NaOH = C6H4(OH)COONa + H2O
М (C6H4(OH)COOH) = 138,12 г/моль
Методика: Точную навеску салициловой кислоты помещают в колбу для титрования, растворяют в 5 см3 нейтрализованного по фенолфталеину спирта, прибавляют 1-2 капли раствора фенолфталеина и титруют 0,1 М раствором гидроксида натрия до слабо-розовой окраски раствора.
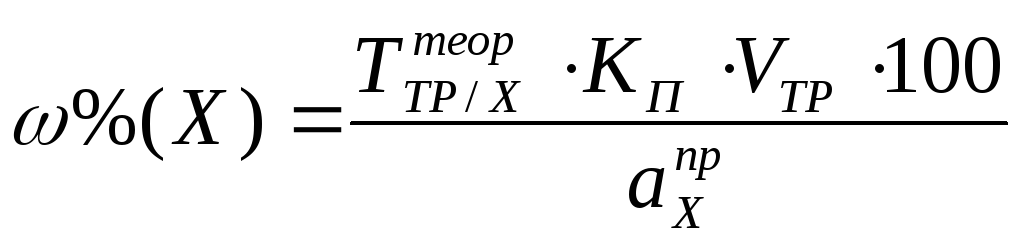
-
Инструментальный анализ.
-
Фотоколориметрия.
-
Фотоколориметрическое определение салициловой кислоты в фармпрепаратах
Фотометрия – это один из методов колориметрического анализа, который в свою очередь входит в группу физико-химических методов анализа. Физико-химические методы анализа основаны на том, что о качестве и количестве исследуемого вещества судят по изменению каких-либо физических свойств, происходящему в результате химической реакции. При колориметрических определениях о количестве определяемого элемента (или иона) судят по интенсивности окраски раствора, вызванной присутствием в нем какого-либо окрашенного соединения этого элемента, полученного по реакции его с каким-либо реактивом. Чем интенсивнее окраска, тем больше элемента (иона) в растворе и наоборот. Если для измерения окраски, а следовательно и концентрации раствора использовать прибор – фотоэлектроколориметр, то такой метод анализа называется фотометрическим. В основе фотометрических измерений лежит закон Ламберта-Бера. Другими словами, при одинаковой толщине слоя раствора данного вещества и прочих равных условиях оптическая плотность этого раствора будет тем больше, чем больше в нем содержится окрашенного вещества. При использовании фотоэлектроколориметра измерение оптической плотности растворов производится фотоэлементами. Световой поток проходит через кювету (с определенной толщиной слоя раствора), наполненную исследуемым окрашенным раствором. Прошедший через раствор световой поток принимается фотоэлементом, в котором световая энергия превращается в электрическую. Возникающий при этом электрический ток измеряется при помощи чувствительного гальванометра. При определении этим методом концентрации исследуемого вещества измеряют оптическую плотность исследуемого раствора (Дисл.) и эталонного (Дэтал.), концентрация которого известна, при одинаковой толщине слоя. Для получения пучка монохроматического света используются светофильтры – набор цветных стекол, которые характеризуются эффективной длиной волны. Для выбора светофильтра в каждом конкретном случае снимают оптическую характеристику раствора – то есть зависимость его оптической плотности от эффективной волны светофильтра. Для этого измеряют оптическую плотность одного и того же раствора при различных светофильтрах и выбирают, при котором она максимальна. Методика измерения светопропускания или оптической плотности на приборе ФЭК-56. Включить прибор и прогреть его 10-15 минут, установить «электрический нуль». Для этого рукояткой привести стрелку гальванометра к нулю, не раскрывая шторку световых пучков рукояткой. В левом световом пучке на все время измерения устанавливается кювета с растворителем.
Если он не окрашен, можно в левый пучок вставить кювету с исследуемым раствором. Индекс правого барабана устанавливают на отсчет 100 по шкале светопропускания. Вращением левого измерительного барабана ее вновь приводят к нулю и отсчитывают по шкале правого барабана оптическую плотность Д. Для массовых фотометрических измерений предварительно строят калибровочную кривую. Для этого готовят серию эталонных растворов различной концентрации, измеряют их оптическую плотность при выбранном светофильтре и определенной толщине слоя ? и строят график зависимости оптической плотности раствора Д от его концентрации С.
-
Применение.
Салициловая кислота - активный компонент ивовой коры. Ещё в XIX в. её использовали для лечения ревматизма и мочекислого диатеза, а сегодня это вещество синтезируют в больших количествах, так как оно служит основой для производства многих лекарств.
Салициловая кислота обладает слабыми антисептическими, раздражающими и кератолитическими (в больших концентрациях) свойствами и применяется в медицине наружно в мазях, пастах, присыпках и растворах при лечении кожных заболеваний; входит в состав пасты Лассара, присыпки «гальманин», препаратов «мозольная жидкость» и «мозольный пластырь».
Производные салициловой кислоты также применяются в медицине (салицилат натрия), её амид (салициламид) и ацетилсалициловую кислоту (аспирин) используют как жаропонижающие, противоревматические, противовоспалительные и болеутоляющие средства; фенилсалицилат — как антисептик, пара-аминосалициловую кислоту (структурно близкую к пара-аминобензойной кислотой, необходимой туберкулезным микобактериям и поэтому метаболически конкурирующую с ней) — как специфическое противотуберкулёзное средство.
Благодаря антисептическому действию салициловую кислоту употребляют при консервировании пищевых продуктов; её используют также в производстве азокрасителей, душистых веществ (сложных эфиров салициловой кислоты), для колориметрических определения Fe и Cu, для отделения тория от других элементов.
9
-
Список литературы.
-
Гузей Л.С., Кузнецов В.Н. «Новый справочник по химии». М. 1998 г. С-261;
-
Методическое пособие по аналитической химии. «Инструментальные методы анализа», Пермь, 2004;
-
Методическое пособие по аналитической химии. «Качественный химический анализ», Пермь, 2003;
-
Методическое пособие по аналитической химии. «Количественный химический анализ», Пермь, 2004;
-
Оганесян Э.Т. «Руководство по химии поступающим в вузы». Москва. 1992 г. С-447;
-
Тюкавкина Н.А., Бауков Ю.И. «Биоорганическая химия». Москва. 1985 г. С-258;
-
Степаненко Б.Н. «Органическая химия». Москва. 1980г. С-253.
10
