
- •1. Понятие о материалах
- •2. Классификация
- •3. Рождение материала
- •Плазма газ жидкость твердое тело (атом молекула вещество)
- •При нормальных условиях – три агрегатных состояния вещества
- •4. Кристаллическое строение материалов
- •5. Плотнейшие шаровые упаковки
- •Плотная упаковка шаров в одном (а) и двух слоях (б) и образующиеся тетраэдрические (в) и октаэдрические (г) пустоты Кубическая плотнейшая шаровая упаковка
- •Гексагональная плотнейшая шаровая упаковка
- •Аллотропные формы некоторых металлов
- •2010 Г Нобелеевская премия по физике
- •Дефекты кристаллического строения
- •Линейные дефекты. Дислокации
- •3. Схема поверхностного слоя детали.
- •Упругая и пластическая деформация
- •Деформация монокристаллов
- •I стадия легкого скольжения
- •IV стадия - фрагментация
- •Деформация поликристаллов
- •Деформирование двухфазного сплава.
- •Разрушение металлов
5. Плотнейшие шаровые упаковки


а б


в г
Плотная упаковка шаров в одном (а) и двух слоях (б) и образующиеся тетраэдрические (в) и октаэдрические (г) пустоты Кубическая плотнейшая шаровая упаковка
шары третьего слоя уложены в октаэдрические пустоты
шары третьего слоя находятся над пустотами первого
упаковка трехслойная, повторение наступает в четвертом слое.
Гексагональная плотнейшая шаровая упаковка
шары третьего слоя уложены в тетраэдрические пустоты
третий слой точно повторяет первый
упаковка оказывается двухслойной.
ГЦК решетка: a = b = c, = = = 90о. Атомы находятся в вершинах куба и в центре каждой грани. Медь, алюминий, никель, золото.
ОЦК решетка: a = b = c, = = = 90о. Атомы находятся в вершинах куба и в центре куба - на пересечении его главных диагоналей (рис.2.3). Решетку имеют хром, вольфрам, ванадий, молибден.
ГПУ решетка. (a = b c, a = b = 90°, = 120°). Атомы находятся в вершинах (узлах) и в центре каждого шестиугольника; три (или 6) дополнительных атомов расположены в центрах трех боковых граней. Цинк, магний, кадмий.
Тетрагональная решетка (a = b c, = = = 90о) бывает объемно-центрированной и гранецентрированной. Индий и радий.

Полиморфизм
Некоторые металлы, в основном, переходные
химические соединения (оксиды, нитриды, карбиды)
При низких температурах - хрупкие (наличие направленной ковалентной связи)
При повышении температуры эти связи разрушаются, металлы переходят в металлические модификации.
Общая закономерность: с повышением температуры наблюдаются переходы от ковалентных структур к металлическим, но не наоборот.
При росте давления – переход к упакованным решеткам: ОЦКГЦК, ГПУ
Белое олово (тетрагональная решетка, металлическая связь)
изменение типа связи - значительные изменения объема
ниже 13,2 С превращается в серое олово с искаженной кубической решеткой, подобной алмазу, и свойствами полупроводника (ширина запрещенной зоны 0,08 эВ)
Превращение сопровождается увеличением объема на 26 %, олово разрушается, рассыпаясь в серый порошок («оловянная чума»).
Кварц
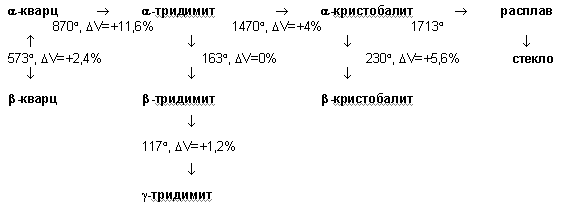

кристалл стекло
Железо
тип химической связи не меняется – не приводит к большим изменениям объема.


Аллотропные формы некоторых металлов
|
Металл |
Аллотропная форма |
Интервал температур, °С |
Кристаллическая решетка |
|
Fe |
δ |
< 911 911 - 1392 1392 - 1539 |
ОЦК ГЦК ОЦК |
|
Ti |
|
< 882 882 - 1671 |
ГПУ ОЦК |
|
Sn |
|
< 18 18 - 232 |
Решетка алмаза Тетрагональная |
|
Co |
|
< 460 460 - 1480 |
ГПУ ГЦК |
|
U |
|
< 668 668 - 720 720 - 1132 |
Орторомбическая Тетрагональная ОЦК |

графен
