
- •3. Кристаллизация.
- •5.Кристаллическая решетка.
- •8. Дефекты кристаллических решеток.
- •10. Понятие о наклепе, текстуре деформации и анизотропии мех. Св-в. Холодная пласт. Деформация.
- •Наклёп – это совокупность структурных изменений и связанных с ними св-в при холодной пластичной деформации.
- •11.Возврат.
- •18.Диаграмма состояния сплавов, компоненты которых имеют полиморфные превращения.
- •19.Связь между типом диаграммы состояния и свойствами сплава.
- •21. Горячая деформация слитка.Влияние горячей пластической деформации на структуру и свойства металла.
- •22. Деформационное упрочнение поликристаллов.
- •23.Компоненты,фазы и структурные составляющие в системе Fe-c (Fe-Fe3c)
- •24 25. Диаграмма состояния железо-цементит (Fe-Fe3c)
- •26. Примеси в стали и влияние их на свойства стали.
- •27. Классификация сталей по содержанию углерода,назначению и качеству.
- •32.Превращения в стали при нагреве. Наследственно мелкозернистые и крупнозернистые стали
10. Понятие о наклепе, текстуре деформации и анизотропии мех. Св-в. Холодная пласт. Деформация.
Упрочнение Ме при деформировании наз-ют наклепом. Наклеп Ме увел-ся до момента разрыва образца, хотя растягивающ. Нагрузка изменяется от Рmax до Рк. Это объясняется появлением местного утонения. В образце участки в которых сосредотачив. пластич. деформация. При значительности деформации в Ме появляется кристаллографическая ориентация зерен, кот наз-ся текстура деформации. Текстура деформации – это результат одновременного деформирования зерен по нескольким системам скольжения. Она зависит от вида деформирования, кристалич стр-ры Ме, наличия примесей и условий деформирования. При прокатке получ-ся более сложная текстура. В этом случае параллельно плоскости прокатки лежит кристаллогафич пл-ть и направление которой образует с напрвлением прокатки опред угол . Текстура деформации делает Ме анизотропным. Анизотропия – различие св-в кристаллов в различн направлениях. Все св-ва, кот зависят от сил в/д атомов спр-ся кристаллограф направл. Анизотропия резче выражена в кристаллах с несиметричной крист решеткой. В этом случае зависит от направления натл-ся для всех св-св. В рез-те ХПД и тех явл происх гуменен .
Наклёп – это совокупность структурных изменений и связанных с ними св-в при холодной пластичной деформации.
В рез-те деф-ции зёрна выстраиваются (вытягиваются в направлении действующей нагрузки. Развивается анизотропия в металле. Под анизотропией понимают различие св-в по различным направлениям в металле. Выше св-ва в направлении пластической деформации (действующей нагрузки).
При холодной пластической деформации прочностные хар-ки (твёрдость, предел прочности и растяжений) увеличиваются в 2-3 раза, тогда как хар-ки пластичности (относит. удлинение, относит. сужение) снижаются 30-40 раз.
Упрочнение металлов при холодной пластической деф-ции обусловлена увелич. дефектов кристаллич. решётки (вакансий, дислакаций), увеличением числа дислокаций одного знака, а также увеличением угла разориентации м/у блоками.
Изменение стр-ры при дорекристаллизационном отжиге.
Пластическая деф-ция приводит к переводу металлов в неравновесное состояние, т.е. с повышенным запасом свободной энергии. Как и любая другая сис-ма металл стремиться к уменьшению свободной энергии. Это уменьшение протекает тем интенсивнее, чем выше тем-ра. В зав-ти от тем-ры отжига различают процессы возврата и процессы рекристаллизации.
11.Возврат.
Возврат явл-ся самой низкой температурной обработкой позволяющей воздействовать на структурные состояния деформированного металла. Различают две стадии возврата: низкотемпературную (отдых) и высокотемпературную. (полигонизация).
В процессе отдыха происходит перераспределение точечных дефектов. Перемещаются по кристаллу и дислокации, однако эти перемещения носят локальный хар-р. Дислокации различного знака встречаясь друг с другом взаимно аннигилируют, т.е. взаимоуничтожаются. Рез-ом этого являются некоторые снижения плотности дислокации. В процессе полигонизации происходит перемещение дислокации по кристаллу. Дислокации перемещ-ся хаотич. по объёму кристалла. Под воздействием тем-ры дислокации перемещаясь концентрир-ся в определённых участках стр-ры с образованием стенок и т.наз. полигонов.
После полигонизации происходит некоторый возврат св-в к св-вам металла до деф-ции.
Рекристаллизация.
После достижения опред. тем-р происходит изменение уже на микроскопическом уровне. Под микроскопом на фоне вытянутых зёрен можно наблюдать мелкие зёрна равноосной формы. По мере увеличения длительности отжига или повышении тем-ры происходит рост мелких зёрен за счёт вытянутых деформируемых зёрен. Образование и рост новых зёрен за счёт деформированных зёрен той же фазы наз-ся первичной рекристаллизацией или рекристаллизацией обработки.
При дальнейшем увелич. тем-ры и длительности отжига происходит «поедание» одними зёрнами других зёрен. Следствием явл-ся разнозёренность стр-р. В пределе можно достичь того, что стр-ра металла будет состоять только зи очень крупных зёрен. Это так наз. собирательная рекристаллизация. Тем-ра начала рекристаллиз. не явл-ся постоянной физ. величиной как, например, тем-ра плавления металла. Тем-ра начала рекристаллиз. будет зависеть от степени предварительной деф-ции металла, длительности процесса и ряда др. факторов.
Тем-ра рекристаллиз. для чистых металлов м.б. рассчитана исходя из соотношения предложенного Бочваром А.А.: Tp=aTпл , а=0,2…0,6.
Отжиг, обеспечивающий получение рекристаллиз. стр-ры после холодной пластической деформации наз-ся рекристаллизационным отжигом. Рекрист. отжиг проводиться как межоперационная обработка после операций холодной пластической деформации.
От размера зерна вообще и после рекристаллиз отжига в частности зависят св-ва металла. Чем мельче зерно, тем выше механические св-ва. Чем крупнее зерно, тем ниже мех-кие св-ва, но выше магн. или электр. св-ва. Поэтому, например, трансформаторную сталь после холодной деф-ции подвергают рекрист. отжигу с тем, чтобы как можно больший размер зерна можно было получить.
Холодная и горячая деформация. Холодная деф. проводиться при тем-рах ниже тем-ры рекристаллиз. и сопровождается наклёпом (наготовка).
Гор. деф. провод-ся при тем-рах выше тем-ры рекристаллиз. При горячей деф. наклёп не происходит поскольку этот наклёп сразу устраняется рекристаллизацией.
12. Сплавы - это вещества, состоящие из нескольких элементов, взятых в произвольных соотношениях. Сплавы получаются главным образом путем сплавления различных элементов в жидком состоянии, но могут быть получены и за счет диффузии в твердом состоянии, и путем совместной конденсации паров или другими способами. Компонентами сплава называют химические элементы или химические соединения, входящие в состав сплава. В зависимости от химической природы элементов, размера их ионов и типа кристаллической решетки компоненты могут растворяться друг в друге (ограниченно или неограниченно), могут быть нерастворимыми друг в друге или образовывать новые химические соединения. Отдельные однородные части сплавов, отделенные от других частей поверхностью раздела, при переходе через которую химический состав и свойства меняются скачком, называются фазами. Графическое изображение фазовых равновесий в зависимости от температуры и состава принято называть диаграммой состояния.
Как правило, в жидком состоянии компоненты сплавов хорошо растворяются друг в друге. При понижении температуры и кристаллизации из жидкой фазы выделяются твердые фазы, которые могут быть твердыми растворами либо чистыми компонентами. Твердые растворы бывают трех видов: замещения, внедрения и вычитания. Твердыми растворами замещения называют фазы, в которых часть узлов кристаллической решетки заполнены атомами одного сорта, а часть узлов атомами другого сорта. Твердые растворы замещения могут быть ограниченными и неограниченными (непрерывными). Твердыми растворами внедрения называют фазы, в которых атомы растворенного компонента внедрены между атомами второго компонента растворителя. Твердые растворы внедрения всегда ограниченны. Твердыми растворами вычитания называют фазы на основе химических соединений. В кристаллических решетках таких сплавов часть узлов не занята атомами того или иного сорта, то есть часть атомов как бы вычтена из кристаллической решетки, и в вместо них в решетке остаются вакансии.
Фазовые превращения:
Наиболее важными из фазовых превращений являются:
кристаллизация - переход жидкой фазы в твердую;
конденсация - переход газообразной фазы в твердую;
превращения структуры в твердом состоянии (изменение типа решетки - полиморфные превращения, изменение растворимости фаз при изменении температуры, мартенситное превращение, упорядочение твердых растворов и так далее);
изменение плотности дислокаций и размера зерен при нагреве деформированных материалов.
Любое фазовое превращение можно рассматривать как результат развития двух процессов: образования зародышей новых фаз и рост этих зародышей. Любое фазовое превращение можно рассматривать как результат развития двух процессов: образования зародышей новых фаз и рост этих зародышей. Термодинамической движущей силой любого фазового превращения является стремление системы к уменьшению свободной энергии F или изобарно-изотермического потенциала G.
15. Построение диаграмм состояния сплавов ,Критические точки, Изотермы свободной энергии.
Д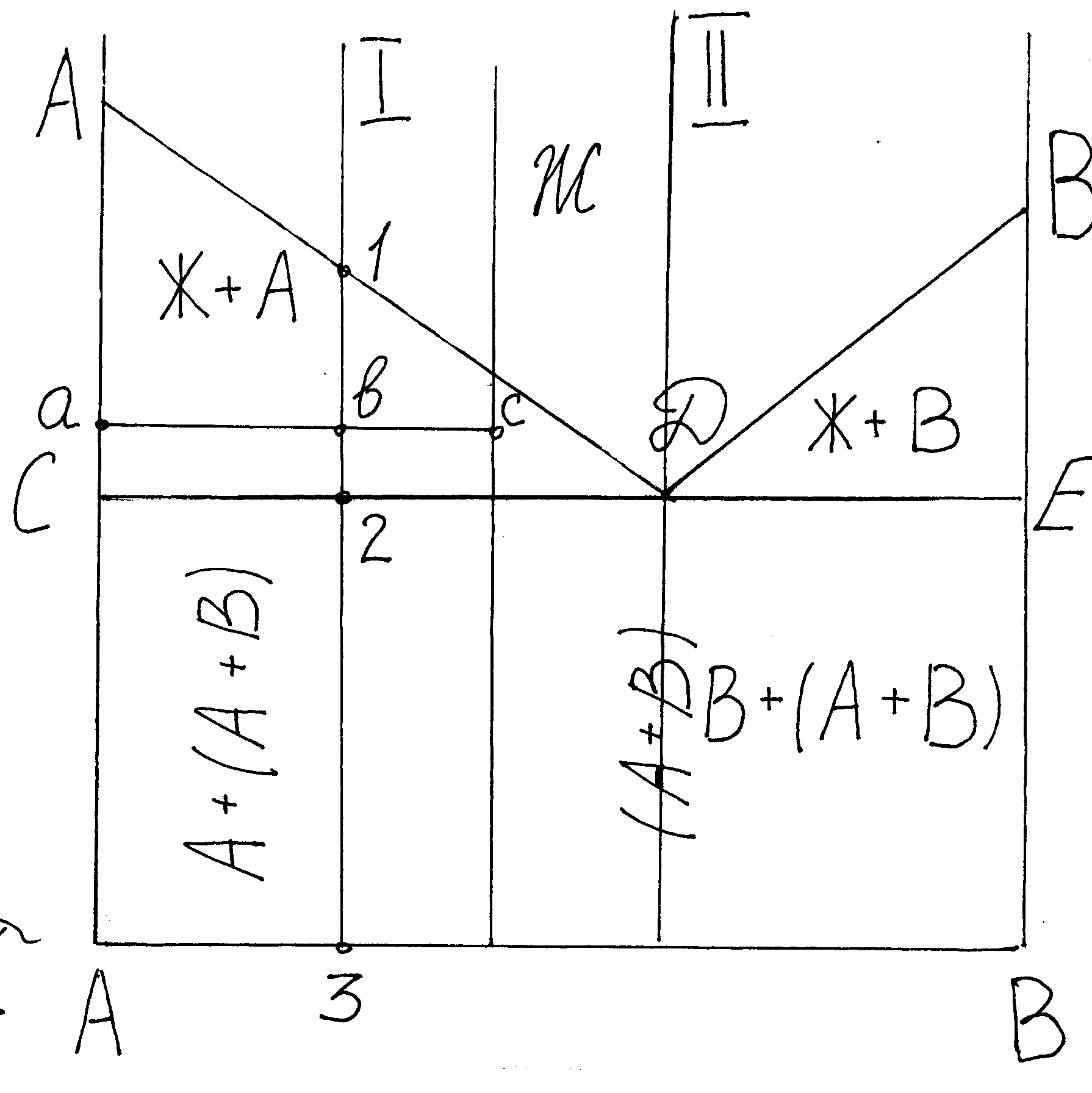
 иаграммы
состояния строятся в координатахt-оси
ординат и концентрация компонентов –
ось абсцисс. Линия АДВ – линия ликвидус.
а представляет собой геометрическое
место точек соответствующих температурам,
при которых из жидкости начинают выпадать
кристаллы, следовательно выше линии
ликвидус сплав находится в жидком
состоянии. Линия СДЕ называется солидус.
Она представляет собой геометрическое
место точек, соответствующих температурам,
при которых жидкая фаза исчезает,
следовательно ниже линии солидус сплав
находится в твердом состоянии. Между
линиями ликвидус и солидус сплав
находится в жидко- твердом состоянии,
и чем ниже температура относительно
линии ликвидус, тем больше кристаллов
и меньше жидкой фазы в сплаве. В точке
Д из жидкости одновременно начинают
выпадать кристаллы компонентов (фаз).
Для диаграмм этого типа компонент и
фаза являются синонимами. Для диаграмм
другого типа необходимо говорить только
о фазах, поскольку компонент и фаза не
являются синонимами. Механическая
смесь, состоящая из двух или более фаз,
одновременно кристаллизующаяся в
жидкости называется эвтектикой. Ниже
точки Д на диаграмме структура представляет
собой чисто эвтектической.
иаграммы
состояния строятся в координатахt-оси
ординат и концентрация компонентов –
ось абсцисс. Линия АДВ – линия ликвидус.
а представляет собой геометрическое
место точек соответствующих температурам,
при которых из жидкости начинают выпадать
кристаллы, следовательно выше линии
ликвидус сплав находится в жидком
состоянии. Линия СДЕ называется солидус.
Она представляет собой геометрическое
место точек, соответствующих температурам,
при которых жидкая фаза исчезает,
следовательно ниже линии солидус сплав
находится в твердом состоянии. Между
линиями ликвидус и солидус сплав
находится в жидко- твердом состоянии,
и чем ниже температура относительно
линии ликвидус, тем больше кристаллов
и меньше жидкой фазы в сплаве. В точке
Д из жидкости одновременно начинают
выпадать кристаллы компонентов (фаз).
Для диаграмм этого типа компонент и
фаза являются синонимами. Для диаграмм
другого типа необходимо говорить только
о фазах, поскольку компонент и фаза не
являются синонимами. Механическая
смесь, состоящая из двух или более фаз,
одновременно кристаллизующаяся в
жидкости называется эвтектикой. Ниже
точки Д на диаграмме структура представляет
собой чисто эвтектической.
Правило отрезков.
Посредством правила
отрезков можно определить состав фаз
в любой двухфазной области и количественное
их соотношение. Правило отрезков состоит
из двух частей. Первая часть: для того
чтобы определить состав фаз через
заданную точку в двухфазной области
(точка соответствует конкретной
температуре) проводят горизонтальную
линию до пересечения с линиями,
ограничивающими эту область. Проекция
точек пересечения на ось концентрации
даст нам состав фаз. Вторая часть: для
того чтобы определить количество фаз
через заданную точку проводят
горизонтальную линию до пересечения с
линией, ограничивающей эту область.
Отрезки между заданной точкой и точками
с соответствующим составом фаз обратно
пропорциональны их количеству.
![]()
![]() Правило
фаз
действует только в двухфазной области.
Правило
фаз
действует только в двухфазной области.
16.Диаграмма состояния сплава с неограниченной растворимостью компонентов в твердом состоянии. Дендритная ликвация.
Диаграммы состояния показывают изменения фазового состояния сплавов при изменении их состава и температуры, а также позволяют предсказывать свойства сплавов. Связь между составом сплава и его свойствами для различных типов диаграмм состояния впервые была установлена Н. С. Курнаковым и получила название закономерностей Курнакова.
При изоморфности кристаллических решеток, близости строения валентных электронных оболочек атомов и малой разнице в размерах атомов в твердом состоянии элементы образуют неограниченные твердые растворы.

Диаграммы состояния и зависимость свойств от состава для случаев:
а), б)неограниченной растворимости компонентов в твердом состоянии;
в), г) отсутствия растворимости компонентов в твердом состоянии;
д), е) ограниченной растворимости компонентов в твердом состоянии.
Верхняя линия на диаграмме состояния представляет собой геометрическое место точек начала кристаллизации или конца плавления линию ликвидус. Выше этой линии все сплавы находятся в однофазномжидком состоянии. Нижняя линия является геометрическим местом точек конца кристаллизации или начала плавлениялиния солидус. Ниже этой линии все сплавы также в однофазномтвердом состоянии.
Когда компоненты полностью не растворяются друг в друге в твердом состоянии и растворимы в жидком состоянии, показана на рис. в). В данном случае линия ликвидус выглядит в виде ломаной, причем при некотором составе, называемом эвтектическим (от греческого слова эвтектикос - легкоплавкий), линия ликвидус касается линии солидус. Линия солидус представляет собой горизонтальную линию. Ниже линии солидус в сплава имеется две твердые фазы, являющиеся чистыми компонентами сплава. Поскольку компоненты не растворимы друг в друге, то свойства линейно меняются при изменении состава в соответствии с тем, как меняется количество фаз. Однако вблизи эвтектического состава наблюдается отклонение от линейного закона. Это связано с тем, что при кристаллизации эвтектических сплавов из жидкости одновременно выпадают две твердые фазы, и формируется мелкозернистая структура. Измельчение зерен ведет за собой увеличение электрического сопротивления и прочности эвтектических сплавов.
Ликвация – хим неоднородность состава в различных частях слитка.Дендритная ликвация- .хим неоднородность в пределах каждого дендрита.( В центре кристалла больше всего содержится твердых компонентов.Это измененим сотава внутри кристалла и наз дендритн ликв) Устраняется термообраб-кой и диффузионным отжигом (гомоденизация).
--------------------------------------------------------------------------------------------------------------------------------------------------------------------
17. Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии и эвтектикой
Диаграмма состояния для двухкомпонентной системы, компоненты в которой образуют ограниченные твердые растворы, при этом в зависимости от типа диаграммы, диаграммы подразделяются на диаграммы с эвтектикой и диаграммы с перитектикой.
Диаграммы с эвтектикой: компоненты А и В. Фазы: жидкость ,;- твердый раствор компонента В в компоненте А; - твердый раствор компонента А в компоненте В.
Линия АВС – ликвидус. ADCFB – солидус, т.к. компоненты вступают во взаимодействие в твердом состоянии с правой и с левой стороны диаграммы будут находиться так называемые области ограниченной растворимости.
Линия ДК- указывает на то, что растворимость компонента В в А увеличивается с повышением температуры. Растворимость В в А при комп. Температуре будет соответственна на диаграммы. При температуре плавления эвтектики точка Д на диаграмме. Противоположность растворимость компонента А в В не изменяется (линия FL) при комнатной температуре растворимость компонента А в В соответственна точке L при температуре плавления эвтектики в точке L. Горизонтальная линия DCF соответствует температуре, при которой происходит эвтектическая реакция.
Эвтектика – это механическая смесь двух или более фаз одновременно кристаллизующихся из жидкости. В точке С происходит чисто эвтектическая реакция, которая записывается как жидкость точки С распадается на - твердый раствор точки Д и - в точке F.
![]()
Кривые охлаждения.
С=К-Ф+1
С0-1=2-1+1=2 С1-2=2-2+1=1
Диаграмма с перлитом.
Компоненты А,В, жидкост, ,.
В отличие от эвтектической реакции при перитектической реакции жидкость взаимодействует с кристаллами выпавшей фазы с образованием кристаллов новой фазы.
 Диаграммы
состояния и зависимость свойств от
состава для случаев: а), б) неограниченной
растворимости компонентов в твердом
состоянии;
Диаграммы
состояния и зависимость свойств от
состава для случаев: а), б) неограниченной
растворимости компонентов в твердом
состоянии;
в), г) отсутствия растворимости компонентов в твердом состоянии;
д), е)ограниченной растворимости компонентов в твердом состоянии
Для систем сплавов с ограниченной растворимостью характерны диаграммы состояния, показанные на рис. д). В таких системах имеются две области существования фаз, представляющих раствор одного компонента в другом, и область существования смеси двух фаз. При составах, соответствующих областям существования твердых растворов на основе какого-либо компонента, изменения свойств аналогично изменению свойств в системах с неограниченной растворимостью компонентов, а в областях составов, соответствующих двухфазным смесям, изменение состава ведет к изменению свойств, характерному для систем с нерастворимыми в твердом состоянии компонентами
--------------------------------------------------------------------------------------------------------------------------------------
