
- •Справочные материалы по химии Содержание
- •Физико-химические постоянные
- •Периодическая система элементов д.И. Менделеева
- •Групповые названия химических элементов
- •Относительные молекулярные массы неорганических соединений
- •Классификация неорганических веществ
- •Амфотерные соединения
- •Растворимость веществ в воде при температуре 25 °с
- •Взаимодействие металлов с водными растворами щелочей
- •Стандартные потенциалы окислительно-восстановительных электродов в щелочной среде
- •Стандартные электродные потенциалы простых веществ
- •Номенклатура кислот
- •Электропроводность слабых электролитов
- •Степень и константа диссоциации некоторых кислот в их децинормальных растворах (0,1 н.) при 18 °с
- •Cильныеэлектролиты:
- •Относительныеэлектроотрицательности элементов
- •Эбуллиоскопические (Кэ) и криоскопические (Ккр) константы некоторых растворителей
- •Произведения растворимости некоторых малорастворимых электролитов при 25 °с
- •Возможные степени окисления элементов
- •Электронное строение атомов в основном состоянии
- •Стандартные термодинамические функции образования
- •Стандартные окислительно-восстановительные потенциалы е0в водных растворах при 250с по отношению к нормальному водородному электроду
- •Не расписываются на ионы:
- •Постоянную степень окисления имеют:
- •Алгоритм решения окислительно-восстановительных реакций
- •Гидролиз
- •Жесткость воды
- •Электрохимический ряд напряжений металлов
Гидролиз
Гидролизом солей называется взаимодействие ионов соли с водой, приводящее к образованию слабого электролита (кислоты, основания, кислого или основного иона). При этом изменяется рН среды.
Если рассматривать соль как продукт взаимодействия кислоты с основанием, то в зависимости от их силы все соли делятся на четыре типа:
Соли, образованные сильной кислотой и сильным основанием: NaCl, K2SO4.
Соли, образованные сильным основанием и слабой кислотой: Na2CO3, K2S.
Соли, образованные слабым основанием и сильной кислотой: ZnSO4, AlCl3.
Соли, образованные слабым основанием и слабой кислотой: CH3COONH4.
Соли первого типа гидролизу не подвергаются, т.к. при их взаимодействии с водой не могут быть получены слабые электролиты. В системе H2O = H+ + OH– равновесия не нарушается, поэтому в растворах этих солей рН = 7.
Соли, нерастворимые в воде, гидролизу не подвергаются.
Примеры:
Гидролиз Na2S идёт по аниону, т.к. NaOH – сильное основание, а H2S – слабая кислота.
S2- + H2O = HS– + OH– pH>7
Na2S + H2O = NaHS + NaOH
Гидролиз ZnCl2 идёт по катиону, т.к. Zn(OH)2 – слабое основание, а HCl – сильная кислота.
Zn2+ + H2O = ZnOH+ + H+ pH<7
ZnCl2 + H2O = ZnOHCl + HCl
Гидролиз CH3COONH4 идёт и по катиону и по аниону, т.к. CH3COOH – слабая кислота, и NH4OH – слабое основание. pH в растворе этих солей определяется по степени диссоциации слабых электролитов.
CH3COONH4 + H2O = CH3COOН + NH4ОН.
Жесткость воды
Жесткость воды, совокупность свойств воды, обусловленная наличием в ней преимущественно катионов Са2+ (кальциевая жесткость воды) и Mg2+ (магниевая жесткость воды ).
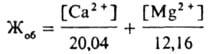
Магниевую жесткость воды определяют из выражения: ЖMg = Жоб - ЖCa.
Электрохимический ряд напряжений металлов
УСИЛЕНИЕ ВОСCТАНОВИТЕЛЬНОЙ СПОСОБНОСТИ (свойства отдавать е)

|
Li |
Cs |
Rb |
K |
Ra |
Ba |
Sr |
Ca |
Na |
La |
Ce |
Nd |
Sm |
Cd |
Y |
Mg |
Lu |
Sc |
Pu |
Th |
Np |
|
-3,04 |
-3,01 |
-2,98 |
-2,92 |
-2,92 |
-2,91 |
-2,89 |
-2,87 |
-2,71 |
-2,52 |
-2,48 |
-2,44 |
-2,41 |
-2,4 |
-2,37 |
-2,36 |
-2,25 |
-2,08 |
-2,07 |
-1,9 |
-1,86 |
|
Li+ |
Cs+ |
Rb+ |
K+ |
Ra2+ |
Ba2+ |
Sr2+ |
Ca2+ |
Na+ |
La3+ |
Ce3+ |
Nd3+ |
Sm3+ |
Cd3+ |
Y3+ |
Mg2+ |
Lu3+ |
Sc3+ |
Pu3+ |
Th3+ |
Np3+ |
|
Be |
Ti |
Hf |
Al |
Zr |
Mn |
Nb |
B |
Zn |
Cr |
V |
Ga |
Fe |
Eu |
Cd |
In |
Tl |
Co |
Ni |
Mo |
Sn |
|
-1,85 |
-1,75 |
-1,7 |
-1,66 |
-1,63 |
-1,18 |
-1,1 |
-0,9 |
-0,76 |
-0,74 |
-0,54 |
-0,53 |
-0,44 |
-0,44 |
-0,40 |
-0,34 |
-0,33 |
-0,28 |
-0,25 |
-0,2 |
-0,14 |
|
Be2+ |
Ti3+ |
Hf4+ |
Al3+ |
Zr4+ |
Mn2+ |
Nb3+ |
B+3 |
Zn2+ |
Cr2+ |
V+4 |
Ga3+ |
Fe2+ |
Eu3+ |
Cd2+ |
In3+ |
Tl+ |
Co2+ |
Ni2+ |
Mo3+ |
Sn2+ |
|
Pb |
D |
H |
Sb |
Bi |
As |
Cu |
Cu |
I |
Pt |
Hg |
Ag |
Rh |
Hg |
Pd |
Br |
Pt |
Cl |
Au |
Au |
F |
|
-0,13 |
-0,003 |
0,00 |
+0,2 |
+0,22 |
+0,3 |
+0,34 |
0,52 |
+0,54 |
+0,77 |
+0,79 |
+0,8 |
+0,8 |
+0,85 |
+0,92 |
+1,07 |
+1,2 |
+1,36 |
+1,5 |
+1,68 |
+2,65 |
|
Pb2+ |
2D+ |
2H+ |
Sb+3 |
Bi+3 |
As3+ |
Cu2+ |
Cu1+ |
2I– |
Pt+4 |
Hg22+ |
Ag+ |
Rh3+ |
Hg2+ |
Pd2+ |
2Br– |
Pt2+ |
2Cl– |
Au3+ |
Au+ |
2F– |

УСИЛЕНИЕ ОКИСЛИТЕЛЬНОЙ СПОСОБНОСТИ (свойства присоединять е)
Справочный материал находится в разработке.
Зенцова Светлана Витальевна
По всем вопросам обращаться: svetozek@mail.ru
Дата обновления: 14.03.2013
