
- •Тема №1 Техническая термодинамика.
- •1.Основные понятия и определения.
- •Уравнение Клайперона 1834г.
- •2. Внутренняя энергия.
- •3.Работа газа.
- •4.Теплота
- •Первый закон термодинамики.
- •5. Теплоемкость.
- •6.Энтальпия
- •7.Энтропия
- •8.Термодинамические процессы
- •Политропный процесс.
- •Водяной пар.
- •Диаграмма pV для водяного пара
- •Ts- диаграмма для водяного пара
- •Второй закон термодинамики
- •IS- диаграмма водяного пара.
- •Расчет тепловых параметров по is- диаграмме.
- •Истечение и дросселирование пара и газа.
- •Истечение газа из сопла.
- •Истечение паров
- •Дросселирования газов и паров.
- •Паротурбинная установка.
- •Цикл паротурбинных установок. Цикл Ренкин.
- •Регенеративный цикл.
- •Теплофикационный цикл.
- •Цикл газотурбинной установки.
- •Тема №2 Основы теплопередачи.
- •Основные понятия и определения.
- •Теория теплопроводности. Закон Фурье.
- •Однослойная плоская стенка.
- •Многослойная плоская стенка.
- •Тема №3 Конвективный теплообмен.
- •Определение коэффициента теплоотдачи.
- •Теплоотдача при вынужденной конвекции.
- •Теплообмен при свободной конвекции.
- •Лучистый теплообмен.
Политропный процесс.
Любой произвольный процесс можно описать в pV- координатах (по крайней мере на небольшом участке.)
pνn = const, подбирая соответствующее значение n.
Процесс, описываемый таким уравнением называется политропным, показатель политропы n может принимать любое значение (+ ;-), но для данного процесса он является величиной постоянной.
Политропные процессы идеального газа.
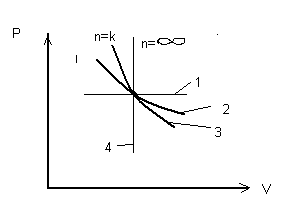
Где: 1. изобара.
2. изотерма.
3. адиабата.
4. изохора.
Теплота процесса:
![]() ;
;
где
![]() - массовая теплоемкость политропного
процесса.
- массовая теплоемкость политропного
процесса.
|
Процесс |
n |
Сn |
|
Изохорный |
+ |
Cv |
|
Изобарный |
0 |
Ср |
|
Изотермический |
1 |
|
|
адиабатный |
к |
0 |
Изохора n= делит поле диаграммы на 2 области: Процессы, находящиеся правее изохор характеризуются положительной работой, т.к. сопровождаются расширением рабочего тела; для процессов, расположенных левее изохоры характерна отрицательная работа. Процессы расположенные правее и выше адиабаты идут с подводом теплоты к рабочему телу; процессы лежащие левее и ниже адиабаты протекают с отводом теплоты.
Для процессов расположенных над изотермой (n=1) характерно увеличение внутренней энергии газа. Процессы, расположенные под изотермой сопровождаются уменьшением внутренней энергией. Процессы, расположенные между адиабатой и изотермой имеют отрицательную теплоемкость.
Водяной пар.
Пар над жидкостью, имеющей туже температуру, что и кипящая вода, но существенно больший объем называется насыщенным.
Сухой насыщенный пар- пар, не содержащий капелек жидкости и получающийся в результате законченного парообразования. Пар, содержащий влагу, называется влажным.
Влажный, насыщенный пар - смесь сухого насыщенного пара с мельчайшими капельками воды, взвешенными в его массе.
Пар, имеющий температуру более высокую, чем температура насыщения при том же давлении называется насыщенным или перегретым паром.
Степень сухости насыщенного пара (паросодержания)- это масса сухого пара в 1 кг. Влажного (Х);
![]() ;
;
где Мсп- масса сухого пара.
Мвп- масса влажного пара.
Для кипящей воды Х=0. Для сухого насыщенного пара Х=1.
Диаграмма pV для водяного пара

Процесс преобразования в pV диаграмме.
В процессе образования из холодной волы при 0С перегретого пара отмечают 3 важнейшие стадии:
1. подогрев холодной воды до температуры кипения.
2. парообразование.
3. перегрев пара.
Этим стадиям соответствуют 4 состояния рабочего тела:
холодная вода при t=0С – точки а1,а2,а3.
кипящая вода при температуре tn (начало парообразования)- точки b1,b2,b3.
сухой насыщенный пар (конец парообразования)- точки с1,с2,с3.
перегретый пар- точки d1,d2,d3.
Точки а1,а2,а3, b1,b2,b3, с1,с2,с3 соответствуют различным давлениям, соединяя между собой одноименные точки, характеризующие холодную воду и сухой насыщенный пар, получим в pV- диаграмме кривые I,II,III.
Процесс получения сухого насыщенного пара при постоянном давлении изображается в общем случае графиком abc, а перегретого пара в общем случае abcd, при этом ab- процесс подогрева воды до температуры кипения, bc- процесс парообразования, протекающий одновременно при постоянном давлении и температуре, т.е. процесс bc является изобарным и одновременно изотермическим. сd- процесс перегрева пара при постоянном давлении, но при возрастающей температуре. Между точками b и с находится влажный пар с различными промежуточными значениями степени сухости. Кривая I изображается линией параллельной оси ординат. Если исходить из предположения, что вода не сжимаема и, следовательно, удельный объем воды практически не зависит о давления. Кривую II называют нижней пограничной кривой или кривой жидкости, а кривую III – верхней пограничной кривой или кривой сухого насыщенного пара. Кривая II отделяет на диаграмме область жидкости от области насыщенных паров, а кривая III- область насыщенных от области перегретых паров.
Точки а1,а2,а3, изображающие состояние 1 кг холодной воды при температуре 0С и разных давлениях располагают практически на одной прямой. Точки b1,b2,b3 с увеличением давления смещаются вправо. Так как при этом соответственно увеличиваются температуры кипения tн, а значит и удельные объемы воды. Точки с1,с2,с3 смещаются влево, так как с увеличением давления удельный объем пара уменьшается, несмотря на возрастание температуры. Из pV диаграммы видно, что с повышением давления точки b1,b2,b3, с1,с2,с3 сближаются, т.е. постепенно уменьшается разность удельных объемов сухого насыщенного пара и кипящей воды (отрезки bс). При некотором объеме, эта разность становится равной 0, т.е. b и с совпадают, а линии II и III сходятся. Точка встречи обеих кривых называется критической точкой и обозначается буквой К. состояние соответствующее точке К называется критическим состоянием.
Параметры водяного пара критического состояния следующие:
tк=374,15С
Рк=225,65 атм.
Vк=0,00326
![]() /кг.
/кг.
В критической точке кипящая вода и пар имеют одинаковый параметр состояния, а изменение агрегатного состояния не сопровождается изменением объема, т.е. в критическом состоянии исчезает условная граница, разделяющая эти 2 фазы вещества.
Для величин (параметров) характеризующих различные состояния воды и пара применяют следующие обозначения. Величины:
- относящиеся к холодной воде при 0С обозначают индексом ноль внизу.
- к кипящей воде отмечают индексом «`» сверху.
- к сухому насыщенному пару, индексом «``» сверху.
- к влажному пару индекс «ВЛ» в низу.
- к перегретому пару индекс «пе» в низу.
