1-Цитизил-3-ацетамид 6-фтор-1,2,3,4-тетрагидро- γ-карболина
Симаков С.В.1, Карцев В.Г.2, Рубан Л.Л.1, Першина С.Г.1, Лягин В.Н.1
1Белгородский государственный НИИ технологий медицинской промышленности
2InterBioScreen Ltd., Черноголовка
|
|
|
O |
|
O |
|
|
Cl |
|
|
F |
|
Cl |
F |
|
NH |
|
N |
|
|
|
|
N |
|
|
N |
Cl |
|
|
|
|
1 |
H |
|
|
H |
2 |
|
|
|
|
O |
|
|
|
F |
|
N |
|
|
|
|
|
|
HN |
N |
|
|
N |
N |
|
O |
|
|
|
|
|
|
|
H |
|
|
|
|
|
3 |
N |
|
|
|
|
|
|
|
|
|
O |
|
(1-Хлор-3-ацетил)6-фтор-1,2,3,4-тетрагидро-γ-карболин (2). К раствору 9.50 г (50 ммоль) 6-фтор-1,2,3,4-тетрагидро-γ-карболина 1 в смеси 100 мл сухого хлороформа и 30 мл диметилформамида прибавляют 3.95 г (50 ммоль) пиридина, затем при перемешивании и температуре не выше 40°С приливают 5.65 г (50 ммоль) хлорацетилхлорида. Реакционную массу перемешивают в течение 1 ч и выливают в 500 мл воды. Из смеси отгоняют хлороформ и выпавший при охлаждении осадок отфильтровывают. После высушивания и кристаллизации из этилового спирта получают 11.2 г (85%) соединения 2, Тпл 196–197°С.
1-Цитизил-3-ацетамид 6-фтор-1,2,3,4-тетрагидро-γ-карболин (3). Смесь 1.33 г (5 ммоль) соединения 2, 0.35 г (2.5 ммоль) К2СО3, 0.9 г (6 ммоль) NaJ и 1.05 г (5.5 ммоль) цитизина в 50 мл ацетона кипятят с обратным холодильником в течение 10 ч. Содержимое колбы выливают в 100 мл воды и оставляют на 12 ч при комнатной температуре. Осадок отфильтровывают, промывают теплой водой (100 мл), сушат. Выход соединения 3 составляет 72%, Тпл 157–158°С (этиловый спирт). Структура соединений 2 и 3 доказана методами ПМР, ИК, масс-спектро- скопии и элементным анализом.
Работа выполнена по идее и при поддержке InterBioScreen Ltd.
Избранные методы синтеза и модификации гетероциклов, том 1 |
591 |
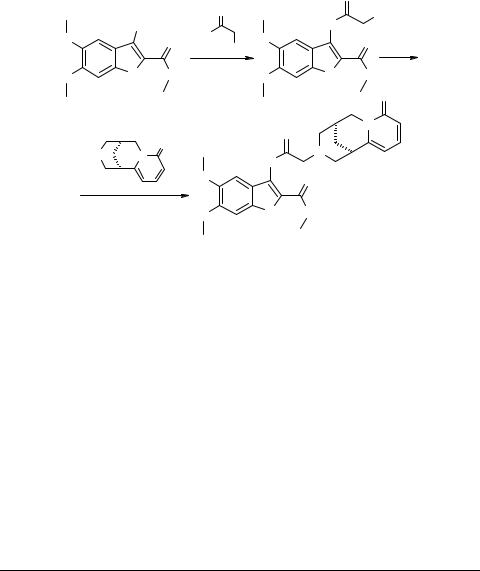
Метиловый эфир 3-(2-цитизил-1-ацетиламино)- 5,6-диметокси-1Н-2-индолкарбоновой кислоты
Симаков С.В.1, Карцев В.Г.2, Фофанов Г.М.1, Рубан Л.Л.1, Першина С.Г.1
1Белгородский государственный университет
2InterBioScreen Ltd., Черноголовка
|
|
|
O |
|
|
|
O |
|
NH2 |
|
|
|
HN |
Cl |
O |
O |
Cl |
Cl |
O |
O |
|
|
|
|
|
|
|
|
|
|
O |
N |
O |
|
|
O |
N |
O |
1 |
H |
|
|
|
|
2 H |
O |
|
|
|
|
|
|
O |
N |
|
|
O |
|
|
|
|
HN |
N |
|
|
|
N |
|
|
|
|
HN |
|
|
|
|
O |
|
|
|
3 |
|
|
|
|
O |
|
|
|
|
O |
|
N |
O |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
4 |
|
|
Метиловый эфир 3-(α-хлорацетил)амино-5,6-диметоксииндол-2-карбоновой кислоты (2). К раствору 25 г (0.1 моль) 3-амино-2-карбометокси-5,6-диметокси- индола 1 в 100 мл сухого хлороформа прибавляют 7.9 г (0.1 моль) пиридина, затем при перемешивании и температуре не выше 40°С приливают 11.3 г (0.1 моль) хлорацетилхлорида. Реакционную массу перемешивают 1 ч и выливают в 500 мл воды. Отгоняют хлороформ, осадок отфильтровывают. После сушки и перекристаллизации из этанола получают 27.8 г (85%) продукта 2, Тпл 167–168°С.
Метиловый эфир 3-(2-цитизил-1-ацетиламино)-5,6-диметокси-1Н-2-индолкар-
боновой кислоты (4). Смесь 3.27 г (10 ммоль) 2, 0.69 г (5 ммоль) K2CO3, 0.9 г (6 ммоль) NaJ и 2.1 г (11 ммоль) цитизина в 50 мл ацетона кипятят с обратным холодильником в течение 12 ч. Содержимое колбы выливают в 100 мл воды и оставляют на 10 ч при комнатной температуре. Выпавший осадок отфильтровывают, промывают теплой водой (100 мл) и сушат. Получают соединение 4, Тпл 183–184°С (из изопропанола). Выход 76%.
Структура соединений 2 и 4 доказана методами ПМР, ИК, масс-спектро- скопии и элементным анализом.
Работа выполнена по идее и при поддержке InterBioScreen Ltd.
592 |
Серия монографий InterBioScreen |
7,8-Дизамещенные 4,5-дигидро-3Н-пиримидо- [5,4-b]индол-4-оны
Симаков С.В., Фофанов Г.М., Антоненко В.В., Шапошников А.Ю.
Белгородский государственный университет
|
|
NH2 |
|
O |
|
|
|
R1 |
|
H2N |
H |
R1 |
|
N |
|
|
|
|
|
|
R2 |
N |
O |
|
|
R2 |
N |
NH |
|
|
|
|
|
H |
O |
|
|
|
H |
O |
|
1a−e |
|
|
|
2a−e |
|
|
|
|
|
|
1a, 2a R1 = F, R2 = H;
1b, 2b R1 = Cl, R2 = H;
1c, 2c R1 = Me, R2 = H;
1d, 2d R1 = Br, R2 = H;
1e, 2e R1 = R2 = OMe
0.1 моль соответствующего 5,6-дизамещенного 2-карбометокси-3-аминоиндола (1a–e) в 200 мл формамида кипятят в течение 4 ч с обратным холодильником, охлаждают до 80°С и выливают в 300 мл воды. Выпавший осадок отфильтровывают, промывают ацетоном (3 × 50 мл), диэтиловым эфиром (100 мл) и сушат. Выход соединений 2a–e составляет 75–80%. Тпл >300°С.
Структура соединений 2a–e доказана методами ПМР, ИК, масс-спектроскопии и элементным анализом.
Избранные методы синтеза и модификации гетероциклов, том 1 |
593 |
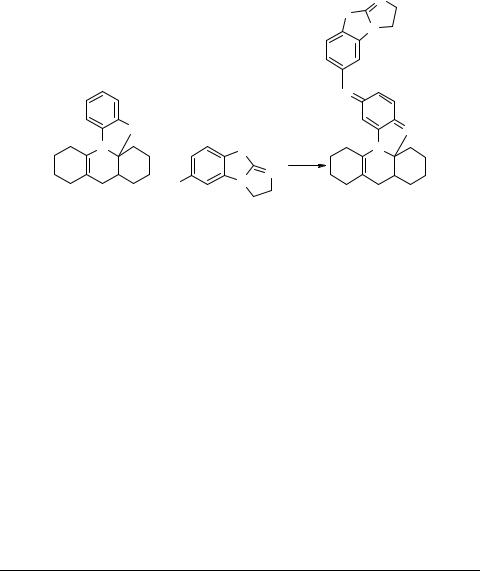
7[6-[2,3-Дигидропиразоло[1,2-b]бензотиазол- 6-ил]имино-1,2,7,10-тетрагидро-1,10а-циклогексано- 3,4-циклогексенопиридо[1,2-а]бензимидазол
Слабко О.Ю., Каминский В.А.
Дальневосточный государственный университет
|
|
|
N |
|
|
|
S |
|
|
|
N |
|
|
|
HN |
NH |
|
|
N |
N |
S |
MnO2 |
N |
+ |
N |
N |
|
H2N |
|
|
1 |
2 |
|
3 |
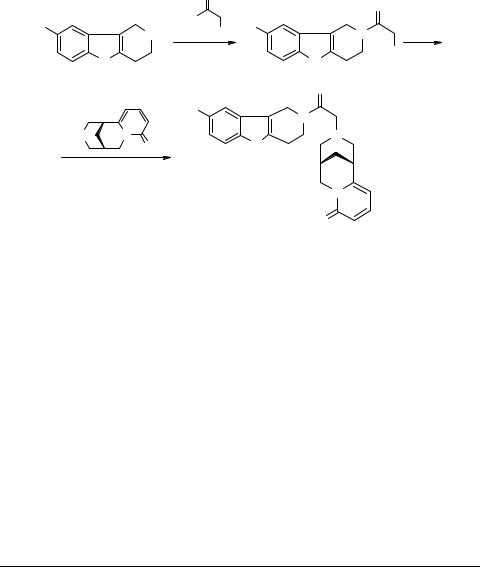
К раствору 0.5 г (2.6 ммоль) соединения 2 в 30 мл ацетона добавляют при перемешивании 0.65 г (2.3 ммоль) соединения 1 [1], 3 г (34.5 ммоль) MnO2 и перемешивают в течение 30 мин до исчезновения в реакционной смеси исходного 1 (контроль с помощью ТСХ). Отфильтровывают MnO2 (фильтр Шотта №3), промывают его несколько раз ацетоном (по 5 мл) до обесцвечивания промывочного раствора. При охлаждении до 0°С из фильтрата выпадает мелкокристаллический осадок продукта 3. Его отфильтровывают и промывают холодным ацетоном. Фильтрат разбавляют водой в 2 раза и добавляют NaCl до выпадения осадка. Оба осадка объединяют и кристаллизуют из смеси гексан–ацетон (1 : 2). В результате получают 0.92 г темно-вишневого кристаллического соединения 3. Выход 88%. Тпл 154–156°С. Структура соединения 3 доказана методами ИК, ПМР спектроскопии и элементным анализом.
Реактив 2 был предоставлен компанией InterBioScreen Ltd.
1.Еремеева Л.М., Московкина Т.В., Василенко Ю.В. и др., ХГС 1979 (2) 240.
594 |
Серия монографий InterBioScreen |
8-Карбоксиметилентио-7-оксо-1,2,7,10-тетрагидро- 1,10а-циклогексано-2-R-3-R1-4-R2-
пиридо[1,2-a]бензимидазолы
Слабко О.Ю., Каминский В.А.
Дальневосточный государственный университет
|
|
|
|
|
|
OH |
|
O |
|
|
|
O |
O |
|
R2 |
|
|
|
R2 |
S |
|
O OH NaOH |
|
|
R1 |
N |
R1 |
N |
|
|
N |
+ |
EtOH |
|
N |
|
R |
HS |
R |
|
|
|
|
|
|
1а, b |
|
|
|
2а, b |
|
aR = H, R1-R2 = Ph
bR = R2 = Ph, R1 = H
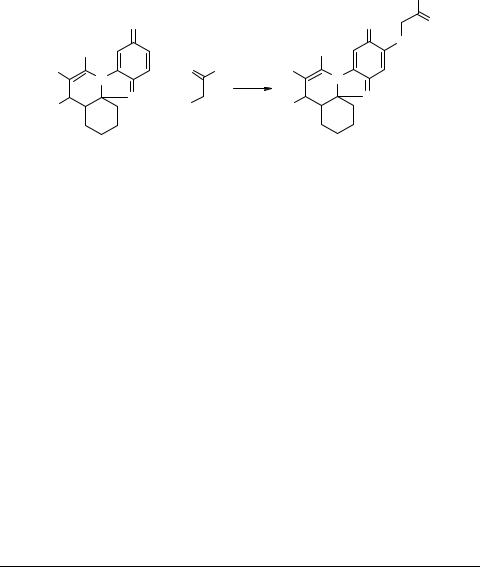
Суспензию 2.2 ммоль соединения 1 [1] (1а 0.65 г, 1b 0.85 г) в 30 мл этанола нагревают до полного растворения, охлаждают до 40°С и добавляют 0.4 г (4.5 ммоль) тиогликолевой кислоты и раствор 0.18 г (4.5 ммоль) NaOH в 10 мл этанола. Перемешивают при комнатной температуре 3–4 ч до исчезновения в реакционной смеси исходного 1 (контроль – ТСХ). Реакционную смесь разбавляют водой в 2 раза и нейтрализуют 5% раствором соляной кислоты. В случае соединения 2а реакционную смесь экстрагируют эфиром, из которого выпадает чистый продукт 2а. В случае соединения 2b после нейтрализации водного раствора выпадает красный осадок, кристаллизацией которого из этилацетата получают чистый продукт 2b. Соединение 2а: выход 65%, Тпл 152–154°С, темнокрасные кристаллы; соединение 2b: выход 77%, Тпл 200–202°С, ярко-красные кристаллы.
Структура соединений 2а, 2b доказана методами ИК, ПМР спектроскопии, масс-спектрометрии и элементным анализом.
1.Каминский В.А., Слабко О.Ю., Тиличенко М.Н., ХГС 1988 (6) 793.
Избранные методы синтеза и модификации гетероциклов, том 1 |
595 |
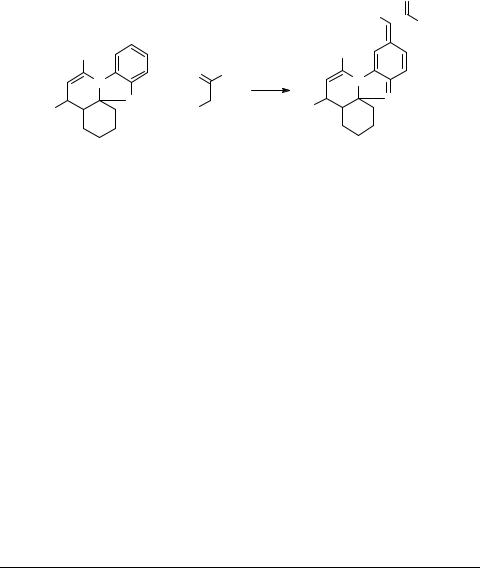
2,4-Дифенил-7-карбэтокси(нитро)метилено- 1,2,7,10-тетрагидро-1,10а-циклогексано- пиридо[1,2-а]бензимидазол
Слабко О.Ю., Каминский В.А.
Дальневосточный государственный университет
O
O2N  OEt
OEt
|
Ph |
|
|
|
Ph |
|
N |
O |
OEt MnO |
|
N |
|
+ |
2 |
|
|
|
|
|
Ph |
NH |
EtOH |
Ph |
N |
|
O2N |
|
|
|
1 |
|
|
|
2 |
К раствору 1.3 г (10 ммоль) этилового эфира нитроуксусной кислоты в 100 мл этанола прибавляют 2 г (5 ммоль) соединения 1 [1] и 10 г (110 ммоль) MnO2 и перемешивают в течение 1.5 ч до исчезновения в реакционной смеси исходного соединения 1 (контроль с помощью ТСХ). Отфильтровывают MnO2 (фильтр Шотта №3), промывают его несколько раз ацетоном (по 5 мл) до обесцвечивания промывочного раствора. Фильтрат разбавляют водой в 2 раза до выпадения осадка. Осадок отфильтровывают, сушат и подвергают хроматографическому делению на Аl2O3 (этилацетат–гексан 1 : 10). После отгонки растворителя получают 1.8 г продукта 2 в виде сине-фиолетового порошка. Выход 68%. Тпл 194–196°С. Структура соединения 2 доказана методами ИК, ПМР спектроскопии и элементным анализом.
1.Еремеева Л.М., Московкина Т.В., Василенко Ю.В. и др., ХГС 1979 (2) 240.
596 |
Серия монографий InterBioScreen |
4-[3-(3-Бромфенил)-5,6-диметокси-1-(4-метилфенил- сульфонил)-1Н-индол-2-ил]-2-бутанон
Смирнов С.К., Строганова Т.А., Бутин А.В.
Кубанский государственный технологический университет
|
|
|
|
|
Br |
|
PCl5 |
|
O |
|
HNO3 |
|
|
|
|
|
O |
|
|
|
|
O AlCl3, |
|
O |
O |
AcOH |
OH |
O |
|
|
2 |
|
|
|
NO2 |
Fe |
O |
|
NH2 |
TsCl |
O |
AcOH |
O |
|
O |
NaHCO3 |
|
|
|
|
|
3 |
Br |
|
|
Br |
|
|
|
4 |
|
NHTs |
NaBH4 |
O |
|
NHTs |
TsOH |
|
|
|
|
O |
|
O |
|
OH |
|
|
|
|
O |
|
|
|
|
|
Br |
|
|
6 |
Br |
5 |
|
|
|
|
NHTs |
|
HCl |
O |
NTs |
|
|
|
|
|
O |
|
O |
|
O |
|
|
|
Br |
|
|
|
Br |
7 |
|
|
8 |
|
|
|
|
|
Избранные методы синтеза и модификации гетероциклов, том 1 |
597 |

3-Бромфенил-3,4-диметоксифенилметанон (2). К раствору 100 г (0.5 моль) 3-бромбензойной кислоты в 120 мл нитробензола при охлаждении водой добавляют 118 г (0.57 моль) PCl5, после чего смесь выдерживают на водяной бане при температуре 50–60°С в течение 45 мин, охлаждают до комнатной температуры и помещают в ледяную баню. К охлажденному раствору добавляют 75 г (0.56 моль) безводного AlCl3 так, чтобы температура не превышала 20°С, затем по каплям 69 мл (0.47 моль) вератрола при той же температуре. Реакционную смесь нагревают на водяной бане при 60–70°С в течение 2 ч. После окончания выделения хлористого водорода реакционную смесь выливают в лед и обрабатывают 20–25 мл соляной кислоты. Растворитель отгоняют с паром, органический остаток в горячем состоянии выливают в холодную воду и перемешивают до затвердения, кристаллизуют из смеси гексан–CH2Cl2. Получают 2 в виде белого порошка. Выход 73%.
Тпл 98–99°С.
3-Бромфенил-4,5-диметокси-2-нитрофенилметанон (3). К раствору 32 г (0.1 моль) 2 в 60 мл AcOH, помещенному в ледяную баню, добавляют по каплям 27 мл HNO3 (красной дымящей) в течение 5 мин. Реакционную смесь выдерживают 10 мин в ледяной бане, 25 мин на кипящей водяной бане, а затем выливают в лед и обрабатывают 95 г KOH. Выпавший осадок фильтруют, промывают водой, сушат и кристаллизуют из смеси гексан–CH2Cl2. Получают кристаллы светло-зеленого цвета. Выход 88%. Тпл 124–125°С.
2-Амино-4,5-диметоксифенил-3-бромофенилметанон (4). Смесь 33 г (0.09 моль)
3, 36 г (0.64 моль) порошкового железа, 40 мл этилацетата и 18 мл AcOH в 120 мл воды перемешивают при нагревании на кипящей водяной бане в течение 10 ч. Реакционную смесь охлаждают и аккуратно добавляют 130 г NaHCO3. Полученную суспензию перемешивают при нагревании еще 2 ч и фильтруют. Осадок на фильтре тщательно промывают горячим этилацетатом. Растворитель отгоняют в вакууме, остаток кристаллизуют из смеси этилацетат–гексан. Получают кристаллы ярко-желтого цвета. Выход 88%. Тпл 111–113°С.
N-[2-(3-Бромбензоил)-4,5-диметоксифенил]-4-метил-бензолсульфонамид (5). К
раствору 24.5 г (0.073 моль) 4 в 120 мл ацетона добавляют 42 г (0.22 моль) п-толуолсульфохлорида и кипятят полученную смесь 5 мин. Затем добавляют 19 г (0.22 моль) NaHCO3 и 40 мл воды. Суспензию кипятят в течение 7 ч. Реакционную смесь охлаждают, выпавший осадок отфильтровывают и кристаллизуют из смеси гексан–CH2Cl2. Получают бледно-желтые кристаллы. Выход 89%.
Тпл 163–164°С.
N-{2-[(3-Бромфенил)-гидроксиметил]-4,5-диметоксифенил}-4-метилбензол-
сульфонамид (6). К кипящему раствору 32 г (0.065 моль) 5 в 450 мл этанола порциями добавляют 5 г (0.13 моль) NaBH4, кипячение продолжают еще 10 мин. Смесь охлаждают и подкисляют разбавленной соляной кислотой до рH 5–6. Выпавший осадок отфильтровывают и кристаллизуют из смеси гексан–CH2Cl2.
Выход 87%. Тпл 232–233°С.
598 |
Серия монографий InterBioScreen |
N-{2-[(3-Бромфенил(5-метил-2-фурил)метил]-4,5-диметоксифенил-4-метил-
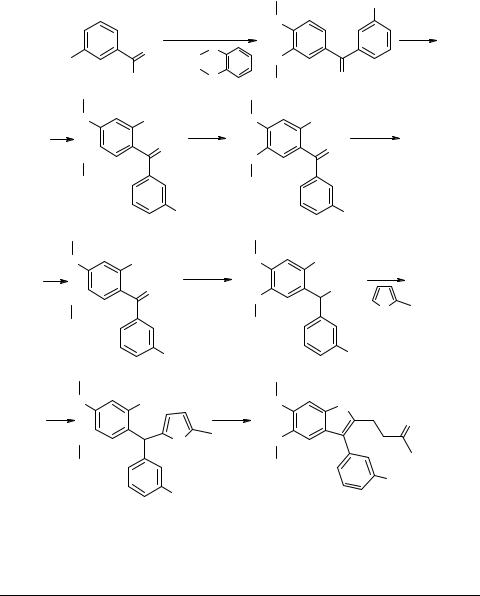
бензолсульфонамид (7). 10 г (0.02 моль) 6 кипятят с обратным холодильником в 200 мл CH2Cl2 с 1 г (0.005 моль) п-толуолсульфокислоты в течение 1 мин, затем добавляют 5.4 мл (0.06 моль) сильвана и кипятят до полного исчезновения исходного продукта 6 (ТСХ контроль). Реакционную смесь охлаждают, добавляют 50 мл холодной воды и нейтрализуют NaHCO3. Органический слой отделяют, сушат над Na2SO4 и отгоняют растворитель. Сухой остаток кристаллизуют из смеси гексан–CH2Cl2. Выход 75%. Тпл 161–162°С.
4-[3-(3-Бромфенил)-5,6-диметокси-1-(4-метилфенилсульфонил)-1Н-2-индолил]- 2-бутанон (8). К раствору 11.1 г (0.02 моль) 7 в 10 мл CH2Cl2 добавляют 50 мл этанола, насыщенного HCl, и кипятят в течение 20 мин, затем приливают 30 мл этанола и продолжают кипячение до полной конверсии 7 (ТСХ контроль). Полученную суспензию разбавляют водой и нейтрализуют NaHCO3, осадок отфильтровывают и кристаллизуют из смеси гексан–CH2Cl2. Выход 75%. Тпл 115–116°С.
Структура соединений 2–8 доказана методами ИК, ПМР спектроскопии и элементным анализом.
Избранные методы синтеза и модификации гетероциклов, том 1 |
599 |
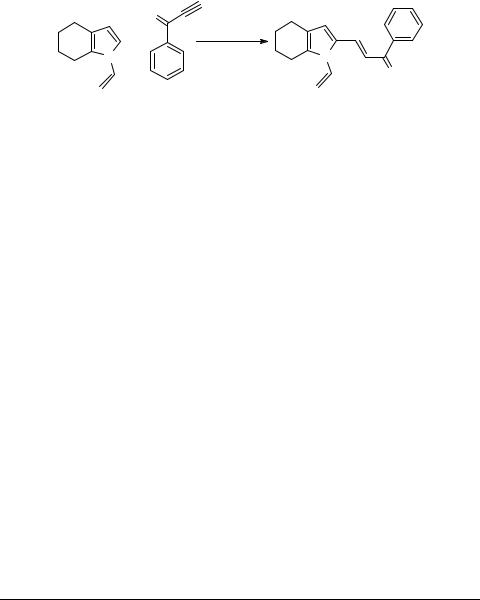
1-Фенил-3-(1-винил-4,5,6,7-тетрагидро- 1Н-индол-2-ил)-пропенон
Степанова З.В., Собенина Л.Н., Михалева А.И., Трофимов Б.А.
Иркутский институт химии им. А.Е. Фаворского СО РАН
|
O |
(SiO2)n mH2O |
|
+ |
|
N |
|
N |
|
|
O |
1 |
2 |
3 |
К смеси 0.073 г (0.5 ммоль) 1-винил-4,5,6,7-тетрагидроиндола 1 [1] и 0.065 г (0.5 ммоль) бензоилацетилена 2 добавляют 10-кратный весовой избыток силикагеля, растирают до однородного состояния и выдерживают при комнатной температуре, периодически встряхивая, до появления устойчивого темно-оранже- вого окрашивания. После этого реакционную смесь выдерживают до полного изчезновения исходных соединений (контроль методом ТСХ ацетонового экстракта), переносят на колонку с Al2O3 и вымывают гексаном желто-оранжевую фракцию. Остаток после удаления растворителей (оранжевое масло) очищают перекристалллизацией из смеси гексан–диэтиловый эфир, 2 : 1. Получают 0.116 г (84%) пиррола 3. Тпл 80–81°C (желтые призмы).
Структура соединения 3 подтверждена 1Н ЯМР, ИК спектрами и элементным анализом.
1.Trofimov B.A., Stepanova Z.V., Sobenina L.N., et al., Synthesis 2001 1878.
600 |
Серия монографий InterBioScreen |









 OEt
OEt

