- •1.Классификация органических соединений. Важнейшие функциональные группы. Примеры.
- •2. Понятие о взаимном влиянии атомов в молекуле, электронные эффекты (положительные и отрицательные индуктивный и мезомерный эффекты).
- •3. Классификация органических реакций (по механизму и по конечному результату). Гомолитический и гетеролитический способы разрыва связей. Электрофильные и нуклеофильные реакции. Примеры.
- •5.Особенности многоатомных спиртов. Биологическая роль этиленгликоля и глицерина.
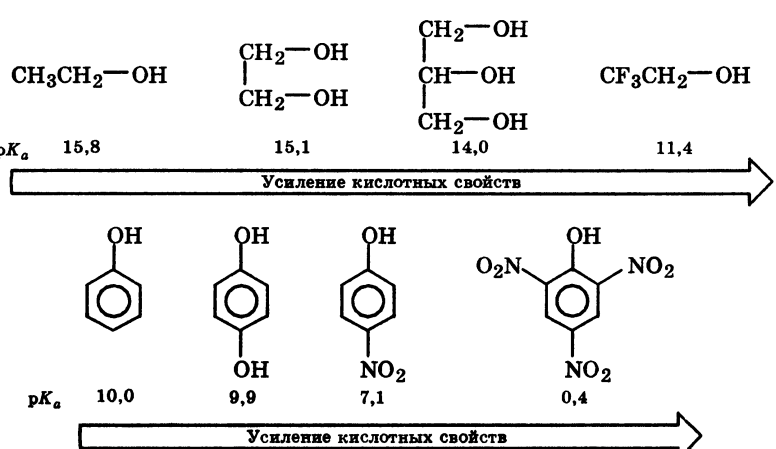
- •6.Химические свойства фенолов: кислотно-основные, окислительно-восстановительные.
- •7. Карбонильные соединения: альдегиды, кетоны. Строение, классификация. Примеры.
- •8.Тип гибридизации атомных орбиталей карбонильного атома углерода. Распределение электронной плотности в молекулах. Реакционные центры альдегидов и кетонов: электрофильный, основный, сн-кислотный.
- •10.Взаимодействие альдегидов а) со спиртами (образование ацеталей и полуацеталей); б) с водой; в) с аммиаком, аминами (образование иминов-оснований Шиффа); г) с циановодородной кислотой.
- •11. Окислительно-восстановительные свойства альдегидов и кетонов: реакции альдольной и кротоновой конденсации, окисление альдегидов, кетонов, биологическое окисление.
- •14.Образование сложных эфиров, тиоэфиров, амидов, ангидридов, галогенгидридов карбоновых кислот. Ацетилкофермент а in vivo как переносчик ацильных групп на нуклеофильные субстраты.
- •16.Гетерофункциональные органические соединения (кетокислоты, гидроксикислоты, аминокислоты, аминофенолы, аминоспирты. Привести примеры.
- •17. Α-Аминокислоты. Строение, классификация α-Аминокислот по природе радикала: алифатические, ароматические, гетероциклические. Заменимые и незаменимые α-Аминокислоты. Привести примеры.
- •18. Свойства α-Аминокислот. Кислотно-основные свойства. Понятие об изоэлектрической точке (рI).
- •21. Липиды как сложная по составу группа органических веществ. Классификация липидов: химическая и функциональная. Биологическая роль липидов.
- •22. Высшие жирные кислоты (вжк): строение, конфигурация двойных связей, биологическая роль.
- •23. Омыляемые простые липиды: а) воски (спермацет, пчелиный воск); б) жиры, масла. Триаглицерины: общая структура, твердые, жидкие. Примеры. Свойства липидов: гидролиз, реакция
- •24. Омыляемые сложные липиды. Фосфолипиды, классификация. Фосфатидные кислоты. Фосфатидилэтаноламин, фосфатидилхолин, фосфатидилсерины, фосфатидилинозиты, плазмагены.
3. Классификация органических реакций (по механизму и по конечному результату). Гомолитический и гетеролитический способы разрыва связей. Электрофильные и нуклеофильные реакции. Примеры.
По конечному результату:
Реакции замещения. Их обозначают символом S (от англ. substitution). В зависимости от природы атакующего реагента замещение может быть радикальное (SR), электрофильное (SE) и нуклеофильное (SN). Замещаемая часть субстрата называется уходящей группой. При радикальном замещении уходящий свободный радикал тут же вступает в реакцию. Реакции присоединения. Их обозначают символом А (от англ. addition). Присоединение может происходить также по трем механизмам: радикальное (АR), электрофильное (AE) и нуклеофильное (AN). Реакции отщепления (элиминирования) обозначают символом Е (от англ. elimination).Чаще в этих реакциях отщепляющиеся группы уходят от соседних атомов углерода (β-элиминирование). Реакции перегруппировки. В результате процесса перегруппировок происходит переход атомов или групп от одного атома к другому. Наиболее распространен переход мигрирующей группы к соседнему атому (1,2-перегруппировка). Мигрирующая группа может переходить с одним (радикальная) или парой электронов (нуклеофильная) перегруппировка.
По механизму разрыва связей:
По
этому признаку реакции подразделяют
на радикальные и ионные. Радикальные
реакции. При
гомолитическом разрыве ковалентной
связи образуются радикалы, имеющие по
одному неспаренному электрону:

Примерами радикальных реагентов являются атомы галогенов Br•, Cl •, гидроксильные НО•, гидропероксильные НОО•, алкилпероксильные ROO•, алкильные R•.
Ионные реакции. При гетеролитическом разрыве ковалентной связи пара электронов переходит к одному из партнеров связи. При этом образуются электрофильные и нуклеофильные частицы:

Электрофилы – частицы, образующие новые ковалентные связи за счет пары электронов партнеров (обозначаются символом Е+). Электрофильными реагентами являются: положительно заряженные ионы Н+, Br+, Cl+, NO2+, ≡C+; нейтральные молекулы, имеющие электронодефицитный центр: SO3, ≡Cδ+→X, кислоты Льюиса (FeBr3, AlCl3, BF3). Нуклеофилы – это частицы, образующие новые ковалентные связи, предоставляя партнеру пару электронов (обозначаются символами :Nu или Nu–). Нуклеофильными реагентами являются: отрицательно заряженные ионы: Br–, Cl–, HO–, HS–, RO–, RS–; нейтральные молекулы, имеющие неподеленную электронную пару гетероатома: H2O, ROH, RSH, NH3, RNH2, R2NH, R3N; доноры π-электронов: = С = С =, ароматическое кольцо.
![]()

![]()

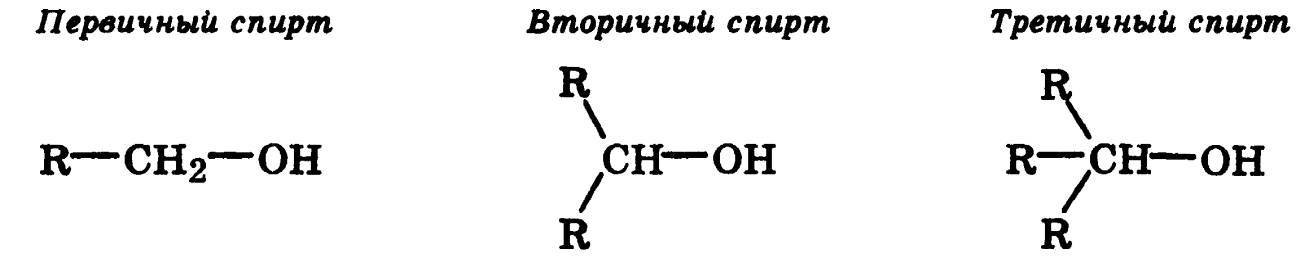
4.классификация и изомерия спиртов и фенолов. Химические свойства спиртов: кислотно-основные, с разрывом связи R-OH, окислительно-восстановительные.

Для спиртов характерна структурная изомерия:
- изомерия положения ОН-группы - начиная с С3;
- углеродного скелета - начиная с С4;
(например, формуле C4H9OH соответствует 4 структурных изомера)
- межклассовая изомерия с простыми эфирами;
(например, этиловый спирт СН3CH2–OH и диметиловый эфир CH3–O–CH3)
- Возможна пространственная изомерия - оптическая;
(например, бутанол-2 СH3"C"H(OH)СH2CH3, в молекуле которого второй атом углерода связан с четырьмя различными заместителями, существует в форме двух оптических изомеров)
Фенолы – гидроксисоединения, в молекулах которых ОН-группы связаны непосредственно с бензольным ядром.
В зависимости от числа ОН-групп различают одноатомные фенолы (например,фенол и крезолы) и многоатомные. фенолам свойственна структурная изомерия (изомерия положения гидроксигруппы)


![]()






![]()

![]()




 окислительно-восстановительные
реакции спиртов:1) внутримолекулярная
дегадратация
окислительно-восстановительные
реакции спиртов:1) внутримолекулярная
дегадратация

2)реакция дегидрирования
 первичные
спирты окисляются в альдегиды, а вторичные
в кетоны!!!
первичные
спирты окисляются в альдегиды, а вторичные
в кетоны!!!
3)

4)

5)