
- •Міністерство Освіти України
- •Змістовий модуль 3. Методи виявлення та ідентифікації іонів.
- •Теми лабораторних робіт
- •Таблиця 2 Аналітичні класифікації іонів
- •Таблиця 3 Кислотно-основна класифікація катіонів
- •I група катіонів.
- •Таблиця 4
- •II група катіонів.
- •Таблиця 5
- •III група катіонів.
- •Таблиця 7
- •Таблиця 8
- •IV група катіонів.
- •Таблиця 9
- •V група катіонів.
- •Таблиця 11
- •VI група катіонів
- •Таблиця 13
- •Таблиця 14
- •Таблиця 15
- •Алгоритм загальної характеристики аніонів
- •I Таблиця 16група аніонів Загальні реакції аніонів I групи
- •Таблиця 17
- •II група аніонів Таблиця 18
- •Таблиця 19
- •III група аніонів
- •Таблиця 20
- •Таблиця 21
- •Таблиця 22
- •Таблиця 23
- •Кислотно-основна схема розділення суміші катіонів I – III груп.
- •Кислотно-основна схема розділення суміші катіонів IV – VI груп.
- •Д Таблиця 24одатки Додаток 1: «Органічні реагенти»
- •Список рекомендованої літератури
- •Кислотно-основна схема аналізу суміші аніонів іі групи…………………... 22
Таблиця 21
Переваги та недоліки методу осадження
|
|
Переваги |
Недоліки |
|
|
Простота і надійність у виконанні |
Тривалість операцій осадження |
|
|
Наочність |
Складності при відділенні осаду від розчину |
|
|
Дозволяє розділити суміші іонів при правильному виборі осаджувача |
Можливість соосадження іонів
|
|
|
Дозволяє знайти велику кількість іонів |
Концентраційні обмеження |
Таблиця 22
Основні осаджувачі кислотно-основного методу
-
Органічні
Неорганічні
диметилгліоксим, 8-оксіхінолін, дитизон, дифенілкарбазид, алізарин, магнезон, дифеніламін, трілон Б.
H2SO4, HCl, NaOH, NH4OH.
Таблиця 23
Прийоми підвищення селективності методу осадження
варіювання величини рН;
попереднє окислювання або відновлення елементів;
маскування елементів.
Систематичний аналіз заснований на послідовному виділенні невеликої кількості іонів, їхніх груп за допомогою селективних реагентів з наступним дробовим виявленням, а при необхідності з додатковим поділом у кожній групі. Існує кілька схем систематичного аналізу сумішей катіонів і аніонів. Будь-яка схема поділу передбачає строгу послідовність відділення груп. На практиці для аналізу сумішей елементів використовують сполучення дробового і систематичного методів. Розглянемо наступні схеми аналізу суміші іонів по кислотно-основній класифікації катіонів:
Кислотно-основна схема розділення суміші катіонів I – ІІ груп
Кислотно-основна схема розділення суміші катіонів IІІ – ІV груп
Кислотно-основна схема аналізу суміші катіонів V– VI груп
Кислотно-основна схема аналізу суміші катіонів I – VI груп
Схема аналізу суміші аніонів II групи
Схема аналізу суміші аніонів I – III групп
Кислотно-основна схема розділення суміші катіонів I – III груп.
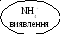

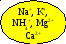

PbCl2,
AgCl, PbSO4,
BaSO4,
SrSO4,
CaSO4
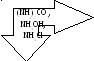
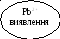


CaCO3 AgCl,
Hg2Cl2,
PbSO4,
BaSO4,
SrSO4,
CaSO4
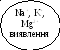
PbSO4,
BaSO4,
CaSO4,
Hg
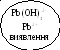


BaCO3,
SrCO3,
CaCO3

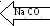
BaSO4,
SrSO4,
CaSO4
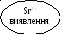
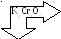
BaCrO4
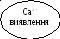
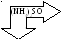
SrSO4
Кислотно-основна схема розділення суміші катіонів IV – VI груп.
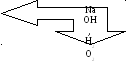


Гідроксиди
V
та VI груп

Al(OH)3

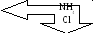
Cu2S
Fe(OH)3,
BiOCl, Mg(OH)2,
MnO(OH)2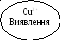


HgS Fe(OH)3,
BiOCl, MnO(OH)2
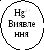
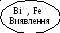
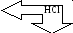
MnO(OH)2
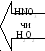
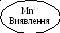
Кислотно-основна схема розділення суміші катіонів I – VI груп.



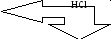 Cu2+
р. с NH3
Cu2+
р. с NH3
Al3+ р. с алізарином
Mn2+ р. с PbO2
Cr3+ р. с H2O2
Катіони
II групи
 Hg2+
р. с Cu
Hg2+
р. с Cu
Fe2+ р. с K3[Fe(CN)6]
Fe3+ р. с KSCN
NH4+ р. с NaOH

 Na+
р. с Zn(UO2)Ac8
Na+
р. с Zn(UO2)Ac8
Co2+ р. с NH4SCN
Катіони
III групи


Катіони
V,
VI груп

Катіони
IV групи
Катіони
III групи
Катіони
V групи
Схема аналізу суміші аніонів II групи.
AgCl,
AgBr, AgI 

AgBr,
AgI


Ag


С хема
аналізу суміші аніонів I – III
груп.
хема
аналізу суміші аніонів I – III
груп.

BaCO3,
BaSO3,
BaSO4,
BaHPO4

NO2-
з KMnO4 NO3-
з
Zn, H2SO4
(конц.)


BaSO4 SO2
з KMnO4 CO2
з
Ca(OH)2,
р-н

MgNH4PO4
