Шпоры / Все шпоры 2
.docx
Mолекулярная биология - это наука о механизмах хранения, воспроизведения, передачи и реализации генетической информации, о структуре и функциях нерегулярных биополимеров - нуклеиновых кислот и белков. История развития: название науки дал Эстбюри в 1939, в 40 впервые получил рентгенограму ДНК.М.б. сформир. Во второй половине 20 века на стыке наук :биоогр.химия, физ-химбио., биофиз, биохим, био, м.б. сначало преобладало физ-хим подход, затем сдвиг перешел в сторону био. М.Б. зародилась в Ронфллеровском фонде 1938г. Основой науки послужило развитие физ-хим метода анализов и открытие отраслей био- ген. Цитологии биохим. Центральное звено М.Б молек основы наследствености механизмы передачи и реализации признаков в поколениях и в онтогенезе. Основные методы: -микроскония: световая, люминесцентная, электронная, -рентгенноструктурный анализ опред. Располож. Атомов в молекле с помощью рентген.лучей -радиоактивные изотопы -центрифугирование -хроматографил -электрофорез -культуры клеток -Бесклеточные системы -клонирование НК систем белков in-vitro и изуч. Их функций Совр. напр. М.Б.: геномика, протогеномика, биоинформатика, моделирование пространственной структуры макромолекул, молекулярные основы эволюции и биоразно, деференцировки развития и строения, канцерогена и иммунитета,), биотехнология производство продуктов и соед(гормонов, энергоносителец) в культурах клетки.
|
3. Строение белков. Строение аминокислот. Стереохимические формы. В белки входят 20 АК протеиногенные и канонические . 21 АК селеноцистеин, входят в состав каталитически активных Б – глутатион-пероксидаза, глицин-редуктаза. АК не обладают зарядом вблизи нейтральных значений рН. В водных растворах превращаются в биополярные ионы-цветирионы. АК производные карбоновых кислот преимущественно альфа-АК. Вета АК встречаются в Б потому что цепь подвижнее, нарушается самопроизвольное свертывание цепи. Альфа и L формы энергетически выгодны. По расположению NH2 и COOH : -транс форма преимуществено в Б 6 атомов наход.в 1 плоскости. Полипептид – цепочка плоских звеньев -цис форма в циклич. Б пептидные антибиотики грамициодин 5 и циклоспорин. Пептиды впервые были синтезированы в нач. 20 в Фишером. 4. Пространственная организация белков: первичная, вторичная, сверхвторичная, третичная, четвертичная структура, домены. 3D структуру Б поддерж.несколькосил:пептидная и дисульфидная связь. Подвидныесвязи:водородные, ионные, гидрофобные. Под первичной понимают порядок чередования АК остатков в полипептидной цепи Б. Вторичная: Полинг и Кори в 1951 сформ.принципы организации вторичных структур Б альфа и бета формы. Альфа спираль правозакрученная из L-АК. Радиус 0,23нм. Стабилизирована водородными связями плотная укладка внутр.часть непроницаема даже для воды. Бета структура водор.связями возникают между перелельными участками цепи. Очень широко представлены в Б- бета фибрион шелка, альфа-кератин. Б. часто состоят из разных типов вторичных структур: тип альфа из альфа-спирали, тип вете из вета спирали, тип альфа+бета тип альфа\бета. Сверхвторичные энергетически предпочитаемые ансамбли. Предпочтительны для форм.полипептидной цепи по мере синтеза и придания стабильности пространственной структуре Б Третичная: хар-сяопред.укладкой в пространстве всех звеньев полипептид.цепи. стали изучать с помощью денатурации и ренатурации Б. денатурация потеря нативной третичной структуры, связан с нарушением внутр связи. Причины: изменения внешнего окружения(рН, ионной силы) Ренатурациявосстонов нормальной глобулярной структуры. Четвертичная :объединение нескольких Б протомеров =субъединицы. Легко диссоциируют и собираются. Как правило Б состоят из четного кол-ва субъединиц. Домены: структурные домены Б установлены по повышенойэлектр плотности участков Б.в одной цепи может быть несколько доменов. Функциональные домены состоят из одного или нескол структурных доменов. Они выполняют несколько функций; ферментативная реакция, присоед вещ-коферментов, антигенов. Многие структ домены сходны у разных Б. |
Белки определяют фенотип организма. Обладают разнообразием структуры и функций. Строение запрограмировано в ДНК но в структуром и функциональном отношении белки более вариабельна, чем кодирующие полинуклиотиды. Белки — важная часть питания животных и человека,поскольку в их организмах не могут синтезироваться все необходимые аминокислоты и часть должна поступать с белковой пищей. В процессе пищеварения ферменты разрушают потреблённые белки до аминокислот, которые используются для биосинтеза собственных белков организма или подвергаются дальнейшему распаду для получения энергии. Функции : -ферменты био катализаторы опред.метаболизм клетки и организма -регуляторные белки регул.репликации транскрипции и трансляции контролируют своевременость и точность основных мол-ген процессов -гормоны физиологическая активность тканей и органов -структурные белки компоненты био мембран основа цитоскелета входят в состав соед.тканей кожи и т.д. -защитные защита от чужерродныхсоед. И паогенных микроорганизмов - транспортные переносчики кислорода
|
Регулярными наз. вторичные структуры, обр. ам/к остат. с одинаковой конформацией главной цепи (углы φ и ψ), при разнообразии конформаций боковых групп. К регулярным вторич. стр. отн.: спирали, к-рые м.б. левозакрученными и правозакрученными с разным периодом и шагом. Водородная связь при этом обр. м/у карбонильной группой одного аминокислотного остатка и аминогруппой др., лежащего ближе к N-концу полипептида. К спиральным структурам, которые встречаются в белках, относятся: -α-спираль, или спираль 413, — самая распространённая в белках вторичная структура. Данная спираль характеризуется плотными витками вокруг длинной оси молекулы, один виток составляет 3,6 аминокислотных остатка, и шаг спирали составляет 0,54 н. -β-листы (β-структура, складчатые слои) — несколько зигзагообразных полипептидных цепей, в которых водородные связи образуются между относительно удалёнными друг от друга (0,347 нм на аминокислотный остаток[3]) в первичной структуре аминокислотами или разными цепями белка, а не близко расположенными, как имеет место в α-спирали. -полипролиновая спираль — плотная левая спираль, которая стабилизирована Ван-дер-Ваальсовыми взаимодействиями, а не системой водородных связей.
Это каталитически активные антитела. В широком смысле термином «абзимы» обычно называют моноклональные каталитически активные антитела, обладающие свойствами ферментов — то есть катализирующие определенные химические реакции. Это соед свойства антител и ферментов, которые узнают вещества и прочнее связывают с лигандами, чем ферменты. Абзимы молока человека обладают амилолитической и протеинкиназовой активностью, фосфорилируют белки молока, часть способна гидролизовать ДНК и РНК. Играют роль в защите новорожденных от вирусных инфекций. Искусственные абзимы были получены в 1986г. Существует два основных механизма происхождения каталитических активностей антител. Согласно первому механизму, активные центры антител могут имитировать переходные состояния соответствующих химических реакций. По второму механизму, называемому Антиидиотипической сетью Эрне, активные центры антител представляют собой антиидиотипы активных центров других антител (которые в таком случае являются антигенами). Показано образование антиидиотипических антител до седьмого порядка.
|
Фолдинг –образование определенных складок,изгибов в полипептидной цепи, т.е процесс становления третичной структуры белка. В 1987г было предложено называть белки обслуживающие фолдинг молекулярными шаперонами . Формирование нативной структуры белка – фолдинг, в клетке может быть затруднена. Существует 3 группы белков помощников способств нормальной укладке- молекул шапероны: -нуклеоплазмины участвуют в сборке нуклеосом в ядре, -группа белков теплового шока, -шаперонины-собственно белки шапероны, помогают сворачивать цепи в нативный белок. Шаперонины-белковые комплексы в бактериях, цитоплазме эукариот клеток, матриксе митохонд и хлоропластов. Способствуют сворачиванию синтезируемых цепей, защищают расплав глобулы цепи от агрегации. Функции шаперонов: 1.в укладке белков-репликации, 2.укладка секреторных белков, 3.укладка рецепторов-гормонов. 8. Надмолекулярные белковые и полиферментные комплексы – адсорбционные, интегральные, метаболоны. Для интенсивного метаболизма продукты передаются по цепочке до полного превращения. Образование таких структур связано с необходимостью поддержания высоких скоростей метаболических превращений в живой клетке. Иными словами скорость обновления молекул должна преобладать над скоростью распада. Среди полиферментативных комплексов различают: абсорбционныеансамбли ферментов образуются за счет сил слабых взаимодеств между молекулами ферментов на поверхности мембраны какой-либо центр молекулы. интегральныекомплексы оказываются встроены во внутриклеточные мембраны.( относят цепочки окис-вост ферментов встроенные во внутренние мембраны митохондрий. Эти ансамбли ферментов осуществляют быструю передачу электронов с окисляемого субстрата на кислород, благодаря чему создаются условия для сопряженного с этим процессом синтеза АТР. Метаболоныэто крупные адсорбционные комплексы ферментов катализирующие серию реакций метаболических путей. В составе известных метаболонов гликолза и цикла Кребса входят адресная эстафетная передача субстратов. |
Один из видов полиферментных комплексов- протеасомы. Это крупные имеющие опред план строения комплексы протеолитических ферментов, расщепляющие различные внутриклеточные белки. Протеасомасодер 28 протомеров, собранных в стопку из 4 колец по 7 протомеров в каждом кольце, внутри стопки располагается полость где и происходит деструкция белков. Два внешних кольца формируется альфа-субъединицами, выполняющие регуляторную функции, а две внутренних вета-субъединицы которые обладают протеолитической активностью.Присутствует в ядрах, ЭПС, матриксе. Сходны у разных организмов.Протеасомы расщепляют белки до коротких пептидов, которые затем гидролизуются до отдельных аминокислот цитоплазматическими экзопептидазами. Механизм расщепления белков протеасомами связан с действием особого внутриклеточного белка-убиквитина. Этот белок способен с участием АТР и трех специал ферментов связываться с подлежащим расщеплению белков. Образующийся полиубиквитированный белок далее вовлекается в протеасому, где и деструктируется до коротких пептидов. 11. Типы матричного синтеза как центральный процесс в передаче, хранении и реализации наследственного материала. Матричная природа синтеза нуклеиновых кислот и белков обеспечивает высокую точность воспроизведения информации. Генетическая информация генотипа определяет фенотипические признаки клетки - генотип трансформируется в фенотип. Это направление потока информации включает три типа матричных синтезов: 1. синтез DNA — репликация 2. синтез RNA — транскрипция 3. синтез белка — трансляция 1)Репликация ДНК (ДНК → ДНК) точное удвоение (репликация) ДНК. Репликация осуществляется комплексом белков, которые расплетают хроматин, затем двойную спираль. После этого ДНК полимераза и ассоциированные с ней белки, строят на каждой из двух цепочек идентичную копию. Воспроизведение исходного генетического материала в поколениях. 2)Транскрипция (ДНК → РНК) биологический процесс, в результате которого информация, содержащаяся в участке ДНК, копируется на синтезируемую молекулу мРНК. Транскрипцию осуществляют факторы транскрипции и РНК-полимераза. 3)Трансляция (РНК → белок) Генетическая информация транслируется в форму полипептидных цепей. Комплексы факторов инициации и факторов элонгации доставляют аминоацилированные транспортные РНК к комплексу иРНК-рибосома. 4) В специальных случаях РНК может переписываться в форму ДНК (обратная транскрипция), а также копироваться в виде РНК (репликация), но белок никогда не может быть матрицей для нуклеиновых кислот. Репарация - это матричный синтез, исправляющий ошибки в структуре ДНК, вариант ограниченной репликации. Восстанавливает первоначальную структуру ДНК. Матрица – это участок неповреждённой нити ДНК.
|
Центральная догма молекулярной биологии - это поток информации от ДНК через РНК на белок: информация передаётся от нуклеиновых кислот к белку, но не в обратном направлении. Правило было сформулировано Френсисом Криком в 1958 году. Переход генетической информации от ДНК к РНК и от РНК к белку является универсальным для всех без исключения клеточных организмов, лежит в основе биосинтеза макромолекул. Репликации генома соответствует информационный переход ДНК → ДНК. В природе встречаются также переходы РНК → РНК и РНК → ДНК (например у некоторых вирусов). ДНК, РНК и белки относятся к линейным полимерам, то есть каждый входящий в их состав мономер соединяется максимум с двумя другими мономерами. Последовательность мономеров кодирует информацию, правила передачи которой описываются центральной догмой.
Общий — встречающиеся у большинства живых организмов; Специальный — встречающиеся в виде исключения, у вирусов и у мобильных элементов генома или в условиях биологического эксперимента; Неизвестные — не обнаружены. Репликация ДНК (ДНК → ДНК) точное удвоение (репликация) ДНК. Репликация осуществляется комплексом белков, которые расплетают хроматин, затем двойную спираль. После этого ДНК полимераза и ассоциированные с ней белки, строят на каждой из двух цепочек идентичную копию. Транскрипция (ДНК → РНК) биологический процесс, в результате которого информация, содержащаяся в участке ДНК, копируется на синтезируемую молекулу мРНК. Транскрипцию осуществляют факторы транскрипции и РНК-полимераза. Трансляция (РНК → белок) Зрелая иРНК считывается рибосомами в процессе трансляции.Комплексы факторов инициации и факторов элонгации доставляют аминоацилированные транспортные РНК к комплексу иРНК-рибосома. Обратная транскрипция (РНК → ДНК) перенос информации с РНК на ДНК, процесс, обратный нормальной транскрипции, осуществляемый ферментом обратной транскриптазой. Встречается у ретровирусов, например, ВИЧ. Репликация РНК (РНК → РНК) копирование цепи РНК на комплемлементарную ей цепь РНК с помощью фермента РНК-зависимой РНК-полимеразы. Вирусы, содержащие одноцепочечную (например, вирус ящура) или двуцепочечную РНК реплицируются подобным способом. Прямая трансляция белка на матрице ДНК (ДНК → белок) Прямая трансляция была продемонстрирована в клеточных экстрактах кишечной палочки, которые содержали рибосомы, но не иРНК. Такие экстракты синтезировали белки с введённых в систему ДНК, и антибиотик неомицин усиливал этот эффект.
|
|||||||||||||||
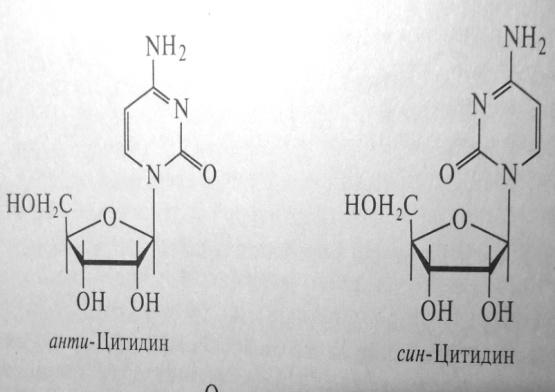
НУКЛЕОТИД - сложная химическая группа, встречающаяся в естественном состоянии. Нуклеотиды являются строительным материалом для НУКЛЕИНОВЫХ кислот (ДНК и РНК). Нуклеотиды построены из трех компонентов: пиримидинового или пуринового основания, пентозы и фосморной кислоты. Нуклеотиды связаны между собой в цепь фосфодиэфирной связью. Она образуется за счет этерификации ОН –группы С-3` пентозы одного нуклеотида и ОН-группы фосфатного остатка другого нуклеотида. В результате один из концов полинуклеотидной цепи заканчивается свободным фосфатом (Р-конец или 5`-конец). На другом коце имеется неэтерифицированная ОН-групппа у С-3`пентозы (3`-конец). В живых клетках встречаются также свободные нуклеотиды, представленные в виде различных коэнзимов, к которым относится АТФ. Все 5 гетероциклических оснований, входящие в входящие в состав нуклеиновых кислот, имеют плоскую конформацию, но это энергетически не выгодно. Поэтому в полинуклеотидах реализуется 2 конформации С3`- эндо и С2`-эндо. С1, 0 и С4 расположены в одной плоскости, С2 и С3 находятся в эндоконформациях, когда они выведены над этой плоскостью, т.е. в направлении связи С4-С5. Важнейшей хар-кой в определении конформации нуклеотидного звена является взаимное расположение углеводной и гетероциклической частей, которая определяется углом вращения вокруг N- гликозидной связи. Здесь существует 2 области разрешенных конформаций, син- и анти -.
|
13. Вторичная структура. Принцип комплементарности. ДНК. Принцип формирования конформаций - А, В, Z-формы ДНК. Триплексы. Палиндромы, формирование шпилек. Биологическое значение конформаций ДНК. ДНК представляет собой правозакрученную спираль , состоящую из двух полинуклеотидных цепей с антипараллельным ходом. Это означает, что 3`-концу соответствует 5`-конец другой цепи и наоборот. Остатки оснований направлены внутрь спирали. На один виток спирали приходится 10 оснований. В формировании вторичной структуры ДНК участвуют следующие типы взаимодействий: водородные связи между комплементарными основаниями (две между аденином и тимином, три — между гуанином и цитозином); стэкинг-взаимодействия; электростатические взаимодействия; Ван-дер-Ваальсовы взаимодействия. Принцип комплементарности ДНК - это строгое соответствие соединения азотистых оснований, соединёнными водородными связями, в котором: А-Т, Г-Ц. В зависимости от внешних условий параметры двойной спирали ДНК могут меняться, причём иногда существенно. Правоспиральные ДНК со случайной нуклеотидной последовательностью можно грубо разделить на два семейства — А и В, главное отличие между которыми — конформация дезоксирибозы. Z-формой -ДНК существуют в виде левой двойной спирали. Ход сахарофосфатного остова такой ДНК можно описать зигзагообразной линией, поэтому этот вид ДНК было решено назвать Z-формой. ДНК с определённой последовательностью нуклеотидов может переходить из обычной В-формы в Z. Необычность Z-формы ДНК проявляется в том, что повторяющейся структурной единицей являются две пары нуклеотидов, а не одна, как во всех других формах ДНК.
Для возникновения биспиральных структур в ДНК должны присутствовать «палиндромные», повторяющиеся последовательности. Палиндром представляет собой двуцепочечную последовательность ДНК, которая одинакого читается в обоих цепях, если каждую читать в соответствии с ее ориентацией. В качестве примера можно привести последовательность 5`GGT:ACC3` 3`CCA:TGG5` Осью симметрии является точка, относительно которой последовательность остается одинаковой при чтении в противоположных направлениях. Благодаря наличию собственной симметрии второго порядка палиндромы могут образовывать шпилечные структуры простой крестообразной формы. Такие последовательности способствуют специфическим нуклеиново-белковым взаимодействиям и учувствуют в процессах регуляции.
|
|||||||||||||||||||||||||||||
Ионные связи образуются между заряженными атомами. Энергия ионной связи определяется по формуле: Wион = - q1q2/4πε0εr, где q1q2 – заряды взаимодействующих ионов; ε0 = 8,85•10-12 Ф/м – электрическая постоянная; ε – относительная диэлектрическая проницаемость среды; r – расстояние между ионами. Ионные связи в макромолекулах обусловлены присутствием ионогенных групп: карбоксильных и аминогрупп в белках, фосфатных групп в нуклеиновых кислотах. В биомембранах ионогенными группами являются фосфаты, а также карбоксилы свободных жирных кислот. За счет ионных связей образуются комплексы различных ионов с макромолекулами. Например, многие белки связывают ионы кальция, а нуклеиновые кислоты еще и ионы магния. Водородные связи образуются между группами, содержащими атом водорода, и атомами кислорода, азота, фтора, хлора за счет электростатических и ван-дер-ваальсовых взаимодействий. Эти связи обусловлены способностью самого малого атомного ядра протона проникать в электронные оболочки соединяемых им электроотрицательных атомов и их стягивать. Водородная связь является направленной и образуется только в том случае, когда все три атома, участвующие в её образовании, лежат на одной прямой. Водородные связи играют важнейшую роль в поддержании определенной вторичной структуры не только белков, но и нуклеиновых кислот. Одновременное образование большого числа водородных (слабых) связей в макромолекулах лежит в основе явления комплементарности, то есть строго структурного соответствия и специфичности связывания больших участков молекул. Гидрофобные взаимодействия способствуют отталкиванию друг от друга неполярных незаряженных групп и молекул воды. Эти силы определяют формирование структуры биологических мембран и глобулярных белков. Стэкинг-взаимодействия - межмолекулярные взаимодействия, направленные вдоль спирали между соседними пространственно сближенными азотистыми основаниями. Таким образом, взаимодействия азотистых оснований между собой скрепляют двойную спираль молекулы ДНК и вдоль, и поперек ее оси. Сильное стэкинг-взаимодействие всегда усиливает водородные связи между основаниями, способствуя уплотнению спирали. При ослаблении стэкинг-взаимодействия молекулы воды, проникая внутрь спирали, конкурентно взаимодействуют с полярными группами оснований, инициируют дестабилизацию и способствуют дальнейшему распаду двойной спирали.
|
Рибонуклеи́новая кислота́ (РНК) — одна из трёх основных макромолекул (две другие — ДНК и белки), которые содержатся в клетках всех живых организмов. РНК состоит из длинной цепи, в которой каждое звено называется нуклеотидом. Каждый нуклеотид состоит из азотистого основания, сахара рибозы и фосфатной группы. Последовательность нуклеотидов позволяет РНК кодировать генетическую информацию. Все клеточные организмы используют РНК (мРНК) для программирования синтеза белков. Нуклеотиды РНК состоят из сахара — рибозы, к которой в положении 1' присоединено одно из оснований: аденин, гуанин, цитозин или урацил. Фосфатная группа соединяет рибозы в цепочку, образуя связи с 3' атомом углерода одной рибозы и в 5' положении другой. Фосфатные группы при физиологическом рН отрицательно заряжены. РНК транскрибируется как полимер четырёх оснований (аденина (A), гуанина (G), урацила (U) и цитозина (C), но в «зрелой» РНК есть много модифицированных оснований и сахаров. Структура. Азотистые основания в составе РНК могут образовывать водородные связи между нуклетидами. Однако возможны и другие взаимодействия, например, несколько аденинов могут образовывать петлю, или петля, состоящая из четырёх нуклеотидов, в которой есть пара оснований аденин — гуанин. Важная структурная особенность РНК, отличающая её от ДНК — наличие гидроксильной группы в 2' положении рибозы, которая позволяет молекуле РНК существовать в А, а не В-конформации, наиболее часто наблюдаемой у ДНК. Второе последствие наличия 2' гидроксильной группы состоит в том, что конформационно пластичные, то есть не принимающие участие в образовании двойной спирали, участки молекулы РНК могут химически атаковать другие фосфатные связи и их расщеплять. «Рабочая» форма одноцепочечной молекулы РНК, часто обладает третичной структурой, которая образуется на основе элементов вторичной структуры, образуемой с помощью водородных связей внутри одной молекулы. Различают несколько типов элементов вторичной структуры — стебель-петли, петли и псевдоузлы. Многие типы РНК, например, рРНК и мяРНК в клетке функционируют в виде комплексов с белками, которые ассоциируют с молекулами РНК после их синтеза или (у эукариот) экспорта из ядра в цитоплазму. Такие РНК-белковые комплексы называются рибонуклеопротеидами. Типы РНК: Матричная (информационная) РНК — РНК, которая служит посредником при передаче информации, закодированной в ДНК к рибосомам, молекулярным машинам, синтезирующим белки живого организма. Кодирующая последовательность мРНК определяет последовательность аминокислот полипептидной цепи белка. Транспортные (тРНК).Они переносят специфические аминокислоты в место синтеза пептидной связи в рибосоме. Каждая тРНК содержит участок для присоединения аминокислоты и антикодон для узнавания и присоединения к кодонам мРНК. Рибосомальные РНК (рРНК) — каталитическая составляющая рибосом. тмРНК - обнаружен во многих бактериях и пластидах. При остановке рибосомы на дефектных мРНК без стоп-кодонов тмРНК присоединяет небольшой пептид, направляющий белок на деградацию. Малые интерферирующие РНК (миРНК) часто образуются в результате расщепления вирусных РНК, но существуют и эндогенные клеточные миРНК. Малые ядерные РНК. Концепция «мир РНК». В живых организмах практически все процессы происходят в основном благодаря ферментам белковой природы. Белки, однако, не могут самореплицироваться и синтезируются в клетке de novo на основании информации, заложенной в ДНК. Но и удвоение ДНК происходит только благодаря участию белков и РНК. Образуется замкнутый круг, из-за которого, в рамках теории самозарождения жизни приходилось признать необходимость не только абиогенного синтеза обоих классов молекул, но и спонтанного возникновения сложной системы их взаимосвязи. В начале 1980-х годов в лаборатории Т. Чека и С. Олтмана в США была открыта каталитическая способность РНК. По аналогии с ферментами (англ. enzyme) РНК-катализаторы были названы рибозимами, за их открытие Томасу Чеку в 1989 году была присуждена Нобелевская премия по химии. Более того, оказалось, что активный центр рибосом содержит большое количество рРНК. Также РНК способны создавать двойную цепочку и самореплицироваться. Таким образом, РНК могли существовать полностью автономно, катализируя «метаболические» реакции, например, синтеза новых рибонуклеотидов и самовоспроизводясь, сохраняя из «поколения» в «поколение» каталитические свойства. Накопление случайных мутаций привело к появлению РНК, катализирующих синтез определённых белков, являющихся более эффективным катализатором, в связи с чем эти мутации закреплялись в ходе естественного отбора. С другой стороны возникли специализированные хранилища генетической информации — ДНК. РНК сохранилась между ними как посредник.
|
|||||||||||||||||||||||||||||