
- •Экзаменационный билет №28
- •2. В состав «Валокордина» входит фенобарбитал.
- •Ответ Фенобарбитал (Phenobarbitalum) Люминал (Luminalum)
- •3. Как должно быть организовано хранение полученного товара («Липы цветки», «Чистотела трава», «Тыквы семена») в условиях аптеки. Ответ обоснуйте.
- •5. Объясните явление катаболитной репрессии если происходит ферментационный процесс получения р-лактамных антибиотиков. Ответ
- •6. В условиях крупного фармацевтического производства:
2. В состав «Валокордина» входит фенобарбитал.
Для установления подлинности фенобарбитала используются реакции с катионами тяжелых металлов, а количественное определение проводится методом кислотно-основного титрования.
К какой группе лекарственных веществ по химическому строению и фармакологическому действию он относится?
В соответствии со строением и свойствами фенобарбитала объясните выбор условий при проведении анализа. Какие еще реакции и физико-химические константы можно предложить для оценки его качества?
Почему в фармакопейной статье регламентируется определение примеси фенилбарбитуровой кислоты?
Ответ Фенобарбитал (Phenobarbitalum) Люминал (Luminalum)

5-Этил-5-фенилбарбитуровая кислота
М.в. 232,24
Фенобарбитал относится к производным барбитуровой кислоты.
Описание: белый кристаллический порошок без запаха слабо горького вкуса.
Растворимость: очень мало растворим в холодной воде, трудно растворим в кипящей воде и хлороформе, легко растворим в 95% спирте и растворах щелочей, растворим в эфире.
Подлинность:
ИК-спектр в области 4000-400 см-1 должен совпадать со спектром стандарта.
УФ-спектр в области 220-280 нмимеет максимум и минимум поглощения при 240 и 224 нм соответственно (р-р в этаноле).
Тпл 174 – 178оС.
Реакция комплексообразования. Реакция основана на способности фенобарбитала образовывать комплексы с солями тяжелых металлов. Препарат растворяют в спирте, прибавляют каплю раствора хлорида кальция, раствор нитрата кобальта (II), раствора натрия гидроксида.
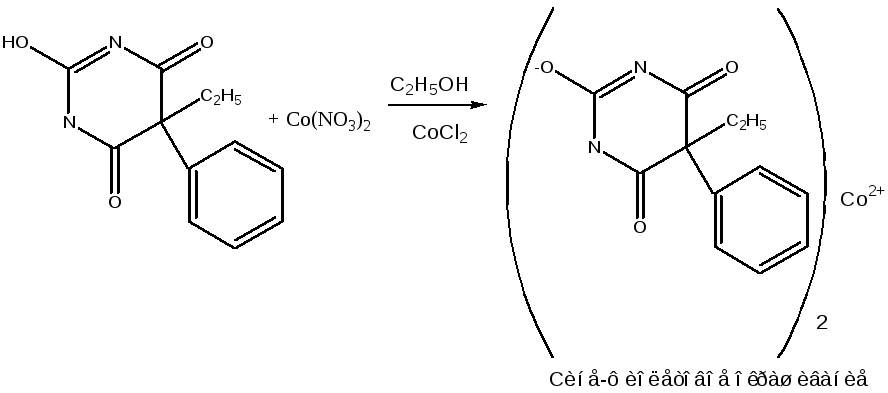
Реакция комплексообразования. К препарату прибавляют натрия гидроксид, калия карбонат и гидрокарбонат, раствор меди сульфата. Появляется бледно-сиреневое окрашивание, не изменяющееся при стоянии.

Не ГФХ. Реакция щелочного гидролиза. Барбитураты – внутренние амиды, и, значит, способны гидролизоваться за счет амидных групп. Гидролиз идет в жестких условиях – при сплавлении с кристаллическим NaOH. В результате чего выделяется аммиак, который обнаруживают по запаху и по посинению лакмусовой бумаги.

Если далее реакционную смесь подкислить соляной кислотой, выделяется углекислый газ в виде пузырьков и ощущается запах диалкилуксусной кислоты.

Реакция нитрования на фенильный радикал в пятом положении. Появляется желтое окрашивание, обусловленное образованием м-нитропроизводного.

Чистота:
Прозрачность и цветность.
Хлориды.
Сульфаты.
Фенилбарбитуровая кислота. Данная примесь проявляет более сильные кислотные свойства (К=4х10-5), чем фенобарбитал. Фенилбарбитуровую кислоту можно легко обнаружить потенциометрически по значению рН суспензии фенобарбитала с водой (5,0 – 6,0).
Органические примеси.
Сульфатная зола и тяжелые металлы.
Количественное определение:
Алкалиметрия. Метод основан на слабых основных свойствах фенобарбитала.
Растворитель – диметилформамид.
Индикатор – нейтрализованный по тимоловому синему в ДМФА.
Т – 0,1М натрия гидроксид.
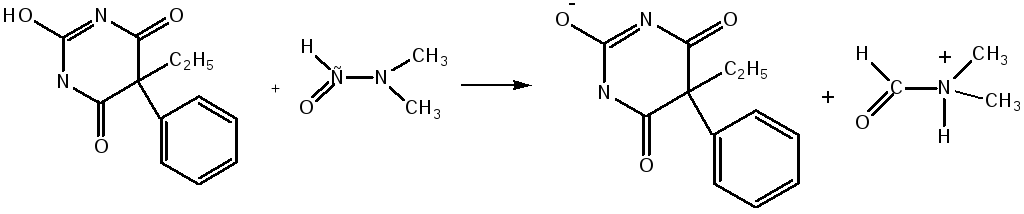
Другими методами количественного определения барбитуратов являются аргентометрия (в прямом и обратном вариантах) и гравиметрия.
Для количественного определения индивидуальных препаратов группы барбитуратов и особенно для их лекарственных форм применяют физико-химические методы анализа (ВЭЖХ, спектрофотметрия)
Хранение: список Б, в хорошо укупоренной таре.
Применение: снотворное, противосудорожное.
