- •А.В. Колобов, в.В. Плахтинский, в.В. Соснина пособие для решения задач по органической хими
- •Список сокращений и обозначений
- •Введение
- •1 Пример решения расчётно-графического задания по теме «Алканы»
- •Способы получения и химические свойства алкенов
- •2 Пример решения расчётно-графического задания по теме «Алкены»
- •Способы получения и химические свойства сопряженных диенов
- •Способы получения и химические свойства алкинов
- •3 Пример решения расчётно-графического задания по теме «Диены. Алкины»
- •Химические свойства бензола и его производных
- •4 Пример решения расчётно-графического задания по теме «Арены»
- •5 Пример решения расчётно-графического задания по теме «Галогеналканы. Галогенарены»
- •Литература
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
Химические свойства бензола и его производных

4 Пример решения расчётно-графического задания по теме «Арены»
Задача 4.1
Рассмотрите механизм реакции алкилирования изопропилбензола пропилбромидом в присутствии хлористого алюминия. Приведите энергетическую диаграмму процесса, укажите медленную стадию, рассмотрите строение -комплекса. Напишите реакцию образования электрофила.
|
Решение 4.1: |
Напоминание: |
|
Механизм:
Энергетическая диаграмма:
Е – энергия; КР – координата реакции; ПС1-ПС3 – переходные состояния. Медленная стадия – образование -К. |
Образование электрофила – карбокатиона – происходит при взаимодействии пропилбромида с хлористым алюминием с образованием комплекса КК1. Он перегруппировывается в более устойчивый вторичный карбокатион в составе КК2 [2, c. 155]. Взаимодействие КК2 с изопропилбензолом приводит к -комплексу -К, который превращается в -комплекс-К. [2, c. 147]. Группа СН(СН3)2 – ориентант I рода и направляет электрофил в орто- и пара-положения [2, c. 155]. . |
|
Решение 4.1 (продолжение): |
Напоминание: |
|
Строение -К:
В данном случае образуется только п--К ввиду стерических препятствий для орто-положения. |
-Комплекс – это карбокатион, положительный заряд которого делокализован в орто- и пара-положениях; строение -К можно представить набором резонансных структур [2, сc. 148, 155]. |
Задача 4.2
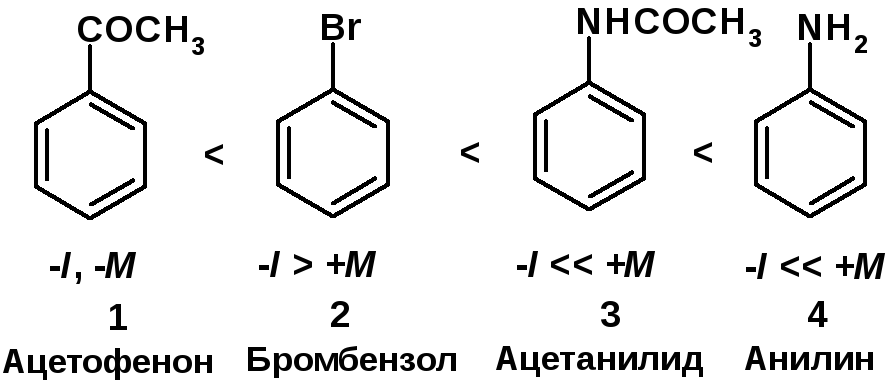
Расположите соединения в порядке увеличения реакционной способности субстраты в реакции бромирования (механизм SEAr):

Укажите электронные эффекты ориентантов. Напишите уравнения реакций.
|
Решение 4.2: |
Напоминание: |
|
Увеличение реакционной способности, электронные эффекты:
|
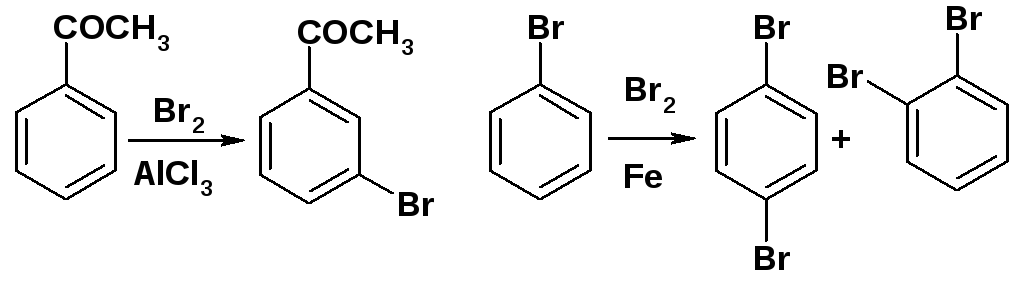
СОСН3 – мета-ориен-тант (II рода), скорость реакции меньше, чем для бензола, требуется катализатор. Br – орто-, пара-ориентант (I рода) скорость реакции меньше, чем для бензола [2, c. 180]. |
|
Решение 4.2 (продолжение): |
Напоминание: |
|
1 - Скорость реакции меньше, чем для бензола. 2 - Скорость реакции меньше, чем для бензола
3 - Скорость реакции больше, чем для бензола, но меньше, чем для анилина - группа СOCH3 снижает электронную плотность на N-атоме. 4 - Скорость реакции много больше, чем для бензола, бромирование протекает в 2-, 4- и 6-положения даже при эквимолекулярном количестве Br2 |
NHCOCH3 - пара-ориентант (I рода) [2, c. 180].
NH2 – орто-, пара-ориентант (I рода) [2, c. 180]. |
Задача 4.3
Рассмотрите механизм ориентирующего влияния цианогруппы CN в реакции нитрования бензонитрила (механизм SEAr).
|
Решение 4.3: |
Напоминание: |
|
|
СN-группа обладает –I и –М-эф-фектами [2, c. 180]. |
|
Решение 4.3 (продолжение): |
Напоминание: |
|
Возможно образование альтернативных -комп-лексов в о-, м- и п-положениях (о-, м- и п--К). о- и п--К будут крайне нестабильны из-за –М-эффекта CN-группы. В м-положении проявляется только ее –I-эффект, и м--К будет менее нестабилен. Скорость реакции меньше, чем для бензола, CN-группа будет выступать как мета-ориентант (II рода). |
Лимитирующей стадией процесса является образование -комплек-са при перегруппировке -комп-лекса [2, c. 147] |
Задача 4.4
Рассмотрите механизм ориентирующего влияния метоксигруппы OCH3 в реакции бромирования анизола (механизм SEAr).
|
Решение 4.4: |
Напоминание: |
|
Скорость реакции больше, чем для бензола, ОСН3-группа будет выступать как пара-ориентант (I рода). |
Метоксигруппа обладает –I и +М-эффектами, причем по силе эффекта -I << +М [2, c. 181]. Лимитирующей стадией процесса является образование -комплекса при перегруппировке -комп-лекса [2, сc. 147, 175]. Экспериментально установлено, что анизол бромируется в основном в п-положение |
|
Решение 4.4 (продолжение): |
Напоминание: |
|
Стабилизация п--К может объясняться возможностью образования резонансной структуры:
|
|
Задача 4.5
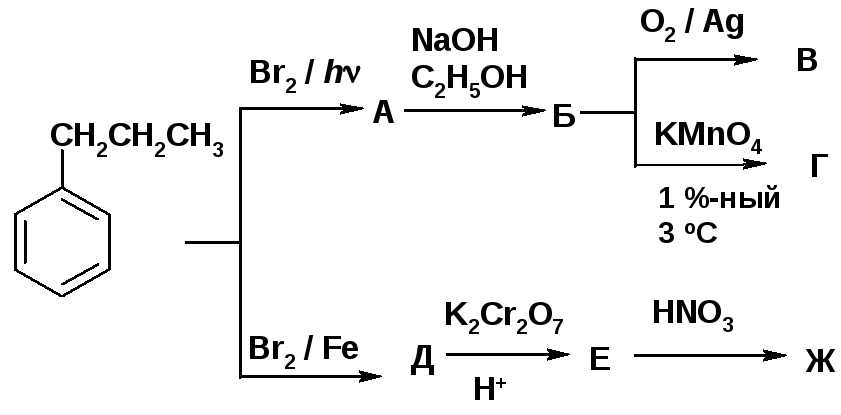
Рассмотрите совместное влияние двух групп на изомерный состав продуктов в следующих реакциях:
Напишите уравнения реакций, дайте названия исходным соединениям и продуктам.
Указание
Ориентирующее влияние каждого заместителя определяют отдельно. Если оба заместителя направляют вводимую группу в одно и то же положение, то это согласованная ориентация.
|
Решение 4.5: |
Напоминание: |
|
Согласованная ориентация – 1 изомер. |
Группа NHCOCH3 обладает –I и +М-эффектами, причем -I << +М: орто-, пара-ори-ентант. Группа СN обладает –I и -М-эффектами: мета-ориентант [2, c. 180]. |
|
Решение 4.5 (продолжение): |
Напоминание: |
|
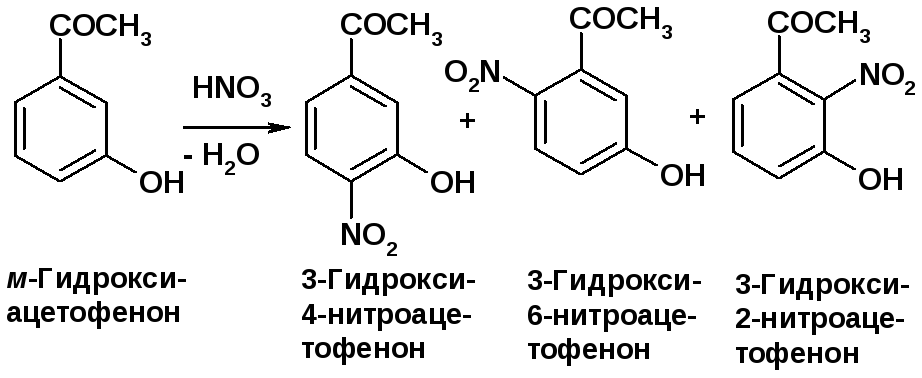
Реакция 2:
Несогласованная ориентация – 3 изомера. Гидроксигруппа за счет +М-эффекта оказывает определяющее влияние на стабильность -комплексов, поэтому в основном получаются указанные изомеры. |
Группа OH обладает –I и +М-эффектами, причем -I << +М. орто-, пара-ори-ентант [2, c 180.]. Группа COCH3 обладает –I и -М-эффектами: мета-ориентант [2, c. 180]. |
Задача 4.6
Из бензола и любых реагентов, кроме ароматических соединений, получите м-пропиланилин.
|
Решение 4.6: |
Напоминание: |
|
Схема синтеза:
|
Алкилбензолы с н-алкильной группой нельзя получить реакцией алкилирования. Надо ацилировать бензол и восстановить карбонильную группу в кетоне [2, c. 162]. Аминогруппу можно ввести в ядро реакцией нитрования с последующим восстановлением нитрогруппы. |
Задача 4.7
Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:
|
Решение 4.7: |
Напоминание: |
|
|
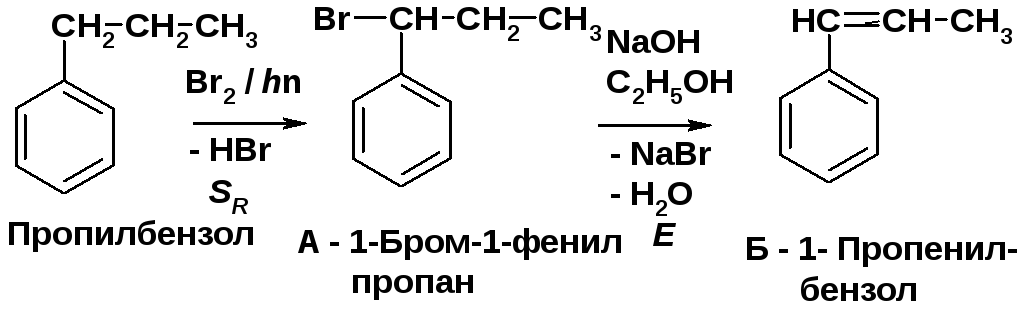
Алкилбензолы взаимодействуют с бромом при УФ облучении с образованием -бром-производных – SR-реакция [2, c. 163]. Бромалканы при действии спиртового раствора отщепляют HBr – E-реакция [2, c. 223]. |
Задача 4.8
Напишите уравнения реакций, назовите все соединения, укажите механизмы реакций:

|
Решение 4.8: |
Напоминание: |
|
|
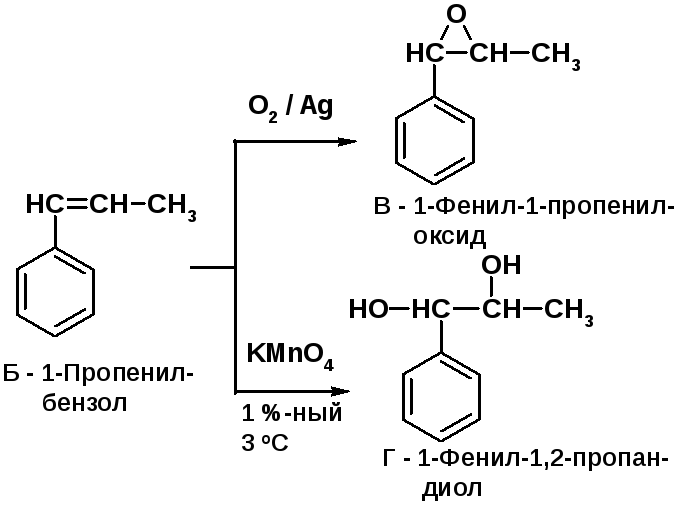
Алкены реагируют с бромом в инертном раст-ворителе по механизму АЕ [2, c. 75]. Br2 в присутствии Fe реагирует по механизму SEAr. Алкены окисляются разбавленным раствором KMnO4 до 1,2-диолов, а концентрированным – до карбоновых кислот [2, c. 34]. При реакции алкенов с надкислотами образуются эпоксиды [2, c. 34]. |
|
Решение 4.8 (продолжение): |
Напоминание: |
|
|
Алкилирование протекает в о-положение к атому хлора из-за стерических препятствий циклопентильной группы. Алкилбензолы взаимодействуют с бромом при УФ облучении с образованием -бром-производных – SR-реакция [2, c. 163]. Озон действует на ароматическое ядро так же, как на другие углеводороды с двойными связями: получа-ются озониды, гидролизующиеся до карбонилсодержаших соединений [2, c. 100]. |
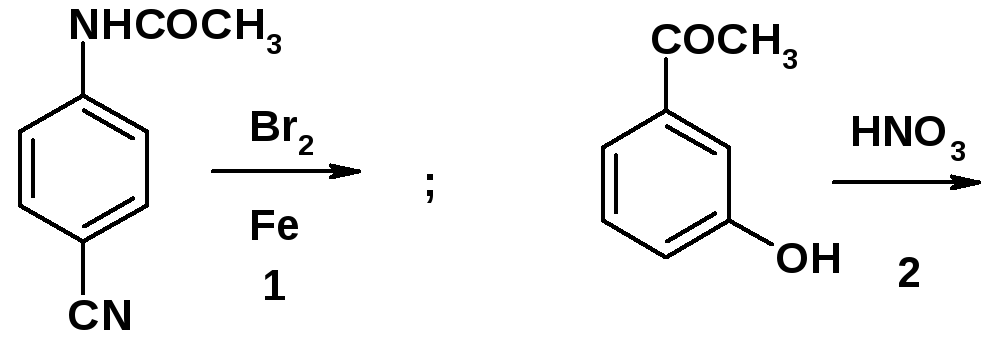
Задача 4.9
Напишите уравнения реакций, укажите механизмы:

|
Решение 4.9: |
Напоминание: |
|
|
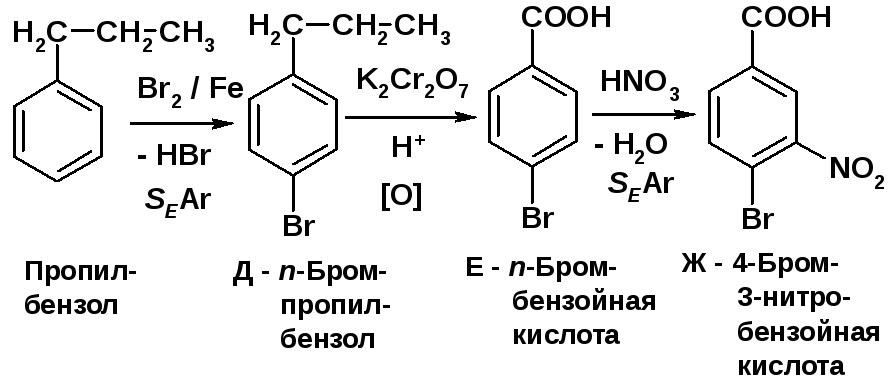
NHCOCH3-группа направляет электрофил в положение 4; NO2-группа - в положение 5 незамещенного кольца [2, c. 187]. Галогенирование протекает в положение 1 [2, c. 186]. При окислении в присутствии V2O5 образуется фталевый ангидрид [2, c. 189]. |
Задача 4.10
Напишите уравнения реакций:
![]()
|
Решение 4.10: |
Напоминание: |
|
|
Бромирование идет в 2- и 5-положения [2, c. 196]. В 2,5-дибромтиофене нитрогруппа вступает в положение 3. |
Задача 4.11
Напишите уравнения реакций, укажите механизмы:
![]()
|
Решение 4.10: |
Напоминание: |
|
|
Атака нуклеофила протекает в положение 2 пиридина [2, c. 200]. Пиридин сульфируется при 350 ºС в положение 3 [2, c. 199]. |
Задача 4.12
Пиридин подвергните взаимодействию с фениллитием, полученный продукт пронитруйте. Укажите механизмы реакций.
|
Решение 4.12: |
Напоминание: |
|
|
SNAr-реакция в пиридине с участием фениллития идет в положение 2 [2, c. 200]. |
|
Решение 4.12 (продолжение): |
Напоминание: |
|
Пиридин мало реакционноспособен в реакциях SЕAr. Нитрованию подвергается бензольное кольцо в м-положение, поскольку N-атом пиридинового кольца выступает как электроноакцепторная группа. |
|
Вопросы и упражнения
4.1. Галогенирование бензола соединением ICl приводит к образованию йодбензола. Рассмотрите механизм реакции, приведите энергетическую диаграмму процесса, укажите медленную стадию, рассмотрите строение -комплекса [1, c. 72].
4.2. Расположите соединения в порядке увеличения реакционной способности в реакции бромирования (механизм SEAr): бензол, нитробензол, бромбензол, толуол. Укажите электронные эффекты заместителей. Напишите уравнения реакций [1, c. 74].
4.3. Рассмотрите совместное влияние двух групп на изомерный состав продуктов в следующих реакциях:

Напишите уравнения реакций, дайте названия исходным соединениям и продуктам [1, c. 83].
4.4. Напишите структурные формулы и назовите соединения, образующиеся в реакциях (если они протекают) бутилбензола со следующими реагентами:
а) разбавленный холодный раствор перманганата калия;
б) горячий концентрированный раствор перманганата калия;
в) хлористый ацетил (AlCl3), а затем Zn(Hg), HCl;
г) Cl2 (Fe), а затем Cl2 при облучении и нагревании;
д) O3, а затем H2O (Zn).
Типичные вопросы, обсуждаемые при защите расчётно-графической работы:
4.5. Какими классами соединений можно алкилировать ароматические соединения?
4.6. Приведите примеры сильных, умеренно сильных и слабых электрофилов.
4.7. Лимитирующая стадия реакции электрофильного ароматического замещения.
4.6. Почему для получения алкилбензолов часто используется схема, включающая не алкилирование, а ацилирование.
4.7. Что такое защитная группа. Сульфирование как способ защиты п-положения.
4.8. Почему алкилбензолы могут галогенироваться в зависимости от условий как в ароматическое кольцо, ток и в боковую цепь?
4.9. В случае несогласованной ориентации какая из групп оказывает наибольшее влияние на образование доминирующего продукта (активирующая или дезактивирующая)?
4.10. Какими классами соединений можно ацилировать арены? Какой класс соединений получается в результате реакции ацилирования?
4.11. Что такое перегруппировка Фриса?
4.12. Промышленный способ получения фенола (кумольный метод).
4.13. Почему для ароматических соединений не характерны реакции присоединения?






 Возможно
образование альтернативных -комплексов
в м-
и п-положениях
(м-
и п--К).
п--К
будет стабилен из-за проявления
–М-эффекта
ОCН3-группы.
В м-положении
проявляется только ее –I-эффект,
поэтому м--К
будет менее стабилен.
Возможно
образование альтернативных -комплексов
в м-
и п-положениях
(м-
и п--К).
п--К
будет стабилен из-за проявления
–М-эффекта
ОCН3-группы.
В м-положении
проявляется только ее –I-эффект,
поэтому м--К
будет менее стабилен.