
- •И.С. Колпащикова, а.Ф. Бетнев, е.М. Алов функциональные производные углеводородов
- •Удк 547
- •Удк 547
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
- •1. Спирты
- •1.1. Физические свойства
- •Сравнение физических свойств спиртов и углеводородов
- •1.2. Химические свойства
- •1.2.1. Реакции с участием связи o−h
- •1.2.2. Реакция с участием связи r–oh
- •1.2.3. Окисление, дегидрирование
- •1.3. Способы получения
- •1.3.1. Гидратация алкенов
- •1.3.2. Гидролиз галогеналканов
- •1.3.3. Синтез с помощью реактива Гриньяра
- •1.3.4. Гидроборирование-окисление алкенов
- •1.3.5. Восстановление карбонильных соединений
- •1.3.6. Брожение сахаров
- •2. Фенолы
- •2.1. Физические свойства
- •Физические свойства фенолов
- •2.2. Химические свойства
- •2.2.1. Кислотность
- •2.2.2. Фенолы и феноксид-ионы – нуклеофильные реагенты
- •2.2.3. Электрофильное замещение в ядре
- •2.2.4. Замещение гидроксигруппы в нитрофенолах
- •2.2.5. Окисление
- •2.2.6. Восстановление
- •3.3. Способы получения
- •4.1. Химические свойства
- •4.2. Способы получения
- •4.2.1. Превращение галогенгидринов под действием оснований
- •4.2.2. Окисление алкенов гидропероксидами (реакция Прилежаева)
- •5. Карбонильные соединения
- •5.1. Строение и физические свойства
- •5.2. Химические свойства
- •5.2.1. Нуклеофильное присоединение синильной кислоты, бисульфита натрия, реактива Гриньяра, ацетиленидов
- •5.2.2. Нуклеофильное присоединение - отщепление g–nh2 и спиртов
- •5.2.3. Нуклеофильное присоединение, нуклеофил – карбанион. Альдольная конденсация
- •Реакции, родственные альдольной конденсации
- •5.2.4. Нуклеофильное присоединение – реакция окисления-восстановления
- •5.2.5. Галогенирование кетонов - реакции с участием карбанионов
- •5.2.6. Взаимодействие альдегидов и кетонов с пентахлоридом фосфора
- •5.2.7. Восстановление
- •5.2.8. Окисление
- •5.3. Способы получения
- •Названия ацилов и ацилатов некоторых карбоновых кислот
- •6.1. Строение и физические свойства
- •6.2. Химические свойства
- •6.2.1. Реакции карбоновых кислот, сопровождающиеся разрывом о–н-связи. Кислотность
- •6.2.2. Реакции, сопровождающиеся разрывом связи с-он. Превращение в функциональные производные
- •6.2.3. Реакции замещения у -углеродного атома.
- •6.2.4. Восстановление кислот
- •7.1.2. Реакции замещения группы х у карбонильного атома углерода
- •7.1.3. Реакции сложного эфира по -углеродному атому
- •7.1.4. Восстановление производных кислот
- •8. Жиры. Воски
- •9. СульфОновые кислоты
- •9.1. Химические свойства
- •9.1.1. Кислотность. Образование солей
- •9.1.2. Превращение в производные кислот
- •Константы кислотности бензолсульфоновой и бензойной кислот и их амидов
- •9.1.3. Реакция замещения сульфогруппы
- •9.1.4. Электрофильное замещение в кольце – seAr
- •9.2. Способы получения
- •10. Дикарбоновые кислоты
- •10.1. Кислотные свойства
- •Физические свойства дикарбоновых кислот
- •10.2. Поведение при нагревании
- •10.3. Способы получения
- •11. Нитросоединения
- •11.1. Строение и физические свойства
- •Некоторые физические свойства нитрометана и ацетона
- •11.2. Химические свойства
- •11.3. Способы получения
- •12.2. Химические свойства
- •12.2.1. Основность
- •12.2.2. Реакции с участием аминогруппы
- •12.2.3. Замещение в кольце ароматических аминов
- •12.2.4. Реакции аминов с азотистой кислотой
- •12.3. Способы получения
- •12.3.1. Восстановление азотсодержащих соединений:
- •12.3.2. Взаимодействие галогенпроизводных с аммиаком или аминами
- •12.3.3. Взаимодействие спиртов с аммиаком или аминами
- •12.3.4. Восстановительное аминирование
- •12.3.5. Расщепление амидов по Гофману
- •13. Диазосоединения. Соли диазония
- •13.1. Свойства солей диазония
- •1. Синтез п-нитроанилинового красного.
- •2. Синтез метилоранжа
- •14. Кетокислоты
- •Физические свойства некоторых кетокислот
- •15. Оксикислоты
- •Физические свойства некоторых оксикислот
- •16. ,-Непредельные карбонильные соединения
- •17. Аминокислоты
- •17.1. Кофигурация аминокислот
- •17.2. Кислотно-основные свойства
- •Аминокислоты
- •17.3. Способы получения
- •О г л а в л е н и е
- •И.С. Колпащикова, а.Ф. Бетнев, е.М. Алов функциональные производные углеводородов
1.3.5. Восстановление карбонильных соединений
Альдегиды восстанавливаются в первичные спирты, кетоны – во вторичные водородом в присутствии катализатора (Ni), при этом восстанавливается и двойная углерод-углеродная связь, или с помощью алюмогидрида лития LiAlH4, не затрагивая двойные углерод-углеродные связи.
![]()

Получение первичных спиртов восстановлением карбоновых кислот предпочтительно в том случае, когда кислоты более доступны, чем спирты.

Первичные спирты также могут быть получены восстановлением эфира, при этом оба фрагмента эфира превращаются в спирты.

Гидрированием окиси углерода в различных условиях можно получить как чистый метиловый спирт, так и смесь его первичных гомологов.
![]()
1.3.6. Брожение сахаров
Дрожжи сбраживают некоторые виды сахаров. Это сложный каталитический многостадийный распад на спирт и диоксид углерода.
![]()
Способы получения и химические свойства спиртов приведены на рис. 1.
2. Фенолы
Фенолами называются соединения, в которых гидроксильная группа связана непосредственно с ароматическим ядром. Как и в случае спиртов, число ОН-групп определяет атомность фенолов. По числу гидроксильных групп в молекуле различают одно-, двух-, трех- и многоатомные фенолы:
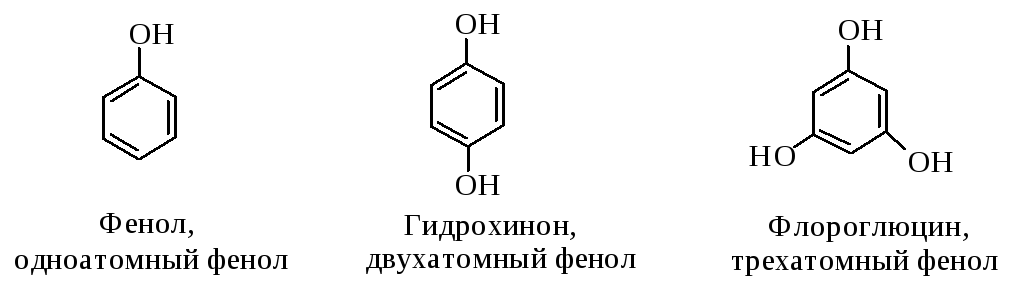
Следует выделить особенности строения и свойства фенолов, в которых проявляются, с одной стороны, сходство со свойствами спиртов, а с другой - влияние ароматического кольца на реакционную способность гидроксильной группы и влияние гидроксильной группы на реакционную способность кольца.
2.1. Физические свойства
Простейшие фенолы – высококипящие жидкости или низкоплавкие твердые соединения. Они имеют высокие температуры кипения из-за обра-
зования
водородных связей
 .
Более высокая температура
кипения фенола (182 °С) по сравнению с
температурой кипения циклогексанола
(161 °С) также связана с тем, что в феноле
прочнее водородные связи.
.
Более высокая температура
кипения фенола (182 °С) по сравнению с
температурой кипения циклогексанола
(161 °С) также связана с тем, что в феноле
прочнее водородные связи.
Фенол
заметно растворим в воде, это объясняется
образованием водородных
связей с водой
 .
Растворимость гомологов фенола
ниже, двух- и трехатомных фенолов –
выше.
.
Растворимость гомологов фенола
ниже, двух- и трехатомных фенолов –
выше.
Фенолы - бесцветные вещества (за исключением нитрофенолов, имеющих желтый цвет), однако обычно окрашены за счет примесей продуктов их окисления кислородом воздуха. Физические свойства некоторых фенолов представлены в табл. 2.
Высокая температура кипения п-нитрофенола обусловлена наличием межмолекулярных водородных связей. Из-за межмолекулярных связей м- и п-нитрофенолы образуют ассоциаты, и поэтому их нельзя перегнать с водяным паром.
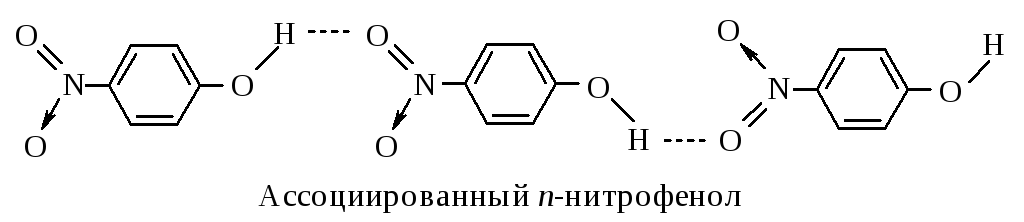
У о-нитрофенола образуется в большей степени внутримолекулярная водородная связь, поэтому он не обладает свойствами ассоциированных жидкостей.

Внутримолекулярная водородная связь образуется всегда, когда это позволяет структура соединения.
Таблица 2
Физические свойства фенолов
|
Название |
Т пл., оС |
Т кип., оС |
Растворимость в 100 мл воды при 25 °С, г
|
Ка∙1010 |
|
Фенол |
43 |
182 |
9,3 |
1,1 |
|
п-Крезол |
35,5 |
201 |
2,3 |
0,07 |
|
п-Фторфенол |
48 |
185 |
- |
5,2 |
|
п-Хлорфенол |
43 |
220 |
2,7 |
6,3 |
|
п-Бромфенол |
33 |
236 |
- |
14 |
|
п-Аминофенол |
186 |
- |
- |
- |
|
о-Нитрофенол |
45 |
217 |
0,2 летуч с водяным паром |
600 |
|
м-Нитрофенол |
96 |
194 |
1,35 нелетуч с водяным паром |
600 |
|
п-Нитрофенол |
114 |
279 разл. |
1,69 нелетуч с водяным паром |
600 |
|
Пирокатехин |
104 |
246 |
46 |
1 |
|
Резорцин |
110 |
281 |
123 |
3 |
|
Гидрохинон |
173 |
286 |
- |
2 |
