- •И.С. Колпащикова, а.Ф. Бетнев, е.М. Алов функциональные производные углеводородов
- •Удк 547
- •Удк 547
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
- •1. Спирты
- •1.1. Физические свойства
- •Сравнение физических свойств спиртов и углеводородов
- •1.2. Химические свойства
- •1.2.1. Реакции с участием связи o−h
- •1.2.2. Реакция с участием связи r–oh
- •1.2.3. Окисление, дегидрирование
- •1.3. Способы получения
- •1.3.1. Гидратация алкенов
- •1.3.2. Гидролиз галогеналканов
- •1.3.3. Синтез с помощью реактива Гриньяра
- •1.3.4. Гидроборирование-окисление алкенов
- •1.3.5. Восстановление карбонильных соединений
- •1.3.6. Брожение сахаров
- •2. Фенолы
- •2.1. Физические свойства
- •Физические свойства фенолов
- •2.2. Химические свойства
- •2.2.1. Кислотность
- •2.2.2. Фенолы и феноксид-ионы – нуклеофильные реагенты
- •2.2.3. Электрофильное замещение в ядре
- •2.2.4. Замещение гидроксигруппы в нитрофенолах
- •2.2.5. Окисление
- •2.2.6. Восстановление
- •3.3. Способы получения
- •4.1. Химические свойства
- •4.2. Способы получения
- •4.2.1. Превращение галогенгидринов под действием оснований
- •4.2.2. Окисление алкенов гидропероксидами (реакция Прилежаева)
- •5. Карбонильные соединения
- •5.1. Строение и физические свойства
- •5.2. Химические свойства
- •5.2.1. Нуклеофильное присоединение синильной кислоты, бисульфита натрия, реактива Гриньяра, ацетиленидов
- •5.2.2. Нуклеофильное присоединение - отщепление g–nh2 и спиртов
- •5.2.3. Нуклеофильное присоединение, нуклеофил – карбанион. Альдольная конденсация
- •Реакции, родственные альдольной конденсации
- •5.2.4. Нуклеофильное присоединение – реакция окисления-восстановления
- •5.2.5. Галогенирование кетонов - реакции с участием карбанионов
- •5.2.6. Взаимодействие альдегидов и кетонов с пентахлоридом фосфора
- •5.2.7. Восстановление
- •5.2.8. Окисление
- •5.3. Способы получения
- •Названия ацилов и ацилатов некоторых карбоновых кислот
- •6.1. Строение и физические свойства
- •6.2. Химические свойства
- •6.2.1. Реакции карбоновых кислот, сопровождающиеся разрывом о–н-связи. Кислотность
- •6.2.2. Реакции, сопровождающиеся разрывом связи с-он. Превращение в функциональные производные
- •6.2.3. Реакции замещения у -углеродного атома.
- •6.2.4. Восстановление кислот
- •7.1.2. Реакции замещения группы х у карбонильного атома углерода
- •7.1.3. Реакции сложного эфира по -углеродному атому
- •7.1.4. Восстановление производных кислот
- •8. Жиры. Воски
- •9. СульфОновые кислоты
- •9.1. Химические свойства
- •9.1.1. Кислотность. Образование солей
- •9.1.2. Превращение в производные кислот
- •Константы кислотности бензолсульфоновой и бензойной кислот и их амидов
- •9.1.3. Реакция замещения сульфогруппы
- •9.1.4. Электрофильное замещение в кольце – seAr
- •9.2. Способы получения
- •10. Дикарбоновые кислоты
- •10.1. Кислотные свойства
- •Физические свойства дикарбоновых кислот
- •10.2. Поведение при нагревании
- •10.3. Способы получения
- •11. Нитросоединения
- •11.1. Строение и физические свойства
- •Некоторые физические свойства нитрометана и ацетона
- •11.2. Химические свойства
- •11.3. Способы получения
- •12.2. Химические свойства
- •12.2.1. Основность
- •12.2.2. Реакции с участием аминогруппы
- •12.2.3. Замещение в кольце ароматических аминов
- •12.2.4. Реакции аминов с азотистой кислотой
- •12.3. Способы получения
- •12.3.1. Восстановление азотсодержащих соединений:
- •12.3.2. Взаимодействие галогенпроизводных с аммиаком или аминами
- •12.3.3. Взаимодействие спиртов с аммиаком или аминами
- •12.3.4. Восстановительное аминирование
- •12.3.5. Расщепление амидов по Гофману
- •13. Диазосоединения. Соли диазония
- •13.1. Свойства солей диазония
- •1. Синтез п-нитроанилинового красного.
- •2. Синтез метилоранжа
- •14. Кетокислоты
- •Физические свойства некоторых кетокислот
- •15. Оксикислоты
- •Физические свойства некоторых оксикислот
- •16. ,-Непредельные карбонильные соединения
- •17. Аминокислоты
- •17.1. Кофигурация аминокислот
- •17.2. Кислотно-основные свойства
- •Аминокислоты
- •17.3. Способы получения
- •О г л а в л е н и е
- •И.С. Колпащикова, а.Ф. Бетнев, е.М. Алов функциональные производные углеводородов
9. СульфОновые кислоты
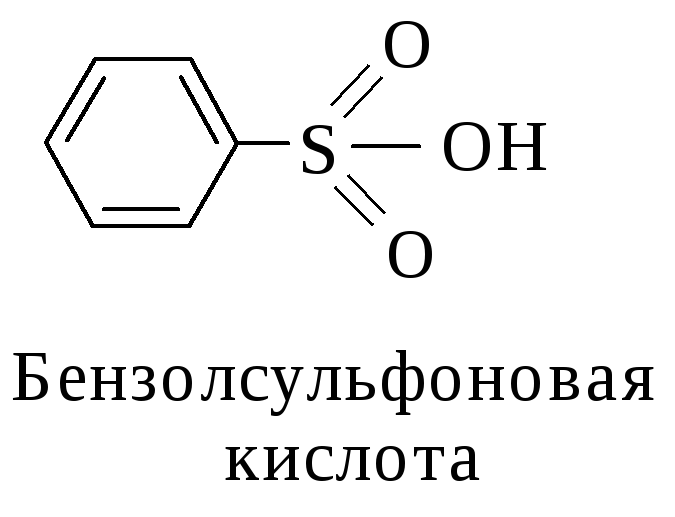
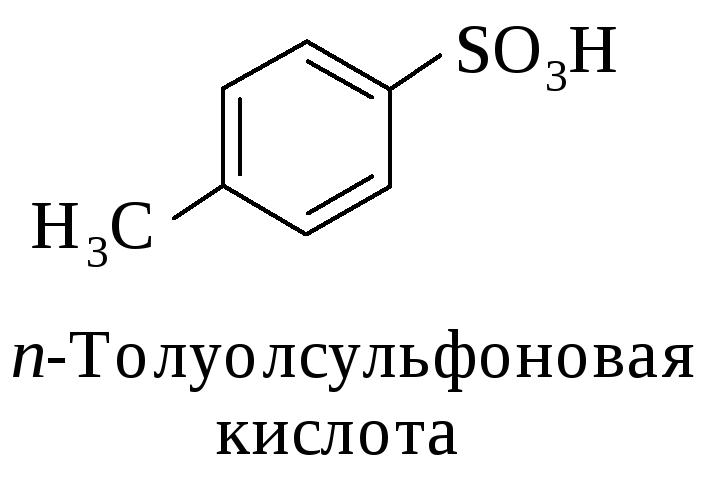
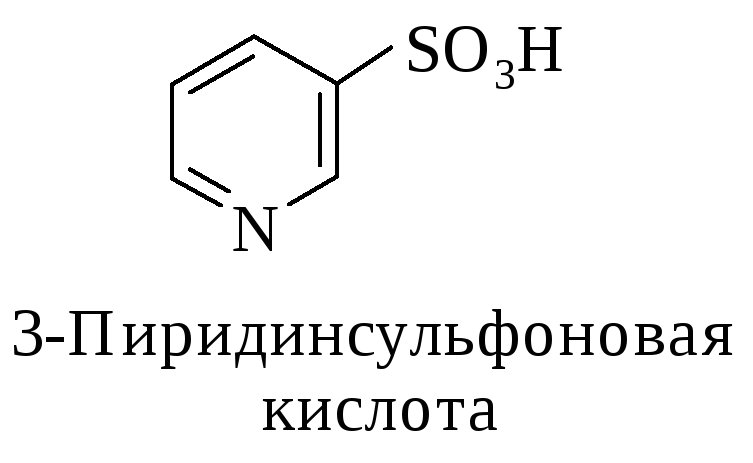
Сульфоновые кислоты (сульфокислоты) содержат функциональную группу – SO2OH.
Сульфоновые кислоты классифицируют в зависимости от природы углеводородного радикала (ароматические, гетероциклические и алкансульфокислоты) и количества сульфогрупп.
|
|
|
| |
|
|
| ||
Сульфоновые кислоты представляют собой сильно полярные соединения. Они лучше растворимы в воде, чем органические соединения других классов. Сульфогруппу –SO3H часто вводят в соединения, чтобы сделать их более растворимыми в воде.
Сульфоновые кислоты мало летучи и разлагаются ниже температуры кипения. Они обычно вязки, и их трудно очищать. Поэтому сульфоновые кислоты удобно выделять и использовать в виде солей.
9.1. Химические свойства
9.1.1. Кислотность. Образование солей
Cульфоновые кислоты полностью ионизированы в водных растворах.
ArSO2OH → ArSO2O+ H
Повышенная кислотность сульфоновых кислот вызвана тем, что отрицательный заряд в сульфонат-ионе распределен между тремя атомами кислорода.
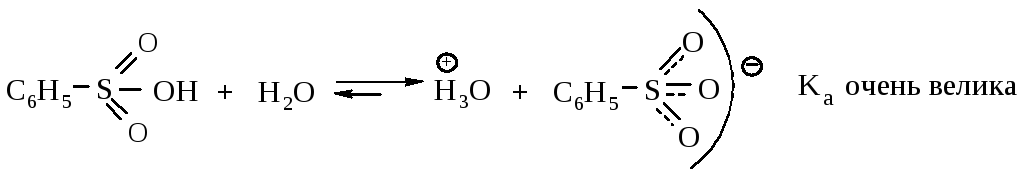
Соли легко образуются при обработке сульфоновых кислот основаниями.
![]()
9.1.2. Превращение в производные кислот
Хлорангидриды сульфоновых кислот (сульфонилхлориды) получают действием пятихлористого фосфора или тионилхлорида на сульфоновые кислоты.
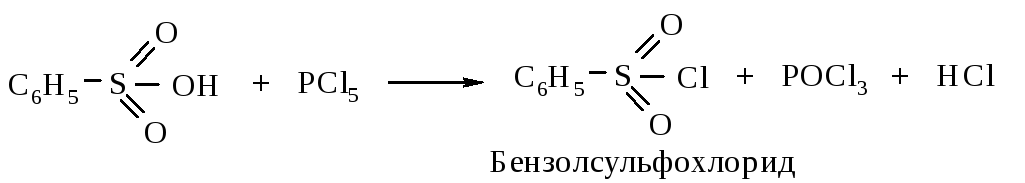
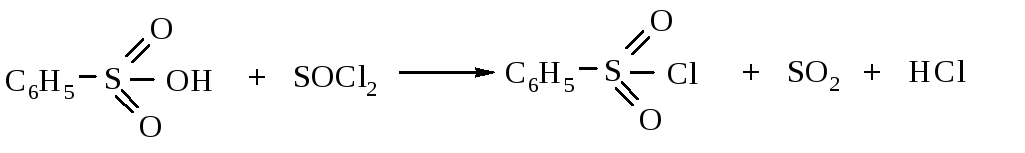
Иногда получают сульфохлориды, действуя на бензол избытком хлорсульфоновой кислоты.
![]()
Сульфохлориды – важные промежуточные продукты в синтезе эфиров, амидов, поскольку их нельзя получить непосредственно из сульфоновых кислот. В этих реакциях сульфохлориды менее активны, чем хлорангидриды ароматических карбоновых кислот.
Сульфохлориды реагируют со спиртами и фенолами в присутствии основания с образованием сложных эфиров (сульфонатов).
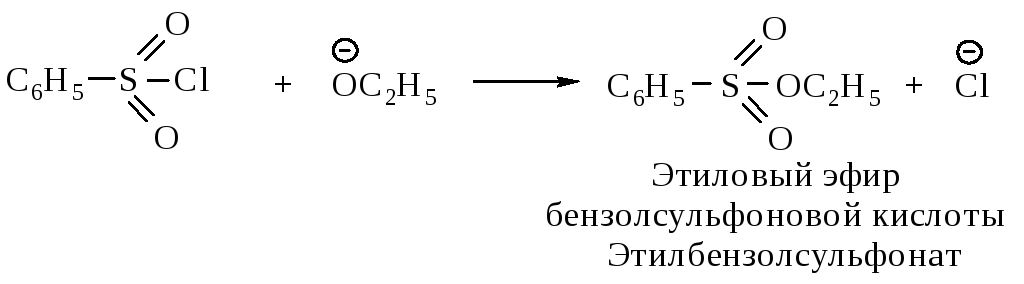
Алкиловые эфиры сульфоновых кислот часто используют в синтезах в качестве алкилирующих агентов вместо алкилгалогенидов.
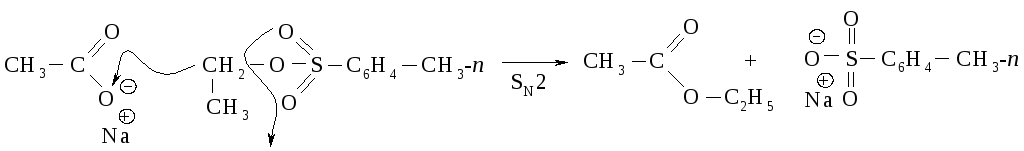
Сульфонат-ион – анион сильной кислоты и поэтому является слабым основанием и “хорошей” уходящей группой.
С аммиаком и аминами сульфохлориды реагируют с образованием амидов (сульфонамидов или сульфамидов).
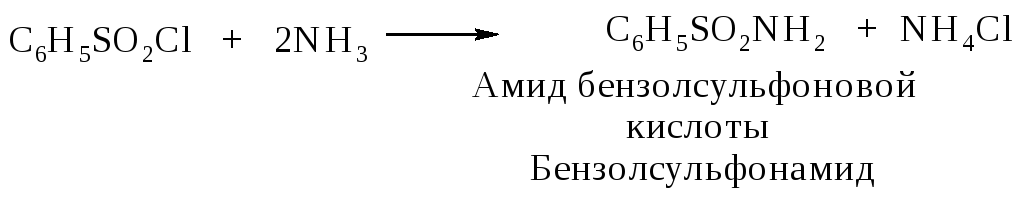
Амиды
сульфоновых кислот
![]() являются
гораздо более сильными
кислотами, чем аммиак, и более сильными
кислотами, чем амиды
карбоновых кислот
являются
гораздо более сильными
кислотами, чем аммиак, и более сильными
кислотами, чем амиды
карбоновых кислот![]() .
Сульфогруппа более эффективно способствует
удалению протона из кислоты, чем
карбоксилат-ион R–COO,
и более
эффективно способствует удалению
протона и от –NH2
группы.
Сульфамиды проявляют заметную кислотность
и легко растворяются в водных растворах
щелочей (табл. 5).
.
Сульфогруппа более эффективно способствует
удалению протона из кислоты, чем
карбоксилат-ион R–COO,
и более
эффективно способствует удалению
протона и от –NH2
группы.
Сульфамиды проявляют заметную кислотность
и легко растворяются в водных растворах
щелочей (табл. 5).
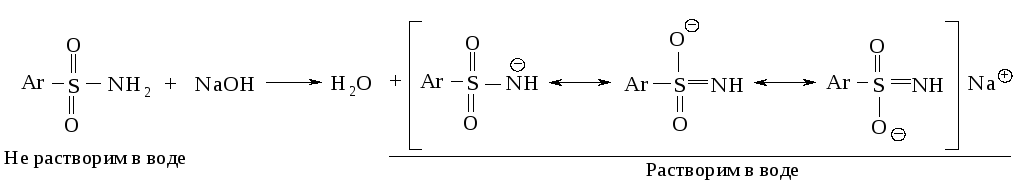
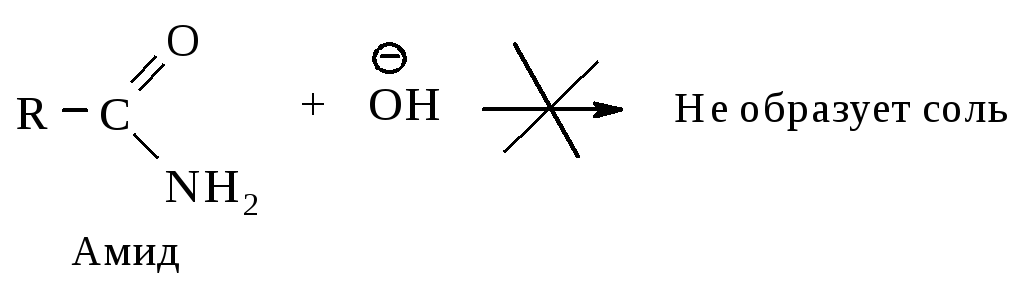
Таблица 5
Константы кислотности бензолсульфоновой и бензойной кислот и их амидов
|
|
Ка |
|
Ка |
|
С6Н5SO2OH С6Н5COOH |
очень большая 6,3·10-5 |
С6Н5SO2NH2 С6Н5CO NH2 |
10-10 10-15 |
9.1.3. Реакция замещения сульфогруппы
Замещение сульфогруппы на водород, десульфирование (SEAr). При нагревании ароматической сульфоновой кислоты при температуре 100-175 оС с раствором кислоты происходит отщепление сульфогруппы. Эта реакция является обратной реакции сульфирования.
![]()
Можно подобрать условия, которые будут направлять реакцию в любую сторону: сульфирование – большой избыток концентрированной серной кислоты, удаление H2O из реакции с помощью SO3; десульфирование – разбавленная кислота и удаление из реакции углеводорода.
Замещение сульфогруппы на -ОН – щелочной плав, получение фенола (SNAr).
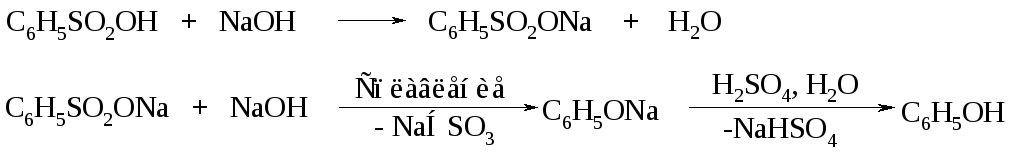
Замещение сульфогруппы на группу -СN сплавлением соли сульфоновой кислоты с цианистым натрием (SNAr).
![]()