
Биохимия. Лекция 8. Обмен белков и аминокислот. 01.04.2015
.pdf
Обмен белков и аминокислот
к.б.н. Басок Ю.Б.

СУДЬБА АМИНОКИСЛОТ В КЛЕТКЕ
Распад белков |
|
|
|
Синтез заменимых |
|
|
|
Внутриклеточный |
|||
аминокислот |
|||
пул аминокислот |
|||
Поступление с |
|||
|
|
||
|
|
||
пищей |
|
|
|
Катаболизм до СО и Н О |
|||
|
2 |
2 |
|
с образованием энергии
Синтез белков
Синтез биогенных аминов, нейромедиаторов, гормонов
Синтез заменимых  аминокислот
аминокислот
 Синтез пуриновых и пиримидиновых оснований
Синтез пуриновых и пиримидиновых оснований
Синтез глюкозы
Синтез триацилглицеролов, холестерола, кетоновых тел
Синтез креатина, карнитина и др.

ОБЩИЕ ПУТИ КАТАБОЛИЗМА АМИНОКИСЛОТ
Превращения аминокислот в клетке:
с участием аминогруппы;
по карбоксильной группе;
по радикалу.

ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
катаболизм аминокислот начинается с реакции
дезаминирования - удаления α-аминогруппы, которая выделяется в виде аммиака (токсичное соединение, в клетках подвергается обезвреживанию), и образования безазотистого остатка (α-кетокислоты).
Дезаминированию подвергаются все аминокислоты кроме
лизина и пролина.
Существует несколько типов реакций дезаминирования:
•неокислительное - характерно для Сер, Тре и Гис
•окислительное прямое - характерно только для Глу;
•окислительное непрямое - для остальных аминокислот.
Окислительное дезаминирование является основным путем катаболизма аминокислот.
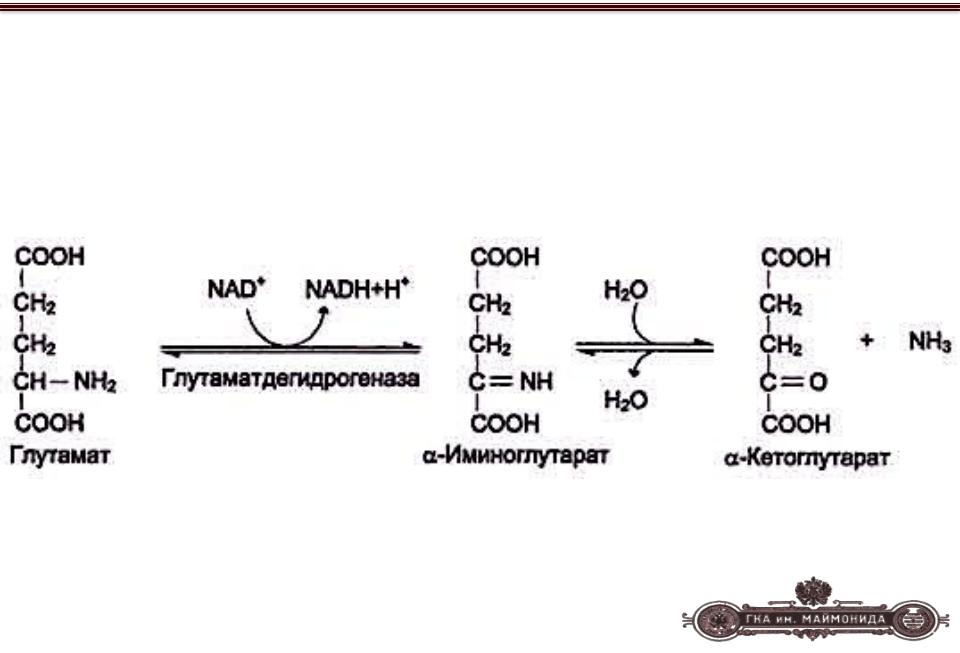
ПРЯМОЕ ДЕЗАМИНИРОВАНИЕ
Напрямую участвует лишь глутаминовая кислота.
Реакция идет в два этапа.

НЕПРЯМОЕ ДЕЗАМИНИРОВАНИЕ
Большинство аминокислот подвергается в клетке непрямому дезаминированию, которое включает две стадии:
1.трансаминирование с α-кетоглутаратом и образование глутаминовой кислоты в цитозоле клетки;
2.прямое дезаминирование глутаминовой кислоты в митохондриях.
аминокислота |
1 |
α-кетоглутарат |
NH3 |
2 |
аминотрансфераза глутаматдегидрогеназа
α-кетокислота глутамат

ТРАНСАМИНИРОВАНИЕ
Трансаминирование происходит во многих тканях, но наиболее активно - в печени.
Трансаминирование - реакция переноса α-аминогруппы с аминокислоты на α-кетокислоту, в результате чего образуются новая кетокислота и новая аминокислота.
Реакции катализируют ферменты аминотрансферазы, коферментом которых служит пиридоксальфосфат - производное витамина В6.
Реакции, протекают по механизму типа "пинг-понг».
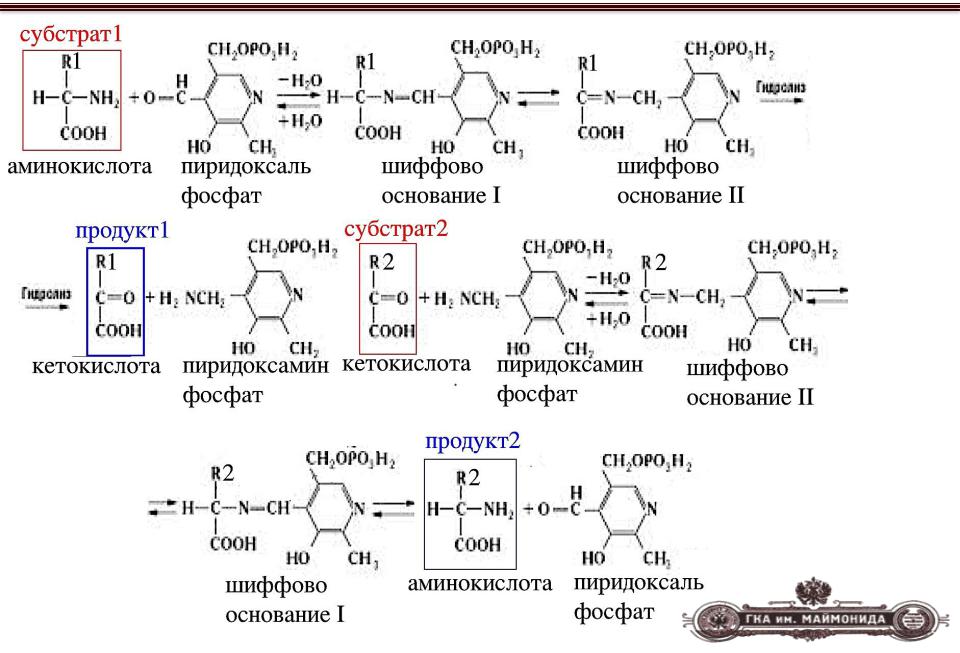
МЕХАНИЗМ РЕАКЦИИ ТРАНСАМИНИРОВАНИЯ

РЕГУЛЯЦИЯ ТРАНСАМИНИРОВАНИЯ
Трансаминирование активируется:
•при поступлении в клетку избыточного количества аминокислот;
•при прекращении использования аминокислот на синтез азотсодержащих соединений: белков, креатина,
фосфолипидов, пуриновых и пиримидиновых оснований;
•при гипогликемиях различного генеза, сахарном диабете, т.е. при внутриклеточном голодании.

ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ ТРАНСАМИНАЗ
Трансаминирование -заключительный этап синтеза заменимых аминокислот из соответствующих α-
кетокислот, если они в данный момент необходимы клеткам.
Трансаминирование - первая стадия дезаминирования большинства аминокислот, т.е. начальный этап их катаболизма. Образующиеся при этом кетокислоты окисляются в ЦТК или используются для синтеза глюкозы и кетоновых тел.
