
- •Аналитическая химия
- •Методические указания
- •Для студентов нехимических специальностей
- •Биологического и химико-технологического факультета
- •Раздел 1. Введение в аналитическую химию
- •Раздел 2. Метрологические основы аналитической химии
- •Раздел 3. Теоретические основы химических методов анализа
- •Раздел 4. Методы определения (количественный анализ). Химические методы
- •Раздел 5. Физико-химические методы анализа
- •Раздел 6.
- •Методические указания к выполнению лабораторных работ Лабораторная работа № 1 Качественный анализ катионов и анионов
- •Анализ смесей катионов
- •Анализ смесей анионов
- •Классификация катионов по кислотно-основной схеме
- •Групповые реакции анионов
- •Выполнение качественных реакций
- •Дробные реакции катионов
- •Анализ смеси анионов
- •Дробные реакции анионов
- •Лабораторная работа № 2 Определение содержания металлов в исследуемом растворе гравиметрическим методом Определение магния с 8-оксихинолином
- •Лабораторная работа № 3 Титриметрические методы анализа
- •1. Введение
- •2. Техника работы
- •1.1. Растворы, применяемые в титриметрии
- •Техника приготовления первичных стандартных растворов
- •2. Практические работы
- •Работа 2 Определение фосфорной кислоты
- •Выполнение определения
- •Лабораторная работа № 4 Окислительно-восстановительное титрование
- •Иодометрия
- •Определение меди
- •Выполнение определения
- •Лабораторная работа № 5 Комплексонометрическое титрование
- •Расчеты в комплексонометрическом титровании
- •Определение кальция и мaгния при совместном присутствии
- •Выполнение определения
- •Лабораторная работа № 6 Абсорбционная молекулярная спектроскопия
- •Фотометрические методы анализа
- •Законы поглощения электромагнитного
- •Определение железа (III) сульфосалициловой кислотой
- •Лабораторная работа № 7 Потенциометрическое титрование
- •Результаты точного титрования
- •Расчетный и графические способы обнаружения ктт
- •Кислотно-основное титрование
- •При их совместном присутствии
- •Лабораторная работа № 8 Потенциометрическое титрование.
- •Определение кобальта (II) в растворе
- •Выполнение определения
- •Лабораторная работа № 9 Кинетические методы анализа.
- •Определение меди (II) в растворах
- •Выполнение определения
- •Данные для приготовления растворов при построении градуировочного графика
- •Лабораторная работа № 10 Разделение смеси катионов металлов методом экстракции
- •Основные понятия
- •Количественные характеристики
- •Экстрагенты
- •Схемы разделения катионов методом экстракции Смесь катионов Cu (II), Zn (II), Mg(II), Mn (II), Аl (III)
- •1. Обнаружение и отделение Cu (II).
- •Марганца и алюминия
- •Лабораторная работа № 11 Разделение и обнаружение катионов и фенолов методом одномерной бумажной хроматографии.
- •Величины Rf. Некоторых катионов
- •Реагенты для обнаружения катионов на хроматограмме
- •IV. Варианты контрольных работ для студентов заочного отделения
- •Вариант № 2
- •Вариант № 3
- •Вариант № 4
- •Вариант № 6
- •Вариант № 7
- •Вариант № 8
- •Вариант № 10
- •Вариант № 14
- •Вариант № 15
- •Вариант № 18
- •Вариант № 20
- •V. Вопросы к экзамену
- •VI. Структура экзаменационного билета
- •VII. Рекомендуемая литература
Лабораторная работа № 2 Определение содержания металлов в исследуемом растворе гравиметрическим методом Определение магния с 8-оксихинолином
OH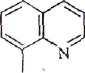
8-Оксихинолин при рН 9,5 - 12,7 количественно осаждает магний в виде желтого кристаллического осадка оксихинолината магния Mg(C9H6NO)2.2Н2О. Это соединение может являться гравиметрической формой, если осадок высушивать при 105°С. При высушивании при 130° С осадок теряет воду и гравиметрической формой является Mg(C9H6NO)2. При осаждении магния в растворе должны отсутствовать все элементы, кроме щелочных металлов. Гравиметрический фактор F Mg = 0,0778 (130°С).
Реагенты
Соляная кислота, НС1, концентрированная с пл. 1,17 г/мл.
8-Оксихинолин, 5%-ный раствор в 2 М уксусной кислоте.
Аммиак, NН3, раствор 1: 1.
Индикатор фенолфталеин, 0,1%-й раствор в 60%-ом этаноле.
Выполнение определения.
Исследуемый раствор соли магния разбавляют водой примерно до 150 мл, добавляют 5 мл НС1, 5-7 капель фенолфталеина и нагревают примерно до 80°С, добавляют 15 мл раствора 8-оксихинолина и прибавляют по каплям из бюретки при перемешивании раствор аммиака до слабого запаха (раствор окрашивается в розовый цвет). Раствор с осадком нагревают на водяной бане 30-40 мин. Затем отфильтровывают осадок в стеклянный фильтрующий тигель, промывают осадок горячей водой пока фильтрат не станет бесцветным. Тигель с осадком высушивают в сушильном шкафу при 130°С до постоянной массы.
Лабораторная работа № 3 Титриметрические методы анализа
«Кислотно-основное титрование»
1. Введение
В титриметрическом анализе количество химических веществ определяют чаще всего путем точного измерения объемов растворов двух веществ, вступающих между собой в определенную реакцию. Реагент берут в количестве, эквивалентном определяемому веществу. Методы титриметрического анализа можно классифицировать, например, по характеру химической реакции, лежащей в основе определения веществ. Эти реакции относятся к различным типам — реакциям соединения ионов и реакциям окисления — восстановления. В соответствии с этим титриметрические определения подразделяют на следующие основные методы: метод кислотно-основного титрования, методы комплексометрического и окислительно-восстановительного титрования. Вещества реагируют между собой в эквивалентных количествах (п1 = п2).
Эквивалент - условная или реальная частица, которая может присоединять, высвобождать, замещать один ион водорода в кислотно-основных реакциях или быть эквивалентна одному электрону в окислительно-восстановительных реакциях. Если определяемое вещество А реагирует с титрантом В по уравнению
аА + bВ ® продукты реакции
то из этого уравнения следует, что одна частица А эквивалентна b/a частицам вещества В. Отношение b/a называют фактором эквивалентности и обозначают fэкв..
Например, для кислотно-основной реакции
H3PO4 + NaOH = NaH2PO4 + H2O
fэкв.. (H3PO4) = 1
а для реакции H3PO4 + 2NaOH = Na2HРО4 + 2H2O
fэкв.. (H3PO4) = 1/2
В окислительно-восстановительной полуреакции:
MnO4- + 8H+ + 5e = Mn2+ + 4H2O
fэкв.. (KMnO4) = 1/5
но в полуреакции
MnO4- + 4H+ + 3e = MnO(OH)2 + H2O
fэкв.. (KMnO4) = 1/3
Молярной массой эквивалента вещества называют массу одного моля эквивалента этого вещества, которая равна произведению фактора эквивалентности на молярную массу вещества. Так как число эквивалентов веществ, вступающих в реакцию, равно
n = cV . 10-3
где с - молярная концентрация эквивалента (нормальная концентрация);
V - объем, то для двух cтехиометрически реагирующих веществ справедливо равенство:
С1V1 = C2V2
Если молярная концентрация одного вещества известна, то, измеряя объемы реагирующих веществ, можно рассчитать неизвестную концентрацию второго вещества.
Молярная концентрация эквивалента (нормальная концентрация) - С - отношение числа молей растворенного вещества к объему. Например. С (l/2H2SO4) = 0,1 моль л -1 или С (l/2H2SO4)= 0,1 М; это означает, что в 1 л раствора содержится 6,02 10 -23 . 0,1 условных частиц 1/2 H2SO4, или в 1 л растворено 4,9г H2SO4.
Например, раствор Ва(ОН)2 стандартизовали по 0,1280 М раствору HC1. Для титрования 46,25 мл раствора кислоты потребовалось 31,76 мл раствора основания. Следовательно,
с (1/2 Ва(ОН)2) = (46,25 . 0,1280)/31,76 = 0,1864 М
т = сМfэкв. = 0,1864 . 171,34 . 1/2= 15,97 г
В реакциях комплексообразования для вещества довольно трудно определить понятие молярная масса эквивалента. В данном случае обычно базируются на стехиометрии реакции. Например, в комплексонометрии независимо от заряда катиона реакции протекают по уравнению:
Mn+ + H2Y2- = MY(n-4)+ + 2H+
