- •И.А. Короткий Научные основы криологии
- •Кемерово 2005
- •Предисловие
- •Введение
- •1. Базовые термодинамические понятия и законы. Применение первого и второго закона термодинамики
- •1.1. Принцип сохранения массы, материальный баланс
- •1.2. Принцип сохранения энергии. Энергетический баланс
- •1.3. Принцип возрастания энтропии. Уравнение энтропийного баланса. Необратимость и затрата работы
- •1.4. Принцип недостижимости абсолютного нуля термодинамической температуры
- •Контрольные вопросы:
- •2. Термодинамические диаграммы и процессы криогенных систем
- •2.1. Равновесные состояния и фазовые переходы чистых веществ
- •2.2. Рабочие диаграммы криогенных систем
- •2.3. Равновесные состояния и фазовые переходы бинарных систем
- •Контрольные вопросы и задания:
- •3. Основные процессы для получения низких температур
- •3.1. Процессы внешнего и внутреннего охлаждения
- •3.2. Сжатие реальных газов в обратных термодинамических циклах
- •Контрольные вопросы и задания:
- •4. Процессы, сопровождающиеся понижением температуры
- •4.1. Дросселирование газов, паров и жидкостей
- •4.2. Равновесное адиабатное расширение газа в детандере
- •Контрольные вопросы и задания:
- •5. Идеальные циклы криогенных систем
- •5.1. Криогенное термостатирование
- •5.2. Криогенное охлаждение
- •5.3. Криогенная конденсация и кристаллизация
- •5.4. Ожижение криогенных газов
- •5.5. Разделение газовых смесей
- •Контрольные вопросы и задания:
- •6. Реальные циклы криогенных систем
- •6.1. Классификация криогенных циклов
- •6.2. Основные характеристики реальных циклов низкотемпературных систем
- •6.3. Энергетический баланс отдельных ступеней охлаждения
- •6.4. Ступени охлаждения криогенных систем
- •6.4.1. Ступень внешнего охлаждения
- •6.4.2. Ступень с расширением потока в детандере
- •6.4.3. Ступень с расширением потока в дроссельном устройстве
- •Контрольные вопросы и задания:
- •7. Основные циклы низкотемпературных установок
- •7.1. Дроссельные циклы ожижения
- •7.1.1. Цикл с простым дросселированием
- •7.1.2. Цикл с предварительным охлаждением и дросселированием
- •7.1.3. Цикл с двойным дросселированием и циркуляцией части потока
- •7.1.4. Цикл с двойным дросселированием и предварительным охлаждением
- •7.2. Комбинированные циклы с дросселированием и расширением рабочего вещества в детандерах
- •7.2.1. Циклы среднего и высокого давления
- •7.2.2. Цикл низкого давления с турбодетандером
- •7.2.3. Цикл с расширением в детандере, дросселированием и предварительным охлаждением
- •Контрольные вопросы и задания:
- •8. Газовые холодильные машины
- •Контрольные вопросы и задания:
- •9. Разделение газовых смесей
- •9.1. Равновесные составы фаз идеальной системы
- •9.2. Процесс ректификации бинарной смеси
- •9.3. Ректификационная колонна
- •9.4. Колонна однократной ректификации
- •9.5. Двукратная ректификация
- •Контрольные вопросы и задания:
- •10. Теплообменные аппараты криогенных установок
- •10.1. Особенности теплообменника в криогенных системах
- •10.2. Теплообменные аппараты, их классификация и виды теплообменных поверхностей
- •10.3. Эффективность теплообменников
- •10.4. Теплоизоляция криогенных систем
- •Библиографический список
- •Оглавление
- •Научные основы криологии
- •650056, Г. Кемерово, б-р Строителей, 47
- •650010, Г. Кемерово, ул. Красноармейская, 52
5.2. Криогенное охлаждение
Рассмотрим охлаждение газа при установившемся изобарном процессе.
Принципиальная схема и идеальный цикл такого процесса представлены на рис. 16.
|
а)
|
б) |
|
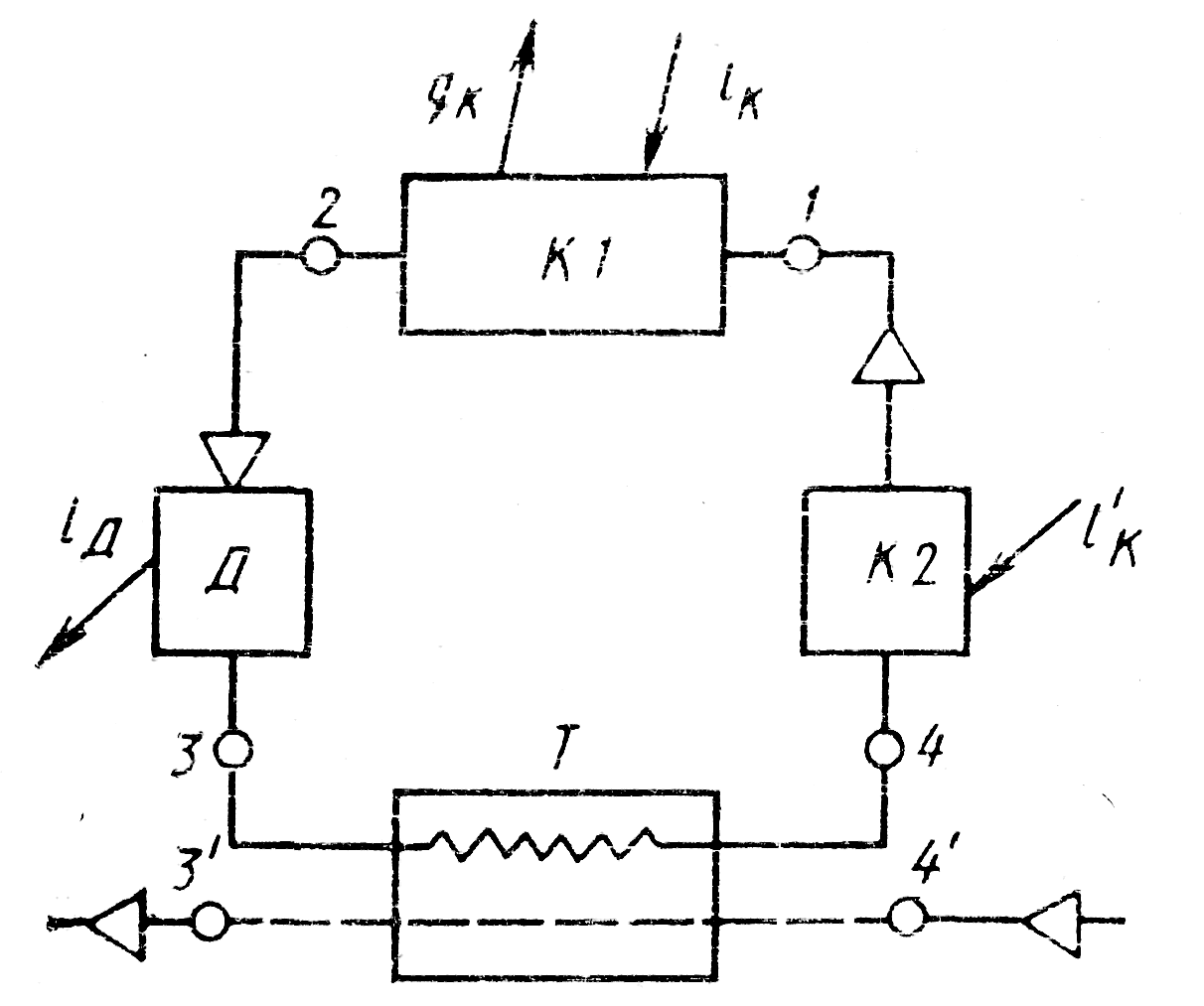
рис. 16. Принципиальная схема и цикл охлаждения: а) схема обратимого цикла для охлаждения газа (сплошная линия - рабочее вещество, штриховая линия - охлаждаемый газ); б) обратимый цикл охлаждения газа в диаграмме Т-s | |
Если температура охлаждаемого вещества снижается от Tx’ до Tx”, то от единицы массы вещества отводится теплота
![]() , (32)
, (32)
где
![]() и
и![]() - энтальпии охлаждаемого вещества при
давленииpх
и температуре Tx’
и Tx”.
- энтальпии охлаждаемого вещества при
давленииpх
и температуре Tx’
и Tx”.
Цикл для осуществления процесса охлаждения 4’ – 3’: 1-2 - изотермическое сжатие; 2-3 - адиабатическое расширение; 3-4 - изобарный нагрев в теплообменнике; 4-1 - адиабатическое сжатие.
Процесс теплообмена в теплообменнике характеризуется отсутствием гидравлических потерь, а также равенством температур охлаждаемого и нагреваемого газа во всех сечениях аппарата.
Работа, затрачиваемая в таком цикле, может быть определена из уравнения энергетического баланса:
lmin = lк +lк’ – lд = qk - qx. (33)
Заменив qk и qx соответствующими значениями, получим
lmin = T0(s1 – s2)(i4 – i3). (34)
5.3. Криогенная конденсация и кристаллизация
Конденсацию и кристаллизацию можно осуществить по-раз-ному: при постоянном давлении, при постоянном объеме.
Наиболее часто на практике встречается изобарный процесс, при конденсации и затвердевании чистого вещества его температура не изменяется, теплота qx выделяется за счет фазового перехода. Следовательно, в криогенном устройстве тепловые процессы подобны процессам термостатирования. Различие заключается в природе возникновения теплового потока, который возникает вследствие фазового перехода.
5.4. Ожижение криогенных газов
Ожижение газа при минимальном расходе энергии представлено на рис. 17.
Пусть первоначальному состоянию газа на диаграмме Т—s соответствует точка 1 (рис. 17, а). Если газ сначала сжать в компрессоре при постоянной температуре, равной температуре окружающей среды То, до очень высокого давления р2 (процесс 1-2), а затем расширить в детандере (процесс 2-f при s = const), то можно получить жидкость в состоянии, соответствующем точке 1. Если оба процесса обратимы, то минимально необходимая для ожижения газа работа определяется следующим образом:
lmin = lk – lq. (35)
При изотермическом сжатии требуется затратить работу, которая рассчитывается по формуле:
lk=T0(s1-s2) - (i1 - i2), (36)
где i1 и i2 - энтальпия газа соответственно в начале и конце процесса сжатия.
При расширении газа в детандере производится работа:
lд = i2 – if, (37)
где if - энтальпия жидкости.
Таким образом,
lmin = T0(s1-s2) - (i1 – if ). (38)
|
а) |
б) |
|
Рис. 17. Идеальное ожижение газов: а) процесс ожижения газа в диаграмме Т-s; б) схема идеального цикла для ожижения газа (сплошные линии - рабочее вещество, штриховая линия - ожижаемый газ) | |
Процесс ожижения газа можно организовать иначе. Пусть ожижение газа происходит по наиболее естественному процессу - изобарному при р1 = const. Тогда газ необходимо предварительно охладить от состояния 1 до состояния 3 (процесс 1-3), а затем сконденсировать (процесс 3-f). При охлаждении газа от него отнимается теплота qoxn = i1 – i3 этому количеству теплоты на рис. 17, а эквивалентна площадь 1-3-b-c-1 При конденсации отводится теплота qкд=i3 – if; площадь f-a-b-3-f на рис. 17, а соответствует теплоте конденсации.
Общее количество теплоты, отведенной от единицы массы газа при его ожижении в изобарном процессе 1-3-f составляет:
qx = qохл + qкд = i1 – if. (39)
Представить осуществление этих обратимых процессов можно при помощи цикла, называемого идеальным циклом для ожижения газов. Представим себе установку, состоящую из компрессора К, детандера Д и теплообменника Т (рис. 17, б). Рабочее вещество (криоагент) сжимается в компрессоре при постоянной температуре То (процесс 1-2), расширяется в детандере при постоянной энтропии (s2 = const) до состояния жидкости f и направляется в теплообменник Т, где вступает в тепловой контакт с ожижаемым газом (криопродуктом); причем во всех сечениях аппарата рабочее вещество и ожижаемый газ имеют одинаковые параметры состояния, но отделены один от другого теплопередающей поверхностью. Уравнение энергетического баланса:
lК-lД=qК-qx, (40)
где qК - теплота, отдаваемая в окружающую среду в процессе 1-2, ее можно определить по формуле (28) (см. стр. 32); qx - теплота, отбираемая криоагентом от ожижаемого газа в процессе lk-3k-fk (параметры состояния в точках lk, 3k и fk такие же, как в точках соответственно 1, 3, f).
Теплота qx численно равна теплоте, отведенной от единицы массы газа при его ожижении, и может быть найдена по формуле (39) (см. стр. 36). Она определяет полезную удельную холодопроизводительность цикла при переменном уровне температуры от То до Tx. После подстановки соответствующих значений в выражение (40) получим:
lmin = T0(s1-s2) - (i1 – if ).
На диаграмме Т-s (рис.17, а) этой работе эквивалентна площадь 1-2-f-3-1.
Минимальная работа lmin, затрачиваемая на ожижение 1 кг и 1 л различных газов, указана в табл. 1.
Для сравнения приведена примерная действительная работа ожижения некоторых газов.
Таблица 1
Минимальная lmin и приблизительная действительная l работа ожижения
некоторых газов при р = 0,1013 МПа и То = 300 К
|
Газ |
i1-if, кДж/кг |
lmin |
l | ||
|
(кВтч)/кг |
(кВтч)/л |
(кВтч)/кг |
(кВтч)/л | ||
|
Азот |
433,3 |
0,213 |
0,172 |
1,21,8 |
11,5 |
|
Аргон |
273,1 |
0,134 |
0,186 |
0,81 |
1,11,4 |
|
Водород |
3953 |
3,31 |
0,235 |
2242 |
1,53,0 |
|
Воздух |
428,3 |
0,205 |
0,179 |
1,21,8 |
11,5 |
|
Гелий |
1563 |
1,9 |
0,237 |
1632 |
24 |
|
Кислород |
406,9 |
0,177 |
0,202 |
11,5 |
1,21,7 |
|
Метан |
912,7 |
0,307 |
0,13 |
0,61 |
0,250,5 |
|
Неон |
368,6 |
0,372 |
0,445 |
3,55,5 |
34,5 |