
- •Биоорганическая и биологическая химия.
- •Биоорганическая химия.
- •Содержательный модуль 1
- •Тема: «Функциональные группы органических соединений, Краткий обзор строения и химических свойств углеводородов, спиртов, фенолов, тиолов и аминов».
- •Тема:»Строение и химические свойства альдегидов, кетонов».
- •Тема:»Строение и химические свойства моно- и дикарбоновых кислот»
- •Тема:»Строение и химические свойства окси, оксокислот».
- •Содержательній модуль 2 тема:» Углеводы. Строение и химические свойства моносахаридов».
- •25. Аминосахара – важные производные моносахаридов. Укажите, при каком углероде гидроксильная группа обычно замещается на аминогруппу:
- •Тема:» Вуглеводы. Строение и химические свойства ди- и полисахаридов».
- •Содержательный модуль 3 тема:» Строение и химические свойства гетероциклических соединений».
- •Содержательный модуль 4 тема:»Аминокислоты. Пептиды. Понятие о нуклеиновых кислотах».
Содержательный модуль 4 тема:»Аминокислоты. Пептиды. Понятие о нуклеиновых кислотах».
1. В каждой макромолекуле белка α-аминокислоты, являющие его структурными компонентами , соединены между собой пептидной связью. Укажите эту группу атомов:
*


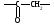

 .
.
2. Аланин – одна из двадцати α-аминикислот, входящих в состав белков. Укажите, какую реакцию среды он имеет в водном растворе:

pH = 3
pH = 5
*pH = 7
pH = 9
pH = 11
3. В организме человека присутствует 8 аминокислот, которые необходимы для синтеза белков, но в организме не синтезируются, а попадают извне. Укажите название таких аминокислот:
β -аминокислоты
α -аминокислоты
Протеиды
*Незаменимые
γ-аминокислоты
4. В ходе лабораторной работы студенты изучали свойства аминокислот. Укажите, реакцией с какими веществами можно доказать их амфотерность:
NaOH и KCN
HCl и C2H5OH
*NaOH и HCl
C2H5OH и KOH
HNO2 и NaCl
5. Для построения белков человеческого организма используются только одного вида стереоизомеры аминокислот. Укажите их:
β –аминокислоты в D-конфигурации
α –аминокислоты в D-конфигурации
β –аминокислоты в L-конфигурации
γ-аминокислоты в D-конфигурации
*α –аминокислоты в L-конфигурации
6. Аминокислоты являются универсальным биологическим материалом, благодаря их способности полимеризоваться. α-аминокислоты – мономеры белков. При помощи какой связи аминокислоты соединяются в цепь?
Водородная
Электростатическая
Пептидная
Гидрофобная
Дисульфидная
7. Для аминокислот существует несколько видов классификаций, одна из учитывает количество амино- и карбоксильных групп в структуре молекулы. Классифицируйте приведенную аминокислоту в зависимости от данного признака:

А. Моноаминомонокарбоновая
В. *Моноаминодикарбоновая
С. Диаминомонокарбоновая
D. Диаминодикарбоновая
Е. Моноаминотрикарбоновая
7. При кислотном гидролизе РНК были получены: гетероциклическое основание, углеводный остаток и остаток неорганической кислоты. Укажите моносахарид, входящий в состав данной нуклеиновой кислоты:
D-глюкоза;
D-фруктоза;
*D-рибоза;
Дезокси-D-рибоза;
D-галактоза.
8. В 1953г. Уотсон и Криг описали в виде модели вторичную структуру ДНК. Укажите компонент этой структуры:
Одинарная α-спираль;
β-складчатая структура;
Двойная левозакрученная спираль;
Фибриллярная структура;
*Двойная правозакрученная спираль.
9. При кислотном гидролизе нуклеиновых кислот образуются нуклеотиды. Укажите их состав:
Нуклеозид-21-фосфат;
Нуклеозид-41-фосфат;
*Нуклеозид-51-фосфат;
Нуклеозид-61-фосфат;
Нуклеозид-81-фосфат.
10. Вторичная структура ДНК существует за счет образования водородных связей между комплементарными парами азотистых оснований. Укажите данные пары:
*Т – А, С – G;
Т – G, C – А;
Т – C, А – G;
Т – Т, А – А;
C – C, G – G.
11.В лаборатории для обнаружения α-аминокислот использовали качественную реакцию. Укажите название данной реакции:
А. Биуретовая реакция
В. *Нингидриновая
С. Метод Ван-Слайка
D. Формольного титрования
Е. Диспропорционирования
12. Фридрих Мишер впервые обнаружил ДНК в ядрах клеток. Укажите роль данных кислот в организме:
Являются структурными компонентами липидов
Важнейшие энергетические вещества
Катализаторы биологических процессов
*Участвуют в передаче наследственной информации
Являются структурными компонентами витаминов
13. В состав макроэргического соединения АТФ входит нуклеозид аденозин. Укажите вещества, которые входят в состав данного нуклеозида:
Аденин и дезокси-D-рибоза;
*Аденин и D-рибоза;
Аденин и фосфорная кислота;
D-рибоза и фосфорная кислота;
Дезокси-D-рибоза и фосфорная кислота.
14. В нуклеиновых кислотах органические основания связаны с моносахаридным остатком химической связью. Укажите тип данной связи:
Водородная;
Семиполярная;
*N-гликозидная;
Ионная;
О-гликозидная.
15. В результате воздействия на нуклеиновые кислоты химических факторов произошло изменение аминокислотной последовательности в синтезируемом белке. Укажите название такого явления:
Рацемизация;
Денатурация;
Мутаротация;
Расщепление;
*Мутация.
16. В процессе биохимических исследований было доказано, что в физиологических условиях нуклеотиды находятся полностью в ионизированном состоянии. Укажите факторы, от которых зависит данное состояние:
Температуры;
*pH среды;
Ферментов;
Давления;
Таутомерии.
17. Аминокислоты гетерофункциональные соединения, содержащие две функциональные группы. Укажите аминокислоту, имеющую неполярный (гидрофобный) радикал:
*Серин.
Аланин.
Лизмн.
Глутаминовая кислота.
Цистеин.
18. Для аминокислот характерна стереоизомерия, поэтому для обозначения их конфигурации применяют D, L – систему.Укажите, конфигурацию аминокислот, входящих в состав белков человека:
β, D аминокислоты
α, D аминокислоты
*α, L аминокислоты
β, L аминокислоты
γ, L аминокислоты.
19. В зависимости от природы радикала аминокислоты (АК) относятся к различным группам. Укажите, к какой группе можно отнести фениаланин:
Гетероциклические
Ароматические.
Алифатические
-аминокислоты
γ-аминокислоты
20. Аминокислоты существуют в растворе в разных ионных формах.Укажите фактор, от которого это зависит:
Природы растворителя.
Степени диссоциации
*рН раствора.
Концентрации аминокислоты.
Температуры
21. Аминокислоты вступают в различные химические реакции.Укажите конечный продукт при взаимодействии глицина с уксусным альдегидом:
Соль.
Лактон.
Кислота.
Имин.
Спирт.

 22.
По кислотно-основным свойствам
аминокислоты делятся на несколько
групп. Укажите аминокислоту, относящуюся
к основным:
22.
По кислотно-основным свойствам
аминокислоты делятся на несколько
групп. Укажите аминокислоту, относящуюся
к основным:
Аланин.
Валин.
Глицин.
*Лизин.
Серин.
23. Аминокислоты вступают в реакции с альдегидами. Укажите класс соединений, образующийся при этом:
Спирты
*Имины
Альдегиды
Кислоты
Сложные эфиры
24. По кислотно-основным свойствам аминокислоты делятся на несколько групп. Укажите аминокислоту, относящуюся к кислым:
Гистиди.
Фенилаланин
*Глутаминовая кислота
Аргинин.
Оксипролин
25. Аминокислоты биологически активные соединения, для которых характерна стереоизомерия. Укажите количество ассиметрических атомов углерода в молекуле -аминопропионовой кислоты:
Один.
Два.
Три.
Четыре
Пять
26. Аминокислота гистидин в своей структуре содержит гетероциклический радикал. Укажите гетероцикл, радикал которого входит в структуру данной аминокислоты:
Пиридин
Индол
Пиразол
Пиримидин
*Имидазол
27. По кислотно-основным свойствам аминокислоты делятся на несколько групп. Укажите аминокислоту, относящуюся к нейтральным:
Лизин.
Аланин
Глутаминовая кислота.
Серин
Аспаргиновая кислота
28. В организме человека глутаминовая кислота подвергается дезаминированию. Укажите продукт ее дезаминировании:
*α-Оксокислота и аммиак
Альдегид и вода
Кетон и аммиак
β-Оксикислота и вода
Е. Молочная кислота и азот
29. Белки состоят из аминокислотных фрагментов и обладают различными уровнями структурной организации. Укажите определение, описывающее первичную структуру белка:
Полинуклеотидная цепь
*Полипептидная цепь
Полисахаридная цепь
Смесь аминокислот
Полиамидная цепь
30. α-Аминокислоты, являющие структурными компонентами клеток, классифицируют по природе радикала, входящего в ее структуру. Классифицируйте аминокислоту аланин:

Дикарбоновая, полярный радикал;
Алифатическая, полярный радикал;
Серусодержащая, полярный радикал;
Кислородсодержащая, полярный радикал;
Алифатическая, неполярный радикал.
31. Практические все природные аминокислоты принадлежат к L-ряду. Укажите L- форму аспарагиновой кислоты:



С.
D.

Е.
32. α-Аминокислоты классифицируют в зависимости от признака, положенного в основу деления на группы. Классифицируйте приведенную аминокислоту в зависимости от количества амино- и карбоксильных групп:

А. Моноаминомонокарбоновая
В. Моноаминодикарбоновая
С. *Диаминомонокарбоновая
D. Диаминодикарбоновая
Е. Моноаминотрикарбоновая
33. При кислотном гидролизе РНК были получены: гетероциклическое основание, углеводный остаток и остаток неорганической кислоты. Укажите моносахарид, входящий в состав данной нуклеиновой кислоты:
А. D-глюкоза
В. D-фруктоза
С. *D-рибоза
D. Дезокси-D-рибоза
Е. D-галактоза.
34. Аминокислоты могут взаимодействовать между собой и образовывать длинные пептидные цепи. Укажите функциональные группы, участвующие в этом процессе:
Гидроксильные а аминогруппы
Гидроксильные группы
Карбоксильные группы
Аминогруппы и карбонильные
*Аминогруппы и карбоксильные
35. Биологические катализаторы – ферменты являются полипептидными веществами. Укажите при помощи, какой реакции можно определить наличие пептидной связи в белках и пептидах:
*Биуретовая реакция;
Ксантопротеиновая реакция;
Метод Ван-Слайка
Реакция формольного титрования;
Реакция серебряного зеркала.
36. При ферментативном гидролизе нуклеиновых кислот были получены гетероциклические основания, углеводный остаток и остаток неорганической кислоты. Укажите пуриновые основания, входящие в состав этих кислот:
Урацил, тимин, цитозин;
Пиррол, индол;
Имидазол, пиразол;
*Аденин, гуанин;
Пиридин, пиримидин.
37. В организме -аминокислоты подвергаются окислительному дезаминированию под действием ферментов оксидаз и окислительного агента кофермента НАД+. Укажите продукт этой реакции:
*


D.

Е.
38.L-Аспарагиновая кислота в организме под действием фермента аспартазы подвергается неокислительному дезаминированию. Укажите конечный продукт реакции:
А. Янтарная кислота
В. Щавелевоуксусная
С. Этиламин
D. *Фумаровая кислота
Е. Ацетоуксусная
39. В лаборатории методом Ван-Слайка проводили окислительное дезаминирование аминокислоты аланин. Укажите конечный продукт реакции:
А. Пировиноградная кислота
В. Этиламин
С. *Молочная кислота
D. Пропионовая кислота
Е. Этаноламин
40. -Аминокислоты могут взаимодействовать с альдегидами. Укажите конечный продукт реакции:
А. Карбоновые кислоты
В. Ангидриды
С. *Имины
D. Сложные эфиры
Е. Оксокислоты
41. -Аминокислоты относительно легко декарбоксилируются. Укажите конечный продукт при проведении этой реакции с аланином:

А. Метиламин
В. Этиламин
С. Молочная кислота
D. Формальдегид
Е. Ангидрид
42. В живом организме -аминокислота гистидин под влиянием фермента декарбоксилазы подвергаются декарбоксилированию. Укажите, какой биогенный амин образуется при этом:
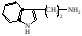

В.

С.

D*.

Е.


