
Ф изика термодинамика бля лекции и вопросы / OF3_2_Pervoe_nachalo_termodinamiki_mini
.pdf3.2. Первое начало термодинамики
3.2.1.Термодинамические процессы; графическое изображение процессов. Направленные процессы
3.2.2.Внутренняя энергия
3.2.3.Циклические процессы
3.2.4.Работа и теплота; первое начало термодинамики
3.2.5.Превращение энергии в химических реакциях
3.2.6.Термохимия
© А.В. Бармасов, 2006-2013 |
1 |
12+ |
|
3.2.1. Термодинамические процессы; графическоеафическое изображение процессов. Направленные процессыпроцессы
Изменение состояния термодинамической системы называют
термодинамическим процессом.
Неравновесные процессы – физические процессы, в которых система проходит через неравновесные состояния.
Процесс релаксации – процесс перехода из неравновесного состояния в равновесное.
Время релаксации τ – характеристика процесса установления термодинамического равновесия в макроскопической физической системе. За время релаксации отклонение какоголибо параметра системы от равновесного значения уменьшается в e ≈ 2,72 раз.
Термодинамическая диаграмма – геометрическое изображение равновесных состояний термодинамической системы при разных значениях параметров, определяющих эти состояния: температуры, давления, концентрации, мольного объёма и т.п.
© А.В. Бармасов, 2006-2013 |
2 |
12+ |
|
Квазистатический процесс
(Quasi-static process)
Итак, термодинамический процесс – переход системы из одного состояния в другое. Если внешнее воздействие осуществляется достаточно медленно, и система успевает приходить в состояние равновесия каждый раз после изменения внешних условий, то говорят о
квазистатическом (квазиравновесном) процессе.
Квазистатические процессы изображаются на координатной плоскости непрерывными кривыми.
© А.В. Бармасов, 2006-2013 |
3 |
12+ |
|
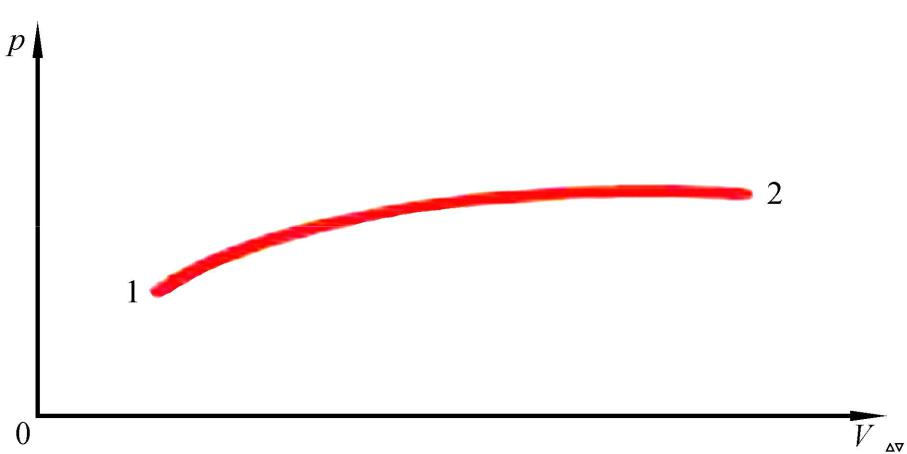
Квазистатический процесс
(Quasi-static process)
© А.В. Бармасов, 2006-2013 |
4 |
12+ |
|
Изотермический процесс
(Isothermal process)
Изотермический процесс – термодинамический процесс, происходящий в системе при постоянной температуре; на термодинамической диаграмме изображается изотермой.
Изотерма – линия на термодинамической диаграмме, изображающая процесс, проходящий в физической системе с постоянной массой при постоянной температуре.
Уравнение изотермы идеального газа (закон Бойля– Мариотта):
pV = const при m = const
© А.В. Бармасов, 2006-2013 |
5 |
12+ |
|

Семейство изотерм для одной и той же массы газа, но при разных температурах на диаграмме p– V (T3 > T2 > T1)
© А.В. Бармасов, 2006-2013 |
6 |
12+ |
|
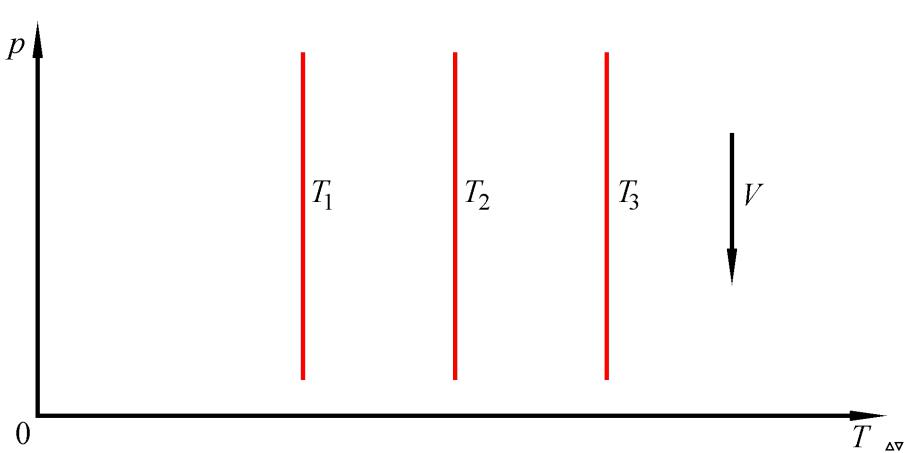
Семейство изотерм для одной и той же массы газа, но при разных температурах на диаграмме p– T
© А.В. Бармасов, 2006-2013 |
7 |
12+ |
|

Семейство изотерм для одной и той же массы газа, но при разных температурах на диаграмме V– T
© А.В. Бармасов, 2006-2013 |
8 |
12+ |
|

Изобарический процесс
(Isobaric process)
Изобара – линия на термодинамической диаграмме, изображающая термодинамический процесс, происходящий в физической системе с постоянной массой при постоянном давлении
(изобарический или изобарный процесс).
Уравнение изобары идеального газа (закон ГейЛюссака):
V = const при m = const
T
© А.В. Бармасов, 2006-2013 |
9 |
12+ |
|

Семейство изобар для одной и той же массы газа, но при разных давлениях на диаграмме V– T (p3 > p2 > p1)
© А.В. Бармасов, 2006-2013 |
10 |
12+ |
|
