
- •Типовые аттестационные задания по химии Учебно-методическое пособие
- •Дорогой студент !
- •1. Классификация и свойства неорганических соединений
- •2. Основные понятия и законы химии
- •3. Строение вещества
- •3.1. Строение атома
- •3.2. Периодический закон и периодическая система химических элементов д.И. Менделеева
- •3.3. Химическая связь
- •4. Основы термодинамики
- •4.1. Термохимические понятия и расчёты
- •4.2. Элементы химической термодинамики
- •5. Общие закономерности химических процессов
- •5.1. Химическая кинетика
- •5.2. Химическое равновесие
- •5.3. Поверхностные явления и адсорбция
- •6. Дисперсные системы
- •6.1. Грубодисперсные системы
- •6.2. Коллоидные системы
- •7. Растворы
- •7.1. Способы выражения состава растворов
- •7.2. Коллигативные свойства разбавленных растворов неэлектролитов
- •8. Растворы электролитов
- •8.1. Свойства растворов электролитов
- •8.2. Ионное произведение воды. Водородный показатель
- •8.3. Реакции ионного обмена
- •8.4. Гидролиз солей
- •9. Окислительно-восстановительные реакции
- •10. Электрохимические процессы.
- •10.1. Активность и коррозия металлов
- •10.2. Гальванические элементы
- •10.3. Электролиз
- •11. Основы аналитической химии
- •11.1. Качественный химический анализ
- •11.2. Количественный химический анализ
- •11.3. Физико-химические и физические методы анализа. Методы разделения
- •12. Основы органической химии
- •12.1. Органические соединения и реакции
- •12.2. Высокомолекулярные соединения. Методы получения, строение
- •12.3. Биополимеры
- •12.4. Белки. Нуклеиновые кислоты.
- •12.5. Углеводы, или сахара. Липиды, или жиры.
- •2. Растворимость кислот, оснований и солей в воде
- •3. Относительные электроотрицательности атомов
- •4. Стандартные электродные потенциалы
- •Типовые аттестационные задания по химии
11. Основы аналитической химии
11.1. Качественный химический анализ
Ионы Сu2+ в смеси с ионами Fе2+, Fе3+ и Zn2+ можно обнаружить, используя в качестве реактива водный раствор … .
1) Н2S 2) К4[Fе(СN)6]
3) К3[Fе(СN)6] 4) NН3
Чёрный осадок с сульфид-ионом (S2–) образует ион … .
1) Zn2+ 2) К+ 3) Рb2+ 4) Nа+
Гексанитрокобальтат(III) натрия Nа3[Со(NО2)6] используется для качественного обнаружения ионов … .
1) Рb2+ 2) Сu2+ 3) К+ 4) Nа+
К аналитическому сигналу можно отнести … .
1) образование воды
2) появление (изменение) окраски
3) выделение газа
4) повышение температуры
Наименьшее количество ионов, которое удаётся обнаружить с помощью качественной реакции, называется … .
1) предельной концентрацией
2) пределом обнаружения
3) обнаруживаемым минимумом
4) предельное разбавление
В голубой цвет окрашены водные растворы солей … .
1) никеля(II) 2) кобальта(II) 3) меди(II) 4) железа(II)
Окрашенным является раствор, содержащий анион … .
1) ![]() 2)
2)![]() 3)
3) ![]() 4)
4)![]()
Признаком протекания качественной реакции между иодом и крахмалом является образование … .
1) коричневого осадка 2) жёлтой окраски
3) белого осадка 4) тёмно-синей окраски
Реагентом для обнаружения ионов аммония служит раствор … .
1) ВаСl2 2) NаОН 3) Fе(ОН)2 4) Н2SО4
Реагентом, используемым для идентификации ионов железа(III), является раствор … .
1) ![]() 2)
2)![]() 3)
3)![]() 4) KOH
4) KOH
При взаимодействии в растворе ионов железа(III) с гекса-цианоферратом(II) калия происходит образование … .
1) коричневого осадка 2) кроваво-красного раствора
3) светло-зелёного раствора 4) тёмно-синего осадка
При взаимодействии в растворе ионов железа(III) с роданидом калия наблюдается появление … .
1) коричневого осадка
2) кроваво-красной окраски
3) тёмно-синей окраски
4) жёлтого осадка
При добавлении в раствор соли железа(II) красной кровяной соли наблюдается образование … .
1) ярко-жёлтого осадка 2) кроваво-красного раствора
3) ярко-зелёного раствора 4) тёмно-синего осадка
Для обнаружения в водном растворе ионов Cu2+ можно использовать раствор … .
1) нитрата аммония 2) аммиака
3) сульфата аммония 4) хлорида аммония
При взаимодействии ионов
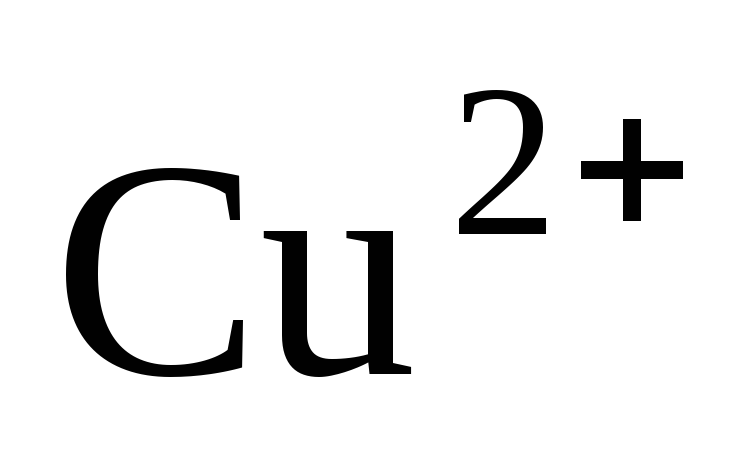 с избытком раствора аммиака наблюдается
появление … .
с избытком раствора аммиака наблюдается
появление … .
1) чёрного осадка 2) кроваво-красной окраски
3) белого осадка 4) ярко-синей окраски
Реагентом, используемым для обнаружения галогенид-ионов в растворе, является … .
1)
СН3СООАg
2)
![]()
3)
Аg2SО4
4)
![]()
Реагентом для качественного обнаружения сульфат-ионов в растворе служит … .
1) нитрат аммония 2) нитрат калия
3) нитрат натрия 4) нитрат бария
Ионы Ва2+ в растворе можно обнаружить в помощью … .
1) Н2S 2) Н2SО4 3) НNО3 4) СН3СООН
При обнаружении сульфат-ионов с помощью ионов бария происходит выпадение … осадка.
1) красного 2) белого
3) бурого 4) чёрного
Для качественного обнаружения карбонат-ионов используется раствор … .
1) сильной кислоты 2) средней соли
3) слабого основания 4) сильного основания
При взаимодействии карбонат-ионов с раствором сильной кислоты наблюдается … .
1) выделение пузырьков газа
2) появление синего окрашивания
3) образование белого осадка
4) образование жёлтого осадка
Пламя в фиолетовый цвет окрашивают атомы … .
1) кальция 2) калия 3) меди 4) натрия
Пламя в ярко-жёлтый цвет окрашивают ионы … .
1) Sr2+ 2) Сs+ 3) Сu2+ 4) Nа+
Пламя в красно-коричневый цвет окрашивают катионы … .
1) кальция 2) свинца(II) 3) бария 4) меди(II)
Пламя в ярко-зелёный цвет окрашивают ионы … .
1) Са2+ 2) Sr2+ 3) Сu2+ 4) Рb2+
