
- •Часть 1. Основы теории
- •1.0. Основные понятия и законы химии
- •Контрольные задания
- •1.1. Основные классы неорганических соединений
- •1.1.2. Основания
- •1.1.3. Амфотерные гидроксиды
- •1.1.4. Кислоты
- •1.1.5. Соли
- •Контрольные задания
- •1.2. Строение атома и периодический закон д. И. Менделеева
- •Контрольные задания
- •Химическая связь и строение молекул
- •Контрольные задания
- •1.4. Основные законы химических превращений
- •Контрольные задания
- •1.5. Растворы
- •Контрольные задания
- •1.5.1. Концентрация растворов
- •Контрольные задания
- •1.5.2. Гидролиз солей
- •Контрольные задания
- •1.6. Комплексные соединения
- •Контрольные задания
- •1.7. Реакции окисления-восстановления
- •Контрольные задания
- •Часть 2. Химия элементов
- •Контрольные задания
- •II. Кислые соли
- •III. Основные соли
1.5.1. Концентрация растворов
Методические советы
В химических расчетах используется в основном три вида концентрации:
— процентная концентрация показывает, сколько граммов растворенного вещества находится в 100 г раствора,
— молярная концентрация показывает, сколько молей растворенного вещества находится в 1 л (1000 мл) раствора,
— нормальная концентрация показывает, сколько молей эквивалентов растворенного вещества находится в 1 л (1000 мл) раствора.
При решении задач по переходу от одного вида концентрации к другому важно четко разграничить количество растворенного вещества и растворителя, массу и объем и т. д. Контролируется это согласованием единиц измерения в «столбиках» составляемых пропорций.
Количество растворенного вещества выражают в граммах mr , в молях nм, в молях эквивалентов nэ.
Количество раствора выражают в граммах G, в миллилитрах V.
Связь между этими величинами:
nm=![]() (1)
(1)
nэ=![]() .
(2),
.
(2),
где М и Э — молекулярная и эквивалентная масса соответственно.
ρ=![]() (3),
(3),
где ρ — плотность раствора.
Задачи на пересчет из одной концентрации в другую являются составным этапом большинства задач, включающих свойства растворов.
Контрольные задания
71-80. В соответствии с номером вашего задания заполните пропуски в таблице 8. Например, в задаче 76 надо найти молярную и нормальную концентрацию 10%-ного раствора СuSO4 (плотность раствора 1,1 г/мл).
Таблица 8
|
№ задания |
Растворенное вещество |
Концентрация раствора |
| ||
|
процента. |
молярная |
нор-мальн. |
Плотность раствора | ||
|
71 |
НNO3 |
10 |
|
|
1,05 |
|
72 |
НС1 |
|
1,2 |
|
1,02 |
|
73 |
NаОН |
5 |
|
|
1,05 |
|
74 |
Н3РO4 |
|
|
0,3 |
1,01 |
|
75 |
Н2SO4 |
|
0,4 |
|
1,027 |
|
76 |
СuSO4 |
10 |
|
|
принять 1,1 |
|
77 |
(NH4)2SO4 |
|
|
0,1 |
принять 1,0 |
|
78 |
КОН |
2 |
|
|
1,01 |
|
79 |
СНзСООН |
|
0,5 |
|
принять1,0
|
|
80 |
КNОз |
|
|
0,2 |
принять 1,0 |
1.5.2. Гидролиз солей
Методические советы
Ввиду особой важности гидролиза солей в регулировании биологических процессов следует четко отработать навыки написания уравнений гидролиза после проработки по учебнику.
Поставим себе задачу составления уравнений гидролиза только по первой ступени (наиболее реальной в обычных условиях). Рекомендуемая последовательность действий:
а) составить уравнения диссоциации соли;
б) выяснить, по какому иону идет гидролиз.
Это и есть сугубо химический аспект гидролиза. Здесь используются справочные данные для определения «слабости» электролита, таблица растворимости (приложение 2), таблица степеней диссоциации (приложение 3).
в) составить для этого иона уравнение реакции взаимодействия с водой (с одной молекулой, т.к. речь идет о первой ступени). Это уравнение и будет сокращенным ионным уравнением гидролиза, оно определяет наступающее в растворе равновесие и характеризуется собственной константой.
г) записать уравнение гидролиза в молекулярном виде. При этом в основу берется ионное уравнение (пункт в), а для составления нейтральных молекул используются противоионы из уравнения диссоциации соли (пункт а).
ПРИМЕР. Составить уравнение гидролиза сульфата меди.
а)
СuSO4=Сu2+
+![]() ;
(1)
;
(1)
б)
из приложений 3 выясняем, что иону Сu2+
соответствует слабое основание, а иону
![]() —
сильная кислота, значит, гидролиз идет
по катиону:
—
сильная кислота, значит, гидролиз идет
по катиону:
в)
Сu2+
+
Н2O![]() (СuОН)
+ +
Н+
(2)
(СuОН)
+ +
Н+
(2)
Естественно, что положительный ион Сu2+ «вырвет» из воды отрицательную часть ОН-. Заряд образовавшегося иона СuОН+ определяем суммированием зарядов Сu2+ и ОН-. Не забудьте, что связывание ионов ОН- ведет к избытку в растворе ионов Н+, что определит кислую реакцию среды.
Выражение для константы гидролиза имеет вид:
Kr=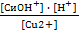 ;
;
г)
при составлении уравнения в молекулярной
форме констатируем,
что
всем положительным ионам уравнения (2)
соответствуют имеющиеся
в
свободном виде (уравнение 1) отрицательные
ионы ![]() .
С учетом
зарядов
ионов составляем электронейтральные
молекулы:
.
С учетом
зарядов
ионов составляем электронейтральные
молекулы:
СuSO4
+
Н2O
![]() (СuОН)
2SO4
+
Н2SO4,
(СuОН)
2SO4
+
Н2SO4,
а затем подбираем необходимые коэффициенты:
2СuSO4
+
2Н2O
![]() (СuОН)
2SO4
+
Н2SO4.
(СuОН)
2SO4
+
Н2SO4.
Напоминаем, что в растворе реально существуют ионы H3O+ а не Н+.
