
- •© ННГАСУ, 2003
- •1. Основы термодинамического и молекулярно-кинетического методов исследования
- •1.1. Исходные положения термодинамики и молекулярной физики
- •1.2. Масса и размеры молекул
- •1.3. Основные понятия термодинамики
- •Рис. 1.2. График равновесного цикла
- •1.4. Разреженный газ как термодинамическая система
- •1.4.1. Экспериментальные газовые законы
- •Рис. 1.4. График изобарического процесса в координатах {V,T}. Сплошная линия – процесс при давлении р1, пунктир соответствует процессу при давлении р2.
- •Рис. 1.5. График изохорического процесса в координатах {p,Т}. Сплошная линия – процесс при объеме V1, пунктир соответствует процессу при объеме V2.
- •Тренировочное задание
- •1.4.2. Уравнение состояния идеального газа
- •Ответы на вопросы тренировочного задания, сформулированные на стр. 11
- •От уравнения (1.7), записанного для одного моля газа
- •1.4.3. Примеры решения задач на уравнение состояния газа
- •Задача 1
- •Задача 2
- •Дано:
- •Дано:
- •1.5. Основное уравнение молекулярно-кинетической теории
- •Давление молекул на стенку сосуда. Давление согласно определению равно силе, с которой газ воздействует на площадку единичной площади, перпендикулярно площадке:
- •Величина суммарной силы воздействия молекул на площадку по III закону Ньютона равна суммарной силе, действующей на систему молекул со стороны площадки. Следовательно, сила может быть найдена по II закону Ньютона для системы материальных точек:
- •1.6. Замечание о средней квадратичной скорости. Распределение Максвелла молекул по скоростям
- •1.7. Закон равнораспределения энергии по степеням свободы. Внутренняя энергия идеального газа
- •1.8. Примеры решения задач
- •Задача 1
- •Задача 2
- •2. Термодинамический подход
- •2.1. Первое начало термодинамики
- •2.1.1. Работа, производимая термодинамической системой
- •Рис. 2.1. Схема вычисления работы при расширении газа
- •Рис. 2.2. Работа системы при ходе процесса
- •2.1.2. Количество теплоты и теплоемкость
- •2.1.3. Применение первого начала термодинамики к изопроцессам в идеальном газе
- •Для равновесных процессов, протекающих в газах, элементарная работа, производимая газом против внешних сил, состоит в работе расширения (2.1), поэтому первое начало термодинамики может быть записано в виде:
- •2.2. Адиабатический процесс
- •2.3. Второе начало термодинамики
- •2.3.1. Термодинамические циклы. Цикл Карно
- •2.3.2. Понятие об энтропии
- •3. Реальные газы. Фазовый переход жидкость - газ
- •3.1. Реальные газы. Уравнение Ван-Дер-Ваальса
- •3.2. Изотермы Эндрюса
- •3.3. Исследование уравнения Ван-Дер-Ваальса
- •3.4. Переход жидкости в пар
- •3.5. Примеры решения задач
- •Дано:
- •4. Зачетная контрольная работа № 2
- •4.1. Варианты домашних зачетных заданий
- •4.2. Приложение. Задачи, включенные в варианты зачетной контрольной работы № 2
- •Литература

|
|
15 |
|
|
|
|
|
Дано: |
|
|
Решение: |
|
|
|
|
|
|
|
|
|
|
||
Н2, |
|
|
Заметим, что объем баллона не меняется: |
||||
V=10л=10−2 м3 |
|
|
V2=V1. |
|
|
|
|
Т1=280К |
|
|
Запишем уравнение состояния утечки: |
||||
р1=5 103 Па |
|
|
p1V1 |
= m1 RT1 |
(1) |
||
Т2=287К, р2=р1 |
|
|
|
µ |
|
|
|
|
|
и для состояния 2 (после утечки): |
|||||
|
|
|
p2V2 |
= |
m2 |
RT2 |
(2) |
|
|
|
|||||
|
|
|
|
µ |
|
|
|
Поскольку p2=p1 V2=V1 (а |
|
значит, и p1V1=p2V2) из (1) и (2) следует: |
|||||
m1 |
RT1 |
= m2 RT2 , то есть m2 = m1 T1 . |
|
||||
µ |
|
µ |
|
T |
|
||
|
|
|
|
2 |
|
||
С другой стороны, масса m1 газа до утечки может быть найдена из (1):
m1 = µ p1V1 .
RT1
Следовательно, можно найти массу газа, покинувшего баллон ∆m=m1-m2:
T1 |
|
T1 |
|
|
p1V1 |
|
T1 |
|
|
|
|
|
|
|
|||||
∆m = m1 − m1 T |
− T |
= µ |
RT |
− T |
|||||
= m1 1 |
|
1 |
. |
||||||
2 |
|
2 |
|
|
1 |
|
2 |
|
Подставляя данные, получим
∆m = 2 10 |
−3 5 103 10−2 |
7 |
кг =1,05 10−6 кг. |
|
8,31 280 |
287 |
|||
|
|
1.5. Основное уравнение молекулярно-кинетической теории
Как следует из названия раздела, здесь мы отойдем на время от термодинамического метода и обратим внимание на статистический подход. Задача данного раздела - количественно объяснить давление газа на стенки сосуда как результат совместного действия молекул, составляющих газ. Вы также убедитесь на примере газа, что термодинамический и статистический подходы действительно дополняют друг друга, давая новую информацию. В частности, будет найдена связь средней кинетической энергии молекул газа с температурой.
Физическая модель идеального газа. В разделе 1 был оценен характерный размер d молекулы (на примере воды), который оказался равным 3 10−10 м. Там же говорилось, что несжимаемость воды, по-видимому, связана с тем, что молекулы практически касаются друг друга, то есть размер d сравним с расстоянием между центрами молекул. В газах это, по-видимому, не так, поскольку объем может сильно уменьшаться.
Оценим среднее расстояние dср между молекулами газа при нормальных
условиях. Согласно закону Авогадро 1 моль любого газа при нормальных условиях занимает объем 22,4 10−3 м3 /моль. Значит, на одну молекулу приходится объем в Na раз меньший:
V1 |
= |
22,4 10−3 |
м3 = 3,7 10−26 м3 . |
|
|
6 1023 |
|

16
Поскольку V1 dср , получим:
dср = 3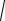 3,7 10−28 м3 3,3 10−9 м
3,7 10−28 м3 3,3 10−9 м
Таким образом, в газе среднее расстояние между молекулами на порядок больше характерного размера молекул: dср/d 10. Это обстоятельство позволяет принять следующую модель идеального газа:
1)Газ сильно разрежен, так что собственный объем молекул газа
Vмол Nаm/µ V1 существенно меньше объема сосуда, в котором находится газ (Vмол. < V).
2)Силами взаимодействия между молекулами такого разреженного газа можно пренебречь и учитывать взаимодействие только при столкновении молекул.
3)Столкновения молекул газа между собой и со стенками сосуда являются абсолютно упругими (молекулы - упругие шарики).
4)Молекулы газа совершают беспорядочное тепловое движение, т.е. направления скоростей ориентированы в пространстве совершенно беспорядочно. Это означает, что в каждом направлении в данный момент движется одинаковое число молекул, т.е. N/6, где N - полное число молекул газа (N/3 молекул движется параллельно каждой из осей координат, причем половина из них движется в положительном направлении, а другая - в противоположную сторону).
Давление молекул на стенку сосуда. Давление согласно определению равно силе, с которой газ воздействует на площадку единичной площади, перпендикулярно площадке:
p = ∆FS ,
где ∆S - площадь плоской площадки, например стенки сосуда.
Величина суммарной силы воздействия молекул на площадку по III закону Ньютона равна суммарной силе, действующей на систему молекул со стороны площадки. Следовательно, сила может быть найдена по II закону Ньютона для системы материальных точек:
F = ∆∆Pt ,
где P - суммарное изменение импульса всех молекул, сталкивающихся за время ∆t с площадкой ∆S.
Для того, чтобы вычислить ∆P, необходимо, во-первых, знать число молекул N', которые ударяются о площадку за малое время ∆t, и, во-вторых, изменение импульса каждой молекулы.
Если молекула массы m0 налетает в направлении, перпендикулярном площадке, со скоростью υ, то в результате абсолютно упругого удара с тяжелой площадкой (масса сосуда много больше массы молекулы) молекула отскочит с такой же скоростью в противоположном направлении (это известно из механики). То есть изменение импульса одной молекулы равно:
17
∆P1 = m0υ −(−m0υ) = 2m0υ .
Теперь необходимо вычислить число молекул N'. Сколько молекул столкнутся с площадкой за время ∆t? Это будут все молекулы, расположенные в объеме ∆V и летящие в направлении, перпендикулярном площадке. Значит, это составит 1/6 от всех молекул, содержащихся в объеме ∆V:
N ′ = 16 n∆V ,
где n - концентрация молекул газа, т.е. число молекул в единице объема.
Чем определяется объем ∆V? Это тот объем, из которого молекулы, движущиеся в сторону площадки, успевают ее достичь за время ∆t (см. рис.1.6). Значит, высота равна υ∆t, а основание - ∆S, что позволяет определить ∆V=∆S υ∆t и записать выражение для числа столкновений:
N ′ = 16 n∆Sυ∆t .
υ∆t
∆S
Рис. 1.6. Объем ∆V, из которого молекулы достигают площадки за время ∆t
Поэтому ∆P=2m0υt N'= 1 nm0υ2 |
∆S ∆t и окончательно получим: |
||||||
3 |
F |
|
|
∆P |
|
1 nm0υ2 . |
|
p = |
= |
= |
|||||
∆S |
∆t ∆S |
||||||
|
|
|
3 |
||||
Таким образом, мы получили формулу:
|
|
p = 1 nm0υ2 . |
(1.12) |
|
|
3 |
|
Используя понятие средней кинетической энергии теплового движения |
|||
молекул ε = |
1 m0υ2 |
, уравнение (1.12) можно записать в виде: |
|
|
2 |
p = 2 nε . |
|
|
|
(1.13) |
|
|
|
3 |
|
Это есть основное уравнение молекулярно-кинетической теории идеального газа,} которое означает:
давление в газе пропорционально средней энергии теплового движения молекул и числу молекул в единице объема.
