
тесты физика
.pdf№ |
|
|
|
Вопросы |
|
|
|
|
|
|
Варианты ответов |
|
||
243. |
Числом |
степеней |
свободы |
механической |
1. |
свободно вращающихся частей системы. |
||||||||
|
системы называется количество… |
|
2. |
независимых величин, с помощью |
||||||||||
|
|
|
|
|
|
|
|
|
которых может быть задано положение |
|||||
|
|
|
|
|
|
|
|
|
системы в пространстве. |
|
||||
|
|
|
|
|
|
|
|
|
3. |
независимых |
координатных |
осей в |
||
|
|
|
|
|
|
|
|
|
системе отсчета. |
|
|
|||
|
|
|
|
|
|
|
|
|
4. |
параметров, |
определяющих |
траекторию |
||
|
|
|
|
|
|
|
|
|
движения системы. |
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
244. |
На |
|
каждую |
степень |
свободы |
1. |
|
3 kT . |
|
|
||||
|
(поступательную, |
вращательную |
и |
|
|
2 |
|
|
|
|||||
|
колебательную) в среднем приходится |
|
|
|
|
|||||||||
|
|
|
1 |
|
|
|
||||||||
|
одинаковая кинетическая энергия, равная… |
2. |
|
kT . |
|
|
||||||||
|
2 |
|
|
|||||||||||
|
(Т – термодинамическая температура, k – |
|
|
|
|
|||||||||
|
|
|
i |
|
|
|
||||||||
|
постоянная Больцмана, i – число степеней |
3. |
|
kT . |
|
|
||||||||
|
2 |
|
|
|||||||||||
|
свободы) |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
4. |
kT . |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||
245. |
Трехатомная |
молекула идеального |
газа с |
1. |
3. |
|
|
|
||||||
|
жесткой связью обладает числом степеней |
2. |
1. |
|
|
|
||||||||
|
свободы, равным… |
|
|
|
|
3. |
5. |
|
|
|
||||
|
|
|
|
|
|
|
|
|
4. |
6. |
|
|
|
|
246. |
Двухатомная молекула идеального газа с |
1. |
3. |
|
|
|
||||||||
|
упругой связью обладает числом степеней |
2. |
7. |
|
|
|
||||||||
|
свободы равным… |
|
|
|
|
3. |
5. |
|
|
|
||||
|
|
|
|
|
|
|
|
|
4. |
6. |
|
|
|
|
|
3.1. Д. Молекулярно-кинетическая теория (дополнительные вопросы) |
|||||||||||||
247. |
Какие из параметров состояния являются |
1. |
Температура и давление. |
|
||||||||||
|
экстенсивными? |
|
|
|
|
2. |
Давление и объем. |
|
||||||
|
|
|
|
|
|
|
|
|
3. |
Объем и внутренняя энергия. |
|
|||
|
|
|
|
|
|
|
|
|
4. Давление и внутренняя энергия. |
|||||
248. |
При |
|
каком |
процессе |
|
молярная |
1. |
При изотермическом процессе. |
||||||
|
теплоёмкость газа равна нулю? |
|
2. |
При изохорическом процессе. |
|
|||||||||
|
|
|
|
|
|
|
|
|
3. |
При адиабатическом процессе. |
||||
|
|
|
|
|
|
|
|
|
4. При политропическом процессе. |
|||||
249. |
Для |
идеального |
газа |
|
коэффициент |
1. |
0,4. |
|
|
|||||
|
Пуассона приблизительно равен |
|
2. |
1,4. |
|
|
||||||||
|
|
|
|
|
|
|
|
|
3. |
1,67. |
|
|
||
|
|
|
|
|
|
|
|
|
4. |
5,33. |
|
|
||
250. |
Метод |
Стокса для экспериментального |
1. |
скорости падающих в жидкости шариков. |
||||||||||
|
определения |
вязкости |
основан |
на |
2. |
объема вытекающей жидкости и времени |
||||||||
|
измерении… |
|
|
|
|
|
ее вытекания через тонкий капиляр. |
|||||||
|
|
|
|
|
|
|
|
|
3. |
силы, действующей на движущееся в |
||||
|
|
|
|
|
|
|
|
|
жидкости тело. |
|
|
|||
|
|
|
|
|
|
|
|
|
4. |
силы Архимеда, действующей на |
||||
|
|
|
|
|
|
|
|
|
движущееся в жидкости тело. |
|
||||
251. |
Из |
закона |
распределения |
Больцмана |
1. |
больше их кинетическая энергия. |
||||||||
|
следует, что молекулы располагаются с |
2. |
меньше их потенциальная энергия. |
|||||||||||
|
большей концентрацией там, где … |
|
3. |
больше их потенциальная энергия. |
||||||||||
|
|
|
|
|
|
|
|
|
4. больше их средняя скорость. |
|
||||
41
№ |
|
|
Вопросы |
|
Варианты ответов |
|
||||
252. |
Какой |
из |
графиков |
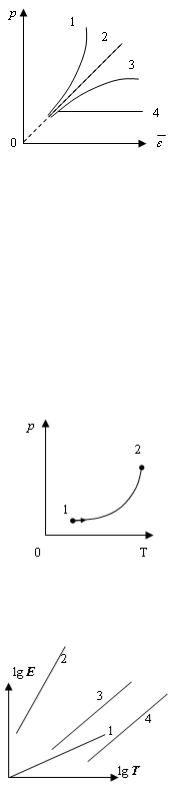
верно отражает |
1. |
1. |
|
|
||
|
взаимосвязь давления р и средней |
2. |
2. |
|
|
|||||
|
кинетической энергии |
поступательного |
3. |
3. |
|
|
||||
|
|
|
при их постоянной |
4. |
4. |
|
|
|||
|
движения молекул |
|
|
|||||||
|
концентрации в сосуде с идеальным газом? |
|
|
|
|
|||||
|
|
|
|
|||||||
253. |
Коэффициент вязкости в законе Ньютона |
1. |
удельный поток импульса при градиенте |
|||||||
|
для силы вязкого трения характеризует… |
скорости равном единице. |
|
|||||||
|
|
|
|
|
|
|
2. |
поток импульса при изменении скорости на |
||
|
|
|
|
|
|
|
единицу. |
|
|
|
|
|
|
|
|
|
|
3. |
импульс силы, проходящий через единицу |
||
|
|
|
|
|
|
|
поверхности при градиенте скорости равном |
|||
|
|
|
|
|
|
|
единице. |
|
|
|
|
|
|
|
|
|
|
4. |
силу, действующую на тело, движущееся в |
||
|
|
|
|
|
|
|
жидкости. |
|
|
|
254. |
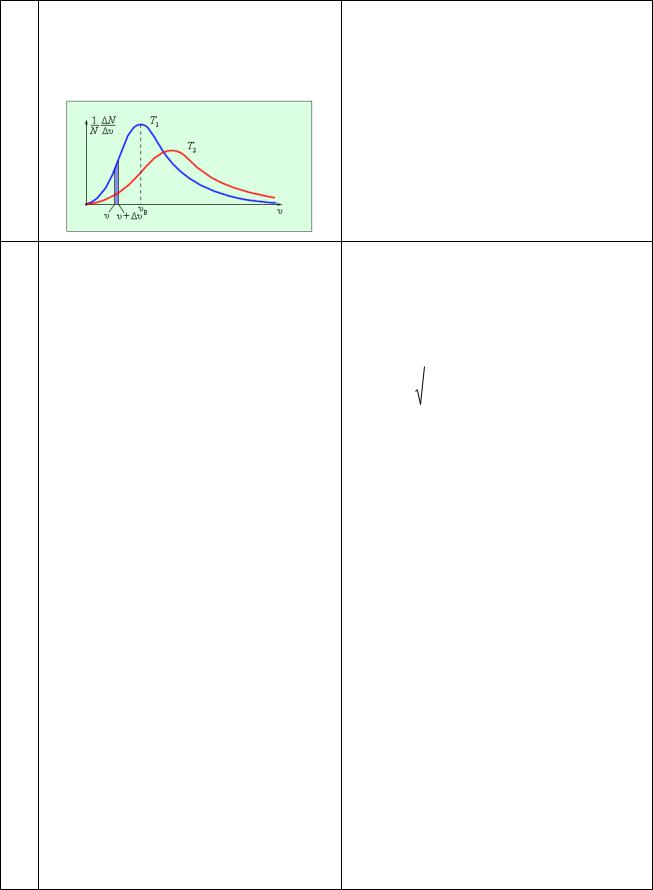
Идеальный газ (число частиц постоянно) |
1. |
Увеличивается. |
|
|
|||||
|
переходит из состояние 1 в состояние 2. |
2. |
Сначала |
увеличивается, |
потом |
|||||
|
Как меняется в этом процессе объем, |
уменьшается. |
|
|
||||||
|
занимаемый газом? |
|
3. |
Уменьшается. |
|
|
||||
|
|
|
|
|
|
|
4. |
Сначала |
уменьшается, |
потом |
|
|
|
|
|
|
|
увеличивается. |
|
|
|
|
|
|
|
|
|
|
|
|||
255. |
Какая |
из |
представленных на рисунке |
1. |
1. |
|
|
|||
|
прямых отражает правильную зависимость |
2. |
2. |
|
|
|||||
|
средней |
кинетической |
энергии молекул |
3. |
3. |
|
|
|||
|
газа Е от температуры T газа? |
4. |
4. |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
42

№ |
|
|
|
Вопросы |
|
|
|
Варианты ответов |
||
256. |
В |
равных |
объемах при одинаковых |
1. |
азот, углекислый газ, метан. |
|||||
|
температурах |
и |
давлении |
|
содержатся |
2. |
метан, углекислый газ, азот. |
|||
|
метан, азот и углекислый газ. Какому газу |
3. |
углекислый газ, азот, метан. |
|||||||
|
соответствуют прямые 1, 2, 3 на графике |
4. |
метан, азот, углекислый газ. |
|||||||
|
зависимости полной кинетической энергии |
|
|
|||||||
|
Ек |
от |
|
кинетической |
|
энергии |
|
|
||
|
поступательного движения Еп. |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
257. |
Коэффициент Пуассона |
cp |
… |
1. |
больше 1. |
|||||
|
2. |
меньше 1. |
||||||||
|
cv |
|||||||||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
3. |
равен 1,4. |
|
|
(ср |
– удельная |
теплоемкость |
газа при |
||||||
|
4. |
не зависит от температуры газа. |
||||||||
|
постоянном давлении, сV |
– |
удельная |
|||||||
|
|
|
||||||||
|
теплоемкость при постоянном объеме) |
|
|
|||||||
|
|
|
|
|
|
|||||
258. |
При |
адиабатическом |
расширении |
1. |
не изменяется. |
|||||
|
температура газа … |
|
|
2. |
плавно возрастает. |
|||||
|
|
|
|
|
|
|
|
|
3. |
уменьшается. |
|
|
|
|
|
|
|
|
|
4. |
в начале процесса – возрастает, в конце – |
|
|
|
|
|
|
|
|
|
убывает. |
|
259. |
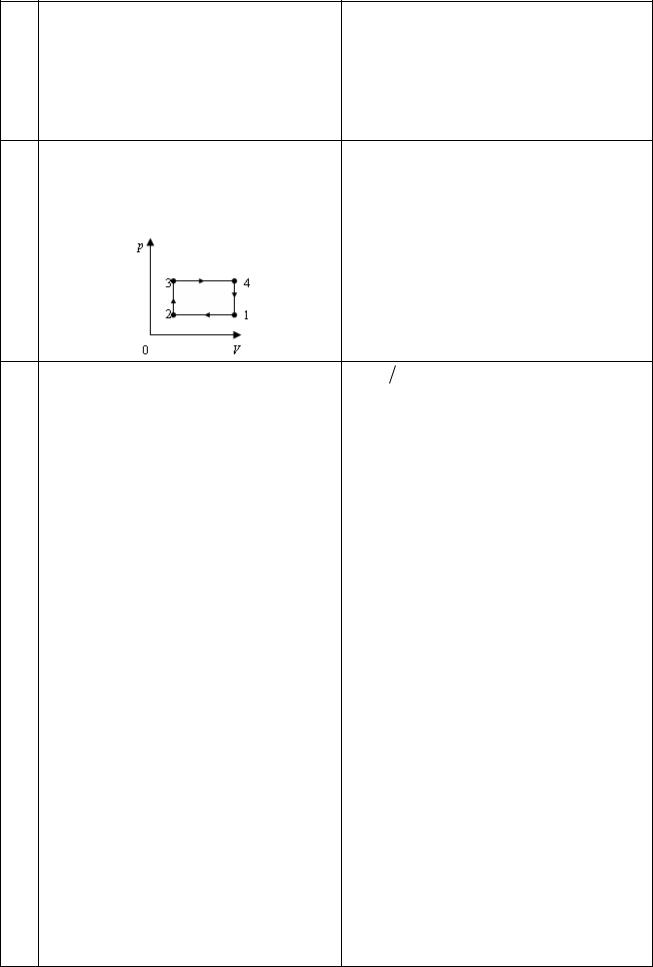
Какая из предоставленных на рис. прямых |
1. |
(1). |
|||||||
|
правильно |
|
изображает |
зависимость |
2. |
(2). |
||||
|
логарифма средней квадратичной скорости |
3. |
(3). |
|||||||
|
молекул газа υ от логарифма температуры |
4. |
(4). |
|||||||
|
Т? |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
260. |
Одинаковые |
|
|
количества |
|
теплоты |
1. |
Наиболее высокая у Ar, наиболее низкая |
||
|
сообщены одинаковым массам аргона, |
у СО2. |
||||||||
|
кислорода и углекислого газа. У какого |
2. |
Наиболее высокая у Ar, наиболее низкая |
|||||||
|
газа в результате этого процесса будет |
у О2. |
||||||||
|
достигнута наиболее высокая температура, |
3. |
Наиболее высокая у О2, наиболее низкая |
|||||||
|
а у какого газа наиболее низкая? |
у СО2. |
||||||||
|
Процесс |
изохорический, |
|
начальные |
4. |
Наиболее высокая у О2, наиболее низкая |
||||
|
температуры одинаковы. |
|
|
у Ar. |
||||||
|
|
|
|
|
|
|
|
|
|
|
43
№ |
Вопросы |
|
|
Варианты ответов |
261. |
На рисунке показаны распределения |
1. |
T1 |
T2 . |
|
Максвелла молекул идеального газа по |
2. |
T1 |
T2 – распределение не зависит от |
|
скоростям при двух температурах T1 и T2 . |
|||
|
температуры. |
|||
|
При этом… |
3. |
|
º |
|
|
температура газа больше 0 С. |
||
|
|
4. |
T1 |
T2 . |
262. Если |
p0 |
– нормальное атмосферное |
|
|
p p0 e |
Mgh |
|
|
|
||||||||||||||||
|
давление, g – ускорение свободного |
1. |
|
RT |
. |
|
|
|
|||||||||||||||||
|
падения, M – молярная масса газа, R – |
2. |
|
p p0 |
ln( |
|
Mgh |
) . |
|||||||||||||||||
|
универсальная газовая |
постоянная, |
Т |
– |
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
термодинамическая |
|
температура, |
|
то |
|
|
|
|
|
|
|
|
|
|
RT |
|
|
|
||||||
|
|
|
|
|
p p0 |
|
Mgh |
|
|
|
|
|
|||||||||||||
|
давление газа над уровнем моря на высоте |
3. |
|
|
. |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
h |
можно |
найти |
по барометрической |
|
|
|
|
|
|
RT |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
Mgh |
|
|
|
||||||||||||||
|
формуле: |
|
|
|
|
|
4. |
|
p p0 |
|
|
. |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
RT |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
263. |
Какая из скоростей молекул газа: средняя |
1. |
Наибольшая – средняя арифметическая, |
||||||||||||||||||||||
|
арифметическая, среднеквадратическая или |
наименьшая – среднеквадратическая. |
|||||||||||||||||||||||
|
наивероятнейшая – наибольшая и какая |
2. |
Наибольшая – среднеквадратическая, |
||||||||||||||||||||||
|
наименьшая при данной температуре? |
|
|
наименьшая – средняя арифметическая. |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
3. |
Наибольшая – среднеквадратическая, |
|||||||||||||||
|
|
|
|
|
|
|
|
|
наименьшая – наивероятнейшая. |
||||||||||||||||
|
|
|
|
|
|
|
|
|
4. |
Наибольшая – наивероятнейшая, |
|||||||||||||||
|
|
|
|
|
|
|
|
|
наименьшая – средняя арифметическая. |
||||||||||||||||
264. |
Отношение теплоёмкости при постоянном |
1. |
|
i 3 . |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
давлении к теплоёмкости при постоянном |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
объёме Cp/CV равно… |
|
|
|
2. |
|
2i |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
(i |
– |
число |
степеней |
свободы молекулы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
идеального газа, NA – число Авогадро). |
|
|
|
i 1 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
i 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
3. |
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
4. |
|
i N A |
. |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
i 2 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
265. |
Для двухатомного газа с жесткой связью |
1. |
i = 1; U m 3 RT . |
||||||||||||||||||||||
|
между атомами число степеней свободы i и |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
M 2 |
||||||||||||||
|
внутренняя энергия U массы m газа |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
i = 2; U |
m |
|
5 |
|
|
||||||||||||||||||
|
соответственно равны… |
|
|
2. |
|
RT . |
|||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||
|
(M |
|
– молярная |
масса газа, |
R |
– |
|
|
|
|
|
|
|
|
|
|
M 2 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
m 5 |
|||||||||||||
|
универсальная газовая |
постоянная, |
Т |
– |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
3. |
i = 5; U M 2 RT . |
|||||||||||||||||||||||
|
термодинамическая температура) |
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
7 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
4. |
i = 6; U |
|
RT . |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M 5 |
||||||
44
№ |
Вопросы |
|
Варианты ответов |
266. |
При увеличении температуры вязкость… |
1. жидкости увеличивается, а у газа |
|
|
|
уменьшается. |
|
|
|
2. |
жидкости уменьшается, а у газа |
|
|
увеличивается. |
|
|
|
3. |
жидкости и газа уменьшается. |
|
|
4. |
жидкости и газа увеличивается. |
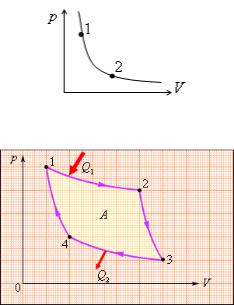
267.В какой из точек циклического процесса, 1. 1. изображенного на p-V-диаграмме, средняя 2. 4.
квадратичная скорость молекул идеального |
3. |
2. |
газа максимальна? (Число молекул газа |
4. |
3. |
постоянно). |
|
|
268. Какая |
из |
зависимостей |
следует |
из |
1. |
CV |
C p R . |
||||
определения показателя адиабаты? |
|
2. |
C p |
CV . |
|||||||
Ср, СV – молярные теплоёмкости при |
|||||||||||
3. |
C p CV |
. |
|||||||||
постоянном давлении и объёме, R – |
|||||||||||
универсальная газовая постоянная. |
|
4. |
C p CV . |
||||||||
|
|
|
|
|
|||||||
269. В сосуде неизменного объема находится |
1. |
Уменьшить в 2 раза. |
|||||||||
идеальный газ в количестве 2 моль. |
|
2. |
Увеличить в 4 раза. |
||||||||
Как |
надо |
изменить |
абсолютную |
3. |
Уменьшить в 4 раза. |
||||||
температуру сосуда с газом при выпуске из |
4. |
Увеличить в 2 раза. |
|||||||||
сосуда 1 моля газа, чтобы давление газа на |
|
|
|
|
|
|
|||||
стенки сосуда увеличилось в 2 раза? |
|
|
|
|
|
|
|
||||
270. При неизменной средней энергии молекул |
1. |
Давление увеличилось, температура не |
|||||||||
уменьшилась концентрация молекул. Как |
изменилась. |
||||||||||
при этом изменились температура и |
2. |
Давление уменьшилось, температура |
|||||||||
давление газа? |
|
|
повысилась. |
||||||||
|
|
|
|
|
3. |
Давление уменьшилось, температура не |
|||||
|
|
|
|
|
изменилась. |
||||||
|
|
|
|
|
4. |
Давление не изменилось, температура |
|||||
|
|
|
|
|
повысилась. |
||||||
271. Показатель политропы n равен: |
|
1. |
0. |
|
|
|
|||||
(C – теплоёмкость системы CV |
– |
2. |
|
(C CV ) . |
|||||||
теплоёмкость при постоянном объёме. Ср – |
|
|
(C Cp ) |
|
|||||||
теплоёмкость при постоянном давлении). |
|
|
|
(Cp ) |
|
|
|||||
|
|
|
|
|
3. |
|
. |
|
|||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
(CV ) |
|
||||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
4. |
|
(C Cp ) |
. |
|||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
(C C ) |
|||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
V |
|
|
272. При изобарном процессе концентрация |
1. |
не изменилась. |
|||||||||
идеального газа увеличилась в 9 раз. |
2. |
увеличилась в 9 раз. |
|||||||||
Средняя кинетическая энергия молекул |
3. |
уменьшилась в 9 раз. |
|||||||||
данной массы газа … |
|
|
4. |
увеличилась в 3 раза. |
|||||||
45
№ |
Вопросы |
|
Варианты ответов |
||
|
3.2. Б. Основы термодинамики (базовые вопросы) |
|
|||
273. |
Первый закон термодинамики: количество |
1. изменение внутренней энергии системы и |
|||
|
теплоты, сообщенное системе, идет на… |
ее теплоемкости. |
|
|
|
|
|
2. |
увеличение её внутренней энергии и |
||
|
|
совершение работы против внешних сил. |
|||
|
|
3. |
изменение |
внутренней |
энергии |
|
|
окружающей среды и совершение внешними |
|||
|
|
силами работы над системой. |
|
||
|
|
4. |
возникновение |
разности |
потенциалов, |
|
|
приводящей к перемещению заряда из одной |
|||
|
|
точки пространства в другую. |
|
||
|
|
|
|
||
274. |
Из второго начала термодинамики следует, |
1. энтропия изолированной |
|
||
|
что … |
термодинамической системы может только |
|||
|
|
возрастать. |
|
|
|
|
|
2. |
энтропия изолированной |
|
|
|
|
термодинамической системы постоянна. |
|||
|
|
3. |
энтальпия изолированной |
|
|
|
|
термодинамической системы может только |
|||
|
|
убывать. |
|
|
|
|
|
4. |
энтропия изолированной |
|
|
|
|
термодинамической системы может только |
|||
|
|
убывать. |
|
|
|
275. |
Третье начало термодинамики утверждает |
1. любого тела остается постоянной в ходе |
|||
|
что энтропия… |
необратимого процесса. |
|
||
|
|
2. |
любого тела стремится к нулю при |
||
|
|
стремлении термодинамической |
|||
|
|
температуры к нулю. |
|
||
|
|
3. |
изолированной системы в равновесном |
||
|
|
состоянии максимальна. |
|
||
|
|
4. |
изолированной системы возрастает в ходе |
||
|
|
необратимого процесса. |
|
||
|
|
|
|
||
276. |
Если в некотором процессе работа |
1. изотермическим. |
|
||
|
совершённая газом равна подведённому к |
2. |
изохорическим. |
|
|
|
газу теплу, то такой процесс является… |
3. |
политропическим. |
|
|
|
|
4. |
адиабатическим. |
|
|
|
|
|
|||
277. |
Теорема Нернста: энтропия…. |
1. изолированной системы в равновесном |
|||
|
|
состоянии максимальна. |
|
||
|
|
2. |
любого тела уменьшается при увеличении |
||
|
|
термодинамической температуры. |
|||
|
|
3. |
изолированной системы возрастает в ходе |
||
|
|
необратимого процесса. |
|
||
|
|
4. |
любого тела стремится к нулю при |
||
|
|
стремлении термодинамической |
|||
|
|
температуры к нулю. |
|
||
|
|
|
|
|
|
46
№ |
|
|
Вопросы |
|
|
|
|
|
|
|
|
|
Варианты ответов |
||||||||||||||||||||
|
3.2. Д. Основы термодинамики (дополнительные вопросы) |
||||||||||||||||||||||||||||||||
278. |
Газ массой |
m |
с |
молярной |
массой |
М |
1. |
Q = A; |
A |
m |
|
RT |
V V |
. |
|||||||||||||||||||
|
участвует в изотермическом процессе, при |
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
2 |
|
|
1 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
температуре Т, |
в котором ему передается |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
Q > A; A |
m |
|
|
|
V V |
. |
|||||||||||||||||||||||||
|
теплота Q, а |
газ |
совершает |
работу |
А, |
2. |
RT |
||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
2 |
|
|
1 |
||||||||||||
|
увеличивая свой объем от V1 |
до V2. При |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
V |
|
|
|||||||||||||
|
этом: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
3. |
Q = A; |
A |
|
|
|
|
|
|
|
|
RT ln |
2 |
|
. |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V1 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
V |
|
|
||||||
|
|
|
|
|
|
|
|
4. |
Q < A; |
A |
|
|
|
|
|
|
|
|
RT ln |
2 |
|
. |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V1 |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
279. |
Величина, |
|
которая |
характеризует |
1. масса макросостояния. |
|
|
|
|||||||||||||||||||||||||
|
количество микросостояний, посредством |
2. |
молярная масса макросостояния. |
||||||||||||||||||||||||||||||
|
которых |
осуществляется |
данное |
3. |
статистический вес макросостояния. |
||||||||||||||||||||||||||||
|
макросостояние, называется… |
|
|
4. |
логарифм статистического веса. |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
280. |
Какая из перечисленных величин не |
1. |
Статистический вес макросостояния. |
||||||||||||||||||||||||||||||
|
является аддитивной величиной? |
|
2. |
Логарифм статистического веса. |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
3. |
Масса. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
4. |
Молярная масса. |
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
281. |
При изохорическом процессе изменение |
1. |
S m R ln V2 . |
|
|
|
|
|
|
||||||||||||||||||||||||
|
энтропии S равно … |
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
V1 |
|
|
|
|
|
|
|
||||||||||
|
(m – масса, М – молярная масса, V1, T1 и V2, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
2. |
0. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
T2 – начальные и конечные объемы и |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
m |
|
|
|
|
|
|
|
|
T2 |
|
|
|
|
|
|
|
||||||||||||
|
температуры, |
|
соответственно, СV |
– |
3. |
S |
|
C ln |
. |
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
M |
V |
|
T1 |
|
|
|
|
|
|
||||||||||||
|
молярная теплоемкость |
при |
постоянном |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
объеме, R – универсальная газовая |
4. |
S |
3 m |
|
R . |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
постоянная) |
|
|
|
|
|
|
2 |
|
M |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||
282. |
Приведенным |
|
количеством |
теплоты |
1. отношение теплоты, полученной телом в |
||||||||||||||||||||||||||||
|
называется … |
|
|
|
|
|
|
изотермическом |
|
|
процессе |
к температуре |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
теплоотдающего тела. |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
2. |
количество теплоты на единицу массы. |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
3. |
количество теплоты на один Кельвин. |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
4. |
количество теплоты, полученное за одну |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
секунду (в СИ). |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||
283. |
Выражение |
для |
изменения |
энтропии |
1. необратимый процесс в изолированной |
||||||||||||||||||||||||||||
|
dS 0 описывает… |
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
2. |
необратимый процесс в неизолированной |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
3. |
обратимый процесс в изолированной |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
4. |
обратимый процесс в неизолированной |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
47
№ |
|
|
Вопросы |
|
|
|
|
Варианты ответов |
||||
284. |
Выражение |
для |
изменения |
энтропии |
1. |
необратимый процесс в изолированной |
||||||
|
dS 0 описывает… |
|
|
|
системе. |
|
|
|
||||
|
|
|
|
|
|
|
|
2. |
необратимый процесс в неизолированной |
|||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
3. |
обратимый процесс в изолированной |
|||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
4. |
обратимый процесс в неизолированной |
|||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
285. |
Обратимый |
процесс |
в неизолированной |
1. |
dS d Q . |
|||||||
|
системе |
описывает |
выражение |
для |
|
|
T |
|
||||
|
изменения энтропии … |
|
|
|
|
|||||||
|
|
|
2. |
dS = 0. |
||||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
3. |
dS |
d Q |
. |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
T |
||
|
|
|
|
|
|
|
|
4. |
dS |
d Q |
. |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
T |
||
286. |
Энтропия |
термодинамической |
системы |
1. |
хаоса в термодинамической системе. |
|||||||
|
является мерой… |
|
|
|
|
2. |
инертности в термодинамической |
|||||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
3. |
беспорядка в термодинамической |
|||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
|
|
|
|
|
|
|
|
4. |
взаимодействия в термодинамической |
|||
|
|
|
|
|
|
|
|
системе. |
|
|
|
|
287. |
Точки 1 и 2 лежат на одной адиабате. В |
1. |
Температура и энтропия больше в точке 2. |
|||||||||
|
каком из состояний, 1 или 2, выше |
2. |
Температура выше в точке 1, энтропия |
|||||||||
|
температура и больше энтропия? |
|
|
одинакова в обеих точках. |
||||||||
|
|
|
|
|
|
|
|
3. |
Температура выше в точке 2, энтропия |
|||
|
|
|
|
|
|
|
|
больше в точке 1. |
||||
|
|
|
|
|
|
|
|
4. |
Температура выше в точке 2, энтропия |
|||
|
|
|
|
|
|
|
|
одинакова в обеих точках. |
||||
|
|
|
|
|
|
|
|
|||||
288. |
Цикл |
Карно |
в |
координатах |
p – V |
1. |
две изотермы и две изохоры. |
|||||
|
содержит… |
|
|
|
|
|
2. |
две изохоры и две адиабаты. |
||||
|
|
|
|
|
|
|
|
3. |
две изотермы и две изобары. |
|||
|
|
|
|
|
|
|
|
4. |
две адиабаты и две изотермы. |
|||
|
|
|
|
|
|
|||||||
289. |
К.п.д. идеальной |
тепловой машины |
при |
1. |
возрастает. |
|||||||
|
повышении температуры холодильника … |
2. |
убывает. |
|||||||||
|
|
|
|
|
|
|
|
3. |
не изменяется. |
|||
|
|
|
|
|
|
|
|
4. |
возрастает, только если в работе |
|||
|
|
|
|
|
|
|
|
участвует идеальный газ. |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
48

№ |
Вопросы |
|
Варианты ответов |
290. |
Если в некотором процессе подведённая к |
1. |
изохорическим. |
|
газу теплота равна изменению его |
2. |
изотермическим. |
|
внутренней энергии, то есть Q = U, то |
3. |
политропическим. |
|
такой процесс является… |
4. |
адиабатическим. |
291. |
Если в некотором процессе газ совершает |
1. изохорическим. |
|
|
работу за счёт подведённой к газу теплоты |
2. |
политропическим. |
|
при неизменной внутренней энергии, то |
3. |
изотермическим. |
|
такой процесс является… |
4. |
адиабатическим. |
3.3. Б. Реальные газы, жидкости, твёрдые тела (базовые вопросы)
292. |
|
|
|
а |
|
|
|
1. |
описывает поведение идеальных газов. |
||
|
Уравнение |
Р |
|
|
|
V b RT |
, |
|
2. |
описывает поведение реальных газов |
|
|
V |
2 |
|
||||||||
|
|
|
|
|
|
|
|
3. |
является уравнением переноса энергии. |
||
|
|
– |
константы; P, V, |
T, |
– |
||||||
|
где: ( а ,b |
|
4. |
описывает поведение вязких жидкостей. |
|||||||
|
давление, объем, температура, количество |
||||||||||
|
|
|
|||||||||
|
вещества газа; R – универсальная газовая |
|
|
||||||||
|
постоянная). |
|
|
|
|
|
|
|
|
||
293. |
Сжижение газа … |
|
|
|
|
1. |
не возможно. |
||||
|
|
|
|
|
|
|
|
|
|
2. |
возможно при температуре ниже |
|
|
|
|
|
|
|
|
|
|
критической. |
|
|
|
|
|
|
|
|
|
|
|
3. |
возможно при температуре выше |
|
|
|
|
|
|
|
|
|
|
критической. |
|
|
|
|
|
|
|
|
|
|
|
4. |
возможно при любой температуре. |
3.3. Д. Реальные газы, жидкости, твёрдые тела(дополнительные вопросы)
294. |
Поведение |
реальных |
газов |
описывает |
|
|
|
2 |
|
b |
|||||
|
уравнение…. |
|
|
|
|
1. |
Р / а V |
1 |
|
T . |
|||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
R |
|||
|
( à , b – |
соответствующие |
поправки, |
|
|
|
|
|
|
||||||
|
2. |
Р а V b RT . |
|||||||||||||
|
включённые в уравнение идеального газа; |
||||||||||||||
|
|
|
|
|
а |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
P, V, T, – давление, объем, температура, |
3. |
|
Р |
|
|
|
V b RT . |
|||||||
|
|
|
|
||||||||||||
|
количество |
вещества |
газа; |
R |
– |
|
|
V 2 |
|
|
|
||||
|
универсальная газовая постоянная). |
|
4. |
Р а V V b RT . |
|||||||||||
|
|
|
|
|
|
|
|
|
|||||||
295. |
Идеальный |
газ |
при |
адиабатическом |
1. |
охлаждается. |
|
|
|||||||
|
расширении в вакуум… |
|
|
|
2. |
нагревается. |
|
|
|||||||
|
|
|
|
|
|
|
3. |
не изменяет своей температуры. |
|||||||
|
|
|
|
|
|
|
4. |
испаряется. |
|
|
|||||
296. |
Выберете правильное выражение для |
1. |
|
T < 0, Tин > 0. |
|||||||||||
|
изменения температуры реальных газов в |
2. |
|
T < 0, |
Tин = 0. |
||||||||||
|
положительном |
эффекте Джоуля |
– |
3. |
|
T > 0, |
Tин < 0. |
||||||||
|
Томсона |
и |
температуры |
инверсии |
4. |
|
T = 0, |
Tин = 0. |
|||||||
|
соответственно. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
297. |
Выберете правильное выражение для |
1. |
|
T < 0, T > 0. |
|
|
|||||||||
|
изменения температуры реальных газов в |
2. |
|
T > 0, |
T < 0. |
||||||||||
|
отрицательном эффекте Джоуля – Томсона |
3. |
|
T > 0, |
T = 0. |
||||||||||
|
и температуры инверсии соответственно. |
|
4. |
|
T = 0, |
T = 0. |
|||||||||
298. |
При температуре инверсии коэффициент |
1. |
равен нулю. |
|
|
||||||||||
|
Джоуля – Томсона … |
|
|
|
2. |
меньше нуля. |
|
|
|||||||
|
|
|
|
|
|
|
3. |
больше нуля. |
|
|
|||||
|
|
|
|
|
|
|
4. |
равен единице. |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
49
№ |
|
|
|
|
Вопросы |
|
|
|
|
|
|
|
|
|
|
|
|
Варианты ответов |
|||
299. |
На диаграмме состояния вещества, кривые |
1. тройной точке. |
|
|
|||||||||||||||||
|
испарения и сублимаций заканчиваются в |
2. |
тройной и критической точке |
||||||||||||||||||
|
… |
|
|
|
|
|
|
|
соответственно. |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
3. |
критической и тройной точке |
|||||||||||
|
|
|
|
|
|
|
|
|
соответственно. |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
4.. критической точке. |
|
|
||||||||||
300. |
При адиабатическом расширении в вакуум, |
1. |
охлаждается. |
|
|
||||||||||||||||
|
реальный газ… |
|
|
|
|
2. |
нагревается. |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
3. |
не изменяет своей температуры. |
|||||||||||
|
|
|
|
|
|
|
|
|
4. |
испаряется. |
|
|
|||||||||
301. |
При адиабатическом сжатии в вакуум, |
1. |
охлаждается. |
|
|
||||||||||||||||
|
реальный газ… |
|
|
|
|
2. |
нагревается. |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
3. |
не изменяет своей температуры. |
|||||||||||
|
|
|
|
|
|
|
|
|
4. |
испаряется. |
|
|
|||||||||
302. |
Молярная |
теплоёмкость |
химически |
1. |
зависит от температуры и равна 3R/T. |
||||||||||||||||
|
простых |
|
тел |
в |
кристаллическом |
2. |
не зависит от температуры и равна R/3T. |
||||||||||||||
|
состоянии… |
|
|
|
|
3. |
зависит от температуры и равна 3RT. |
||||||||||||||
|
|
|
|
|
|
|
|
|
4. |
не зависит от температуры и равна 3R. |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЧАСТЬ 2 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
1.Электростатика |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
1.1.Б. Основные характеристики и свойства электрических зарядов и |
||||||||||||||||||||
|
|
|
|
электростатических полей (базовые вопросы) |
|
|
|||||||||||||||
1. |
Сила |
|
электростатического |
взаимодей- |
|
|
q1q2 |
|
|
|
|
|
|
||||||||
|
ствия |
между двумя точечными зарядами |
1. |
k |
|
r 2 . |
|
|
|||||||||||||
|
F |
|
|
|
|||||||||||||||||
|
q1 и |
q2, |
взаимное положение которых |
|
|
|
q1q2 |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
2. |
|
|
. |
|
|
|
|
|||||
|
определяется |
радиус-вектором |
r , |
|
|
k r |
2 |
|
|
|
|
||||||||||
|
вычисляется по формуле (k – коэффициент |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
q q |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
||||
|
пропорциональ-ности): |
|
|
|
3. |
|
k |
|
|
1 |
|
|
r . |
|
|
||||||
|
|
|
|
|
|
r3 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
4. |
|
k |
q1q2 |
. |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
r3 |
|
|
|
|
|
||
2. |
Заряд металлической сферы увеличили в 9 |
1. увеличилась в 3 раза. |
|
|
|||||||||||||||||
|
раз. Напряженность поля, создаваемая |
2. увеличилась в 9 раз. |
|
|
|||||||||||||||||
|
зарядом в центре сферы… |
|
|
|
3. не изменилась. |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
4. |
увеличилась в некоторое число раз, |
|||||||||||
|
|
|
|
|
|
|
|
|
|
зависящее от радиуса сферы. |
|||||||||||
3. |
Линии |
|
напряженности |
электрического |
1. линии, |
|
которые в любой точке совпадают |
||||||||||||||
|
поля - это… |
|
|
|
|
|
по |
|
|
|
|
|
направлению |
с |
градиентом |
||||||
|
|
|
|
|
|
|
|
|
|
напряженности поля. |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
2. |
линии, перпендикуляры к которым в |
|||||||||||
|
|
|
|
|
|
|
|
|
|
каждой точке совпадают по направлению с |
|||||||||||
|
|
|
|
|
|
|
|
|
|
вектором напряженности поля. |
|||||||||||
|
|
|
|
|
|
|
|
|
3. |
линии, касательные к которым совпадают |
|||||||||||
|
|
|
|
|
|
|
|
|
|
с |
направлением вектора |
напряженности |
|||||||||
|
|
|
|
|
|
|
|
|
|
электрического поля. |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
4. |
линии, которые охватывают заряды. |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
50
