
- •1. Основные классы неорганических соединений. Номенклатура
- •1.1. Оксиды
- •1.2. Гидроксиды
- •1.3. Кислоты
- •1.4. Соли
- •1.5. Задачи для решения
- •2. Строение атома
- •1S2s2p3s3p4s3d4p5s4d5p6s5d1(La)4f (лантаноиды)5d6p7s6d1(Ac)5f(актиноиды)6d…
- •2.1. Примеры решения задач
- •2.2. Задачи для решения
- •4. Основные понятия и законы химии
- •4.1. Моль, молярная масса
- •4.2. Основные газовые законы
- •4.3. Закон эквивалентов
- •4.4. Примеры решения задач
- •4.5. Задачи для решения
- •5. Растворы
- •5.1. Концентрации растворов
- •5.1.1. Примеры решения задач
- •5.1.2. Задачи для решения
- •Задачи на приготовление раствора
- •5.2. Коллигативные свойства растворов
- •5.2.1. Закон Рауля
- •5.2.2. Изменение температур фазовых переходов растворов
- •5.2.3. Осмотическое давление
- •5.2.4. Примеры решения задач
- •5.2.5. Задачи для решения
- •5.3. Водородный показатель
- •5.3.1. Расчет рН в растворах сильных кислот и оснований
- •5.3.2. Расчет рН в растворах слабых кислот и оснований
- •5.3.3. Примеры решения задач
- •5.3.4. Задачи для решения
- •5.4. Гидролиз
- •Соль образована одним слабым электролитом
- •5.4.1. Примеры решения задач
- •5.4.2. Задачи для решения
- •5.5. Равновесия в буферных растворах
- •5.5.1. Примеры решения задач
- •5.5.2. Задачи для решения
- •5.6. Равновесия в насыщенных растворах
- •5.6.1. Растворимость в бинарной системе соль - вода
- •5.6.2. Растворимость в многокомпонентной системе с одноименными ионами
- •5.6.3. Условия образования осадков
- •5.6.4. Примеры решения задач
- •5.6.5. Задачи для решения
- •6.Окислительно-восстановительные реакции
- •6.1. Примеры решения задач
- •6.2. Задачи для решения
- •Приложение 1
- •Приложение 2
- •Приложение 3
- •Оглавление
5.2.5. Задачи для решения
Определить осмотическое давление раствора глицерина в воде, содержащего 30 г глицерина в 120 г воды, если плотность этого раствора близка к единице, температура 27С.
Определить осмотическое давление раствора хлорида натрия в воде концентрацией 5 %, если плотность раствора 1,04 г/см3, температура 17С, кажущаяся степень диссоциации 95 %.
К 100 мл 0,5 М водного раствора сахарозы С12Н22О11добавлено 300 мл воды. Чему равно осмотическое давление полученного раствора при 25С?
При 293 Kдавление насыщенного пара над водой равно 2,34 кПа. Сколько граммов глицерина С3Н5(ОН)3надо растворить в 180 г воды, чтобы понизить давление пара на 133,3 Па?
При растворении 13 г неэлектролита в 400 г диэтилового эфира (С2Н5)2О температура кипения раствора повысилась на 0,453K. Определить молярную массу растворенного вещества.
В 60 г бензола растворено 2,09 г некоторого вещества, элементарный состав которого С – 50,69 %, Н – 4,23 %, О – 45,08 %. Установить молекулярную формулу вещества. Чистый бензол кристаллизуется при 5,5С.
Температура кипения водного раствора сахарозы С12Н22О11равна 101,4С. Вычислить молярную концентрацию и массовую долю сахарозы в растворе. При какой температуре замерзает этот раствор?
Определить осмотическое давление раствора хлорида бария в воде, если его концентрация 5 %, плотность 1,08 г/см3, температура 7С, кажущаяся степень диссоциации 97 %.
Определить кажущуюся степень диссоциации хлорида калия в его 0,1 н. водном растворе, если при температуре 27С осмотическое давление раствора составляет 4,72105Па.
Осмотическое давление гипертонического раствора (водный раствор хлорида натрия концентрацией 10 %) при температуре 20С составляет 84105Па. Определить кажущуюся степень диссоциации соли в этом растворе, если его плотность 1,1 г/см3.
Определить концентрацию раствора сульфата натрия в воде и выразить ее всеми способами, если известно, что осмотическое давление раствора при температуре 15С составляет 32,5105Па, кажущаяся степень диссоциации 91 %.
Водный раствор соли хрома (III) имеет осмотическое давление 18,1105Па, плотность раствора 1,06 г/см3. Определить концентрацию раствора и выразить ее всеми способами, если соль диссоциирована нацело.
Сколько граммов хлорида кальция надо растворить в одном литре воды, чтобы полученный раствор при температуре 27С имел осмотическое давление, равное 23,7105Па? Кажущаяся степень диссоциации 95 %.
Сколько граммов сульфата меди (II) надо растворить в 100 мл воды, чтобы при температуре 7С полученный раствор имел осмотическое давление равное 16105Па, кажущаяся степень диссоциации 87 %?
Определить концентрацию хлорид-ионов в растворе хлорида ртути (II), если при температуре 17С и концентрации раствора 0,1 моль/л осмотическое давление его составляет 2,62105Па.
Раствор роданида железа (III) в воде с концентрацией 0,5 моль/л при температуре 27С имеет осмотическое давление 15,5105Па. Определить концентрацию роданид-ионов в данном растворе.
Определить давление паров воды над раствором хлорида натрия концентрацией 5 %, если температура раствора 20С, кажущаяся степень диссоциации 98 %,
 =2,3105Па.
=2,3105Па.Определить молярную концентрацию раствора карбамида, если при температуре 35С давление паров воды над раствором оказалось на 2 % ниже, чем над индивидуальной водой (
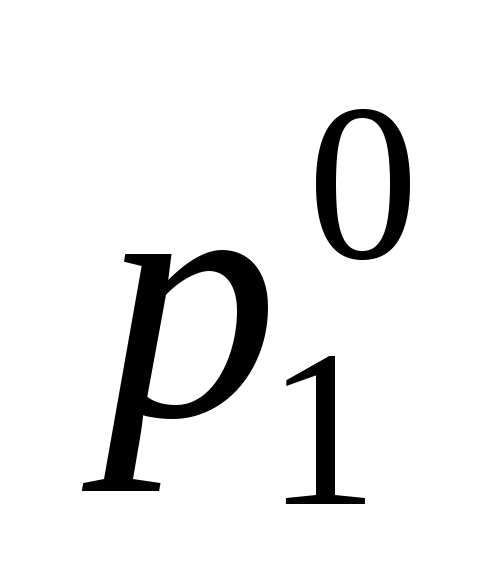 =5,55105Па).
Карбамид в водных растворах не
диссоциирует.
=5,55105Па).
Карбамид в водных растворах не
диссоциирует.Определить кажущуюся степень диссоциации сульфата калия в его водном растворе концентрацией 3 %, если относительное понижение давления паров воды над раствором составляет 9,23103.
Определить давление паров воды над 0,5 % раствором хлорида бария при 15С, если кажущаяся степень диссоциации составляет 96 %,
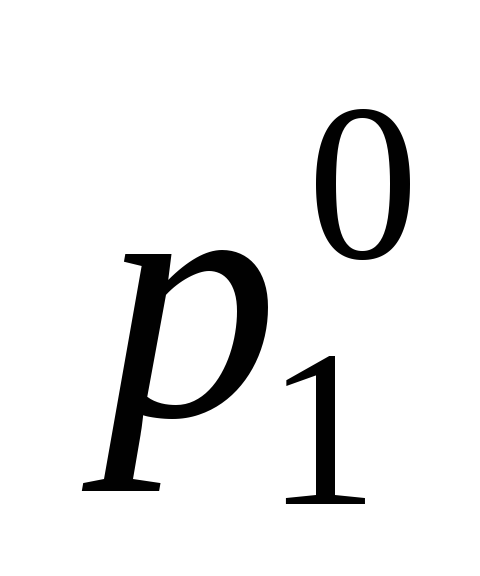 =
1,683105Па.
=
1,683105Па.Определить концентрацию сульфата цинка в водном растворе, если относительное понижение давления пара над этим раствором составляет 0,1 %, соль диссоциирована нацело.
Какова концентрация хлорида алюминия в растворе, если относительное понижение давления пара над раствором составляет 0,16 %, степень диссоциации соли – 100 %?
Осмотическое давление раствора хлорида натрия при температуре 20С составляет 8,4105па. Определить давление паров воды над этим раствором, если плотность раствора 1,05 г/см3, кажущаяся степень диссоциации соли 92 %,
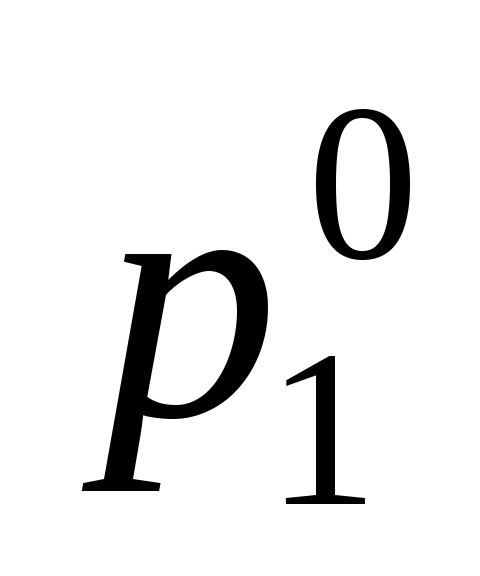 =2,31103Па.
=2,31103Па.Раствор хлорида калия в воде имеет осмотическое давление 9,44105Па. Определить давление паров воды над этим раствором, если его температура 27С, плотность раствора 1,07 г/см3, кажущаяся степень диссоциации соли 92 %,
 =3,5105Па.
=3,5105Па.Определить давление паров воды над раствором глицерина С3Н5(ОН)3, если в 100 г воды растворено 20 г глицерина, плотность раствора 1,1 г/см3,
 =1,95105Па.
=1,95105Па.Определить концентрацию раствора сульфата натрия в воде, если при температуре 22С давление паров воды над этим раствором составляет 2,61103Па, кажущаяся степень диссоциации 95,7 %,
 =2,62103Па.
=2,62103Па.При какой температуре закипит водный раствор хлорида меди (II) концентрацией 2 %, если кажущаяся степень диссоциации 97 %?
Определить температуру кипения раствора сульфата натрия в воде, если при 27С раствор этой соли имеет осмотическое давление 7,16105Па, плотность 1,06г/см3, кажущаяся степень диссоциации 96 %.
Какой должна быть концентрация раствора хлорида цинка в воде, чтобы этот раствор закипал при температуре 100,52С? Соль диссоциирована на 100 %. Выразить концентрацию раствора всеми способами (плотность раствора 1,04 г/см3).
Определить кажущуюся степень диссоциации нитрата натрия, если этот раствор кипит при температуре 100,1С, а в 100 г воды растворено 0,85 г соли.
Раствор хлорида алюминия в воде концентрацией 0,2 моль/кг кипит при температуре 100,406С.определить осмотическое давление этого раствора при температуре кипения, если его плотность 1,06 г/см3.
В 100 г воды содержится 0,58 г хлорида натрия. При какой температуре закипит этот раствор, если кажущаяся степень диссоциации 96 %?
Определить кажущуюся степень диссоциации бромида калия растворе концентрацией 2 %, если он закипает при 100,17С.
Определить эбуллиоскопическую постоянную этилового спирта, если известно, что раствор, содержащий 0,506 г йодноватой кислоты в 31,8 г этанола кипит при температуре 78,464С. В данных условиях кислота диссоциирована на 32,6 %, а температура кипения чистого этанола 78,3С.
Определить относительное понижение давления водяного пара над раствором хлорида кобальта (II), если при кажущейся степень диссоциации 93 % данный раствор кипит при температуре 100,30С.
Определить, сколько граммов глицерина надо добавить к 100 г воды, чтобы получившийся раствор не замерзал до температуры -3,2С.
При какой температуре начнется кристаллизация воды из раствора хлорида калия концентрацией 3 %, если кажущаяся степень диссоциации 89 %?
Определить кажущуюся степень диссоциации сульфата магния в его 0,1 н. растворе плотностью 1,02 г/см3, если этот раствор начинает кристаллизоваться при температуре -0,153С.
При какой температуре начнет кристаллизоваться раствор сульфата железа (II) концентрацией 2 %, если его температура кипения 100,136С?
При какой температуре закипит раствор глицерина в воде, если он кристаллизуется при температуре -1,5С?
Кажущаяся степень диссоциации некоторой соли, диссоциирующей на три иона, составляет 97 %. Определить при какой температуре начнет кристаллизоваться раствор этой соли в воде, если он закипает при температуре 100,2С.
Относительное понижение давления паров воды над раствором сульфата калия концентрацией 3 % составляет 9,23103. Определить при какой температуре начнется кристаллизация воды из этого раствора.
Раствор хлорида калия в воде концентрацией 0,8 % плотностью 1,02 г/см3при температуре 27С имеет осмотическое давление 5,13105Па. Определить при какой температуре начнется кристаллизация этого раствора.
Температура кристаллизации бензола составляет +5,5С, а раствора, содержащего 0,2242 г камфары в 30,55 г бензола+5,254С. Определить молярную массу камфары, если для бензола константа кристаллизации составляет 5,16Kкгмоль1.
Раствор некоторого органического вещества в этиловом спирте закипает при температуре 78,41С. Определить его молярную массу ,если для приготовления раствора было взято 2 г этого вещества, 48 г этилового спирта, температура кипения которого 78,3С,Kэб=1,19 Ккгмоль-1.
Сколько граммов хлористого натрия надо добавить к 100 г воды, чтобы получившийся раствор не замерзал до температуры -1,8С? Считать, что соль диссоциировала на 100%.
Сколько сахара С12Н22О11надо растворить в 200 г воды, чтобы полученный раствор кипел при температуре 100,3С?
Сколько граммов хлорида бария, диссоциирующего нацело, надо растворить в одном литре воды, чтобы получившийся раствор замерзал при температуре -3,2С?
Осмотическое давление раствора глицерина в воде при температуре 7С составляет 5,3105Па. Определить при какой температуре закипит этот раствор, если его плотность 1,02 г/см3.
Определить степень диссоциации бензойной кислоты С6Н5СООН, если раствор ее в бензоле кристаллизуется при температуре +5,32С. Температура кристаллизации индивидуального бензола +5,5С,Kкр=5,16 Ккгмоль1, а для приготовления раствора взято 62,5 г бензола и 0,26 г бензойной кислоты.
Определить молярную массу бензойной кислоты, если известно, что ее раствор в бензоле кристаллизуется при температуре +5,18С. Для бензолаТкрист=5,5С,Kкр=5,16 Ккгмоль1, а для приготовления раствора взято 100 г бензола и 0,757 г бензойной кислоты. Считать, что в растворе кислота практически не диссоциирована.
При какой температуре закипит раствор иодида калия в воде, если для его приготовления взято 300 мл воды и 1,33 г соли, кажущаяся степень диссоциации 98 %?
Относительное понижение давления паров воды над раствором некоторой соли составляет 1 %. Определить, при какой температуре закипит этот раствор.
Относительное понижение давления паров над раствором некоторого сильного электролита в воде составляет 1,5 %. Определить, при какой температуре начнется кристаллизация этого раствора.
Раствор, в 100 мл которого находится 2,3 г вещества, обладает при 298 К осмотическим давлением, равным 618,5 кПа. Определить молярную массу вещества.
В одном миллилитре раствора содержится 1018молекул растворенного неэлектролита. Вычислить осмотическое давление раствора при 298 К.
В каком отношении должны находиться массы воды и этилового спирта, чтобы при их смешении получить раствор, замерзающий при 20С?
При 25С осмотическое давление некоторого водного раствора равно 1,24 МПа. Вычислить осмотическое давление раствора при 0С.
