
- •18. Ароматические углеводороды (арены). Строение бензола. Номенклатура. Способы получения. Химические свойства: реакции замещения, окисления, присоединения.
- •19. Механизм электрофильного замещения в ароматическом ядре. Реакции электрофильного замещения: сульфирование, нитрование, алкилрование, ацилирование, галогенирование.
- •21. Нитроалканы и нитроарены. Строение нитрогруппы. Получение. Химические свойства. Применение.
- •22. Амины и ароматические и алифатические. Влияние строения аминов на их основность. Получение. Получение анилина. Химические свойства аминов. Отдельные представители и их применение.
- •23. Карбоновые кислоты. Номенклатура. Строение. Способы получения карбоновых кислот. Химические свойства. Механизм этерификации. Отдельные представители и их применение.
- •24. Двухосновные карбоновые кислоты. Способы получения. Химические свойства. Отдельные представители и их применение.
- •25. Ароматические одно – и двухосновные кислоты (бензойная и фталевые кислоты). Способы получения. Химические свойства. Отдельные представители и их применение.
- •26. Непредельные кислоты. Номенклатура, изомерия, строение и способы получения, химические свойства. Применение. Отдельные представители. Акриловые и метакриловые кислоты.
- •27. Фуран. Получение, строение, химические свойства. Применение.
- •Строение
- •Получение фурана
- •Химические свойства
- •Применение
- •Применение
- •29. Пиррол. Получение, строение, химические свойства. Применение.
- •Строение
- •Получение
- •Химические свойства
- •Применение
- •30. Шестичленные гетероциклы с одним гетероатомом. Пиридин. Получение, строение и химические свойства. Применение. Строение
- •Получение
- •Химические свойства
- •Применение пиридина
- •31. Соединения со смешанными функциями. Оксокислоты. Номенклатура, изомерия, строение, способы получения, химические свойства. Применение. Отдельные представители.
- •32. Соединения со смешанными функциями. Гидроксикислоты. Номенклатура, изомерия (структурная и оптическая), строение и способы получения, химические свойства. Применение. Отдельные представители.
- •33. Производные карбоновых кислот. Сложные эфиры и амиды. Номенклатура, изомерия, строение и способы получения, химические свойства. Применение. Отдельные представители.
- •34. Производные карбоновых кислот. Ангидриды и галогенангидриды. Номенклатура, изомерия, строение и способы получения, химические свойства. Применение. Отдельные представители.
Применение пиридина
Пиридин и его производные - основа пиридиновых алкалоидов, а также многих лекарственных средств. Используют пиридин также в синтезе красителей, инсектицидов, применяют для денатурации спирта. Комплекс пиридин с SO3-пиридинсульфотриоксид - мягкий сульфирующий агент; C5H5NBr2· HBr - бромирующий агент; C5H5N · HCl - реагент для дегидратации эпоксидов и N-дезалкилирования, C5H5N · H2Cr2O7 - окислитель. пиридин - хороший растворитель, в том числе для многих неорганических солей (AgBr, Hg2Cl2 и др.).
31. Соединения со смешанными функциями. Оксокислоты. Номенклатура, изомерия, строение, способы получения, химические свойства. Применение. Отдельные представители.



Номенклатура:
Некоторые оксокислоты сохранили свои тривиальные названия, другие рациональные названия. По номенклатуре ИЮПАК названия оксокислот производят от названий соответствующих карбоновых кислот добавлением приставки оксо-.
Ацетоуксусная к-та (3-оксобутановая кислота), пировиноградная (2-оксопропановая) кислота, щавелевоуксксная (2-оксобутандиовая) кислота.
Изомерия: изомерия положения 2-х функциональных групп, альдегидо и кетокислоты.
Соединения,
содержащие карбоксильную и карбонильную
(альдегидную или кетонную) группы. В
соответствии с взаимным расположением
этих групп в молекуле различают![]() и
т.д. оксокарбоновые кислоты. Эти кислоты
сильнее соответствующих алканкарбоновых,
причем самые сильные-
и
т.д. оксокарбоновые кислоты. Эти кислоты
сильнее соответствующих алканкарбоновых,
причем самые сильные-![]() -оксокислоты.
Оксокислоты вступают в реакции,
характерные для групп СООН и СО.
-оксокислоты.
Оксокислоты вступают в реакции,
характерные для групп СООН и СО.
Альдегидная группа под влиянием соседней карбоксильной легко присоединяет нуклеофильные реагенты, в частности с Н2О образуется прочный гидрат (НО)2СНСООН. Превращается в щавелевую и гликолевую кислоты в результате диспропорционирования:
2НС(О)СООН → НООССООН + НОСН2СООН.
Применяется в производстве душистых (в т.ч. ванилина) и лекарственных веществ, красителей, для расщепления оксимов и гидразонов кетонов.
![]() Кетокислоты
получают окислением
Кетокислоты
получают окислением![]() гидроксикислот.
Важнейшая из них -пировиноградная
гидроксикислот.
Важнейшая из них -пировиноградная![]() кетопропионовая)
СН3СОСООН.
Может быть получена перегонкой винной
кислоты над KHSO4,
из ацетилхлорида или 2,2-дихлорпропионовой
кислоты.
кетопропионовая)
СН3СОСООН.
Может быть получена перегонкой винной
кислоты над KHSO4,
из ацетилхлорида или 2,2-дихлорпропионовой
кислоты.

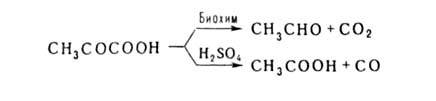
Легко отщепляет СО2 или СО:
α-КЕТОКИСЛОТЫ ПОЛУЧАЮТ ГИДРОЛИЗОМ α- α-дигалогенкарбоновых кислот:

Окислением α-гидроксикислот

Для![]() и
и![]() альдегидо-
и кетокислот характерны кето-енольная
(как для ацетоуксусного эфира) и
кольчато-цепная таутомерия, напр.:
альдегидо-
и кетокислот характерны кето-енольная
(как для ацетоуксусного эфира) и
кольчато-цепная таутомерия, напр.:

Левулиновая
кислота не отщепляет самопроизвольно
СО2.
Как и др.![]() оксокислоты,
при нагревании с водоотнимающими
средствами превращается в изомерные
непредельные
оксокислоты,
при нагревании с водоотнимающими
средствами превращается в изомерные
непредельные![]() лактоны (бутенолиды):
лактоны (бутенолиды):

Альдегидо- и кетокислоты обладают свойствами, присущими соединениям, содержащие эти функциональные группы в отдельности.
Кетокислота вступает в реакции по карбонильной группе, характерные для кетонов (нуклеофильное присоединение, гидрирование), по карбоксильной группе( ионизация, образование эфиров, амидов и т.д.)
Оксокислоты являются болле сильными ОН-кислотами, чем уксусная и пропионовая.
Пировиноградная кислота (СН3СОСООН) (α-кетопропионовая) – бесцветная жидкость, t пл=13,6, кип=165, растворима в воде, эфире, спирте. Применяется в производстве лекарственных веществ (цинкофена).
Ацетоуксусная кислота (β-кетомаслянная) вязкая жидкость, смешивается с водой, растворима в спирте, эфире.
Левулиновая кислота(γ-кетокислота CН3COCH2CH2COOH) Применяется в производстве лекарственных средств, в гальванотехнике при хромировании, как флюс для пайки.
