
физика_ часть 1
.pdf
6.4. Измерительное устройство поляриметра
Прибор предназначен для определения концентрации растворов оптиче-
ски активных веществ. Определение концентрации сводится к определению уг-
ла поворота плоскости поляризации исследуемым раствором.
Рис. 5.8. Измерительная шкала поляриметра
На рис. 5.8 показана измерительная шкала поляриметра. Слева ос-
новная шкала (от 0 до 3600), справа неподвижная шкала нониуса.
На примере измерительной системы поляриметра произведем расчет це-
ны деления по формуле (5.1)
Для нониуса nн =25; Сш=0,5. Тогда Cн |
|
nн 1 |
|
25 1 |
0,5 0,48 |
|
25 |
||||
|
|
nн |
|
||
Цена деления отсчета такого устройства (5.2)
С0=Сш - Сн=0,50-0,48=0,020
Задание к лабораторной работе
1.Измерьте с помощью штангенциркуля стороны бруска. Для каждой сто-
роны проведите не менее 8 измерений. Результаты измерений занесите в таблицу:
71

Экспериментальные и расчетные данные
n |
hi |
h |
hi |
( |
h |
hi )2 |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
….. |
|
|
|
|
|
|
8 |
|
|
|
|
|
|
2.Вычислить абсолютную и относительную погрешности прямых измере-
ний сторон.
3.Вычислить средний объем бруска.
4.Вычислить абсолютную и относительную погрешности косвенных изме-
рений объема бруска.
5.Запишите доверительный интервал измерений объема.
РАБОТА № 7. ИДЕНТИФИКАЦИЯ ВЕЩЕСТВ ПО ПЛОТНОСТИ С ПОМОЩЬЮ ПИКНОМЕТРА
Актуальность работы:
Денситометрия – физический метод анализа, основанный на определении плотности вещества. Плотность характеризует инерционные и гравитационные свойства вещества и является одной из важнейших физических констант. При исследовании лекарственных веществ по величине плотности можно иденти-
фицировать подлинность лекарственных препаратов.
Цель работы:
Изучить способ определения плотности твердого тела, нерастворимого в данной жидкости; освоить метод определения плотности пикнометром.
Целевые задачи:
знать: нахождение плотности однородного и неоднородного тела, зависи-
мость плотности от температуры.
72
уметь: определять плотность твёрдого тела, имеющего неправильные гео-
метрические формы (рассыпчатого) и нерастворимого в воде с помощью пикнометра, определять плотность неизвестной жидкости.
План подготовки конспекта:
1.Основные теоретические сведения
2.Выяснить, что измеряется в лабораторной работе, каким методом и для
чего.
2.Подготовить таблицы.
3.Записать расчётные формулы.
Вопросы для подготовки к входному тестированию:
1.Как найти плотность однородного и неоднородного тела?
2.Как зависит плотность от температуры?
3.В чём заключается метод определения плотности твёрдого тела,
имеющего неправильные геометрические формы (рассыпчатого) и нераствори-
мого в воде с помощью пикнометра?
4. В чём заключается метод определения плотности неизвестной жидко-
сти?
Теоретические сведения
Денситометрия - физический метод анализа, основанный на определении плотности вещества. Плотность характеризует инерционные и гравитационные свойства вещества и является одной из важнейших физических констант. При исследовании лекарственных веществ по величине плотности можно иденти-
фицировать подлинность лекарственных препаратов.
Плотностью однородного тела называется физическая величина, равная отношению массы тела m к его объёму V:
|
m |
(6.1) |
|
V
В СИ плотность измеряется в кг/м 3.
73

В неоднородных телах плотность различных его участков различна. По-
этому расчет плотности неоднородного вещества по указанной формуле не правомочен. Выберем в таком теле малый объём V, внутри которого тело можно считать практически однородным. Тогда средняя плотность выбранного
объёма будет равна m . Переходя к пределу, получим плотность тела в вы-
V
бранной точке:
lim |
m |
|
dm |
. |
|
|
|||
V 0 V |
dV |
|||
Для большинства веществ составлены таблицы плотности для температу- |
||||
ры 200С. При определении плотности различных веществ, с целью их иденти-
фикации, не обязательно доводить температуру до 200С. Плотность вещества определяют при температуре исследуемого объекта, а затем используют фор-
мулу объемного теплового расширения твердых и жидких тел, по которой объ-
ем тела V при температуре t 0 С, равен:
V=V0 (1 t0 ),
где V0 - начальный объём при температуре t0 0С; - коэффициент объем-
ного расширения, t 0 = t0 - t00 .
Следовательно, зависимость плотности от температуры можно записать в виде:
|
m |
|
V0 0 |
|
0 |
, где –плотность при t0 . |
|
|
|
|
|||||
V V0 (1 t) |
|
1 t |
0 |
0 |
|||
|
|
|
|||||
7.2. Определение плотности твердого тела опытным путем
Приборы и принадлежности:
- пикнометр, аналитические весы, разновесы, термометр, пипетки, ис-
следуемые жидкость и твердое тело; - дистиллированная вода.
Рассмотрим методику определения плотности твердого тела, нераствори-
мого в данной жидкости, с помощью пикнометра. Пикнометр - стеклянная кол-
74
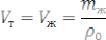
бочка с определенным объёмом (чаще это 25 мл или 50 мл), снабженная при-
тертой пробкой и имеющая метку на горлышке (см. рис. 6.1).
Чтобы определить плотность твердого тела, используя формулу (6.1), нужно знать массу исследуемого тела m и его объём V. Массу твердого тела можно определить взвешиванием на аналитических весах, но исследуемое тело может иметь неправильные геометрические размеры и определение его объёма путем измерений весьма проблематично. Поэтому объём тела определяют косвенным путем, основываясь на законе Архимеда, используя пикнометр. Объем тела равен объему вытесненной им жидкости, который можно найти по формуле:
где ρ0-плотность жидкости, mж- масса вытесненной твердым телом жид-
кости, равная
mж=Мпв+m-Mп
Объем тела определим расчетным путем: V |
|
V |
выт |
|
Мпв m Мпв |
. |
||
|
|
|||||||
|
Т |
|
|
|
|
0 |
||
|
|
|
|
|
|
|
||
Тогда, подставляя в формулу (6.1) выражения для объема и массы твер- |
||||||||
дого тела получим расчетную формулу для плотности твердого тела: |
||||||||
|
|
0 |
m |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мпв m Мпв
7.3.Порядок выполнения работы
I. Определение плотности твердого тела, нерастворимого в воде.
1.Измерить температуру дистиллированной воды и из справочных таблиц
найти плотность воды 0.
2. Определить взвешиванием массу m, выбранных для анализа кусочков твер-
дого тела.
3.Определить массу сухого и чистого пикнометра Мп.
4.Аккуратно, чтобы не осталось капель на стенках горлышка внутри пикно-
метра, наполнить пикнометр жидкостью до метки и взвесить Мпв.
75
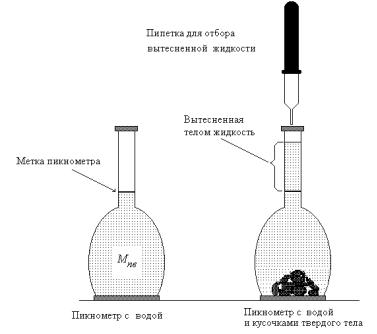
5. Поместить в пикнометр кусочки исследуемого твердого тела, встряхивая,
удалить пузырьки воздуха. Пипеткой удалить воду, вытесненную телом, до метки на пикнометре. Пикнометр с оставшейся водой и твердыми телами взве-
сить Мпвт.
Рис. 6.1
6.Все опыты провести для трех разных по массе тел m1, m2, m3.
7.Результаты измерений занести в таблицу
8.Провести статистическую обработку результатов измерений.
Результаты измерений
№ п/п |
m |
M п |
М пв |
Мпвт |
|
|
|
|
|
|
|
1. |
|
|
|
|
|
|
|
|
|
|
|
2. |
|
|
|
|
|
|
|
|
|
|
|
3. |
|
|
|
|
|
|
|
|
|
|
|
76

II. Определение плотности жидкости
Используя сделанные выше рассуждения, выведете формулу для опреде-
ления плотности жидкости.
Массы пустого пикнометра М п и пикнометра с водой М пв возьмем из предыдущих опытов.
Масса воды в пикнометре mв= Мпв – Мпв (6.2)
Обозначим через М ж массу пикнометра с исследуемой жидкостью, тогда по аналогии с (6.2), масса исследуемой жидкости:
m ж = М ж - М п .
Используем формулу (6.1), откуда объём воды: V в = |
mв |
, а объём иссле- |
|||||||||||
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
о |
|
дуемой жидкости: Vж |
|
mж |
. Так как объёмы воды и исследуемой жидкости |
||||||||||
|
|||||||||||||
|
|
|
ж |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
равны V в = V ж , то: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
m |
и ж |
m |
|
. |
||
|
|
|
|
|
в |
|
ж |
о |
ж |
||||
|
|
|
|
|
|
|
m |
|
|||||
|
|
|
|
|
о |
|
ж |
|
в |
|
|
|
|
Выполнение работы
Заполните пикнометр исследуемой жидкостью до метки, взвесьте и зане-
сите в таблицу значение М ж. Опыт повторить трижды.
Таблица 2
№ п/п |
М п |
М пв |
М ж |
|
1.
Примечание: значения М п и Мпв взять из первого опыта.
77
РАБОТА № 8. ОПЫТНОЕ ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ТЕПЛОЕМКОСТЕЙ ГАЗА
Актуальность работы:
Коэффициент Пуассона – это отношение теплоёмкости газа при постоян-
ном давлении к теплоёмкости газа при постоянном объёме. Эта величина зави-
сит от числа степеней свободы газа и является одной из характеристик газа.
Цель работы:
Определение отношения теплоемкостей газа (коэффициент Пуассона) ме-
тодом Клемана-Дезорма.
Целевые задачи:
знать: уравнение Менделеева-Клайперона, изопроцессы, определение теп-
лоёмкости, теплоёмкости газов в любом изопроцессе
уметь: определять отношения теплоемкостей газа (коэффициент Пуассона)
методом Клемана-Дезорма.
План подготовки конспекта:
1.Основные теоретические сведения
2.Выяснить, что измеряется в лабораторной работе, каким методом и для
чего.
2.Подготовить таблицу.
3.Записать расчётную формулу.
Вопросы для подготовки к входному тестированию:
1.Первое начало термодинамики.
2.Удельная теплоемкость. Связь между удельными теплоемкостями.
3.Молярная теплоемкость при постоянном объеме.
4.Молярная теплоемкость при постоянном давлении.
5.Почему Cp, больше Cv?
6.Какой процесс называется адиабатическим?
7.Что происходит с внутренней энергией газа и его температурой при адиабатическом расширении, при адиабатическом сжатии?
78

8.Чему равна внутренняя энергия газа?
9.В какой момент вашей работы происходит адиабатический процесс,
изохорический процесс, объясните на графике.
10.Почему кран открывается на короткий промежуток времени? 11.Какие значения принимает i для 1, 2 и 3 атомных газов.
12.Какое влияние на результат опыта окажет присутствие водяного пара.
Теоретические сведения
Любое состояние газа можно характеризовать тремя основными парамет-
рами: давлением (Р), объемом (V) и температурой (Т). Уравнение, которое свя-
зывает эти параметры, называется уравнением состояния газа. Таким уравнени-
ем для идеального газа является уравнение Менделеева – Клапейрона:
PV=nRT,
где n – число молей в объеме V.
Зная массу газа и его молекулярный вес , можно определить число молей n, содержащихся в этом объеме:
n m , тогда
PV |
m |
PT . |
(8.1) |
|
|||
|
|
|
|
Для одного моля n = 1 уравнение имеет вид:
PV=RT , (8.2)
где R – универсальная газовая постоянная, ее численное значение опреде-
ляется соотношением:
R= P0V0 ,
T0
где P0 = 1атм., V0 = 22,4 литра (это объем, занимаемый одним молем газа при Т0 = 2730 К).
В системе СИ R = 8,31.103 дж/кмоль градус. В калориях R 2
кал/моль градус.
Теплоемкость газа зависит от условий нагревания газа. Удельная теплоем-
79
кость газа c - количество тепла, которое необходимо подвести к единице массы вещества, чтобы повысить его температуру на один градус. Ее можно опреде-
лить, воспользовавшись выражением:
Q= сm Т, |
откуда с = |
Q |
. |
(8.3) |
|
||||
|
|
m T |
|
|
Молярная теплоемкость «C» - количество тепла, которое необходимо под-
вести к одному молю вещества, чтобы повысить его температуру на один гра-
дус. Она связана с удельной теплоемкостью соотношением:
С= с, |
С = |
|
|
Q |
. |
(8.4) |
m |
|
|||||
|
|
|
T |
|
||
Чтобы определить значение теплоемкости в разных процессах, воспользу-
емся первым началом термодинамики.
1-е начало термодинамики. Теплота, подводимая к газу, расходуется на увеличение внутренней энергии газа U и на работу совершаемую газом против внешних сил.
Q= U+A |
(8.5) |
||||
Внутренняя энергия идеального газа равна: |
|
||||
U = |
i |
|
m |
RT , |
(8.6) |
|
|
||||
|
2 |
|
|||
где i - число степеней свободы молекулы газа. Эта величина отражает ко-
личество координат характеризующих положение частицы в пространстве. Ее изменение равно
U = |
i |
|
m |
R T |
(8.7) |
|
|
||||
2 |
|
|
|
||
Внутренняя энергия газа изменяется при изменении температуры газа.
Элементарная работа, совершаемая газом, равна:
A=P V или dА=PdV (8.8)
В формулу, определяющую молярную теплоемкость (8.4), подставим вы-
ражение (8.5):
C= |
|
U |
|
A |
(8.9) |
||
|
|
|
|
|
|
||
m |
|
|
|||||
|
T |
|
T |
|
|||
80
