
- •Кинематика материальной точки. Системы отсчета. Траектория, перемещение, путь, скорость, ускорение. Равномерное и равнопеременное прямолинейные движения.
- •Криволинейное движение. Нормальное и тангенциальное ускорения.
- •Траектория, путь, перемещение, линейная скорость, линейное ускорение.
- •Частные случаи движения
- •Движение точки по окружности. Угловые перемещение, скорость, ускорение. Связь между линейными и угловыми характеристиками.
- •Угол поворота, угловая скорость, угловое ускорение.
- •Связь между линейными и угловыми характеристиками
- •Динамика материальной точки. Инерциальные системы отсчета и первый закон Ньютона
- •Первый закон Ньютона (закон инерции)
- •Фундаментальные взаимодействия. Силы различной природы (упругие, гравитационные, трения), второй закон Ньютона. Масса. Третий закон Ньютона.
- •Динамические характеристики поступательного движения
- •Импульс () векторная величина, равная произведению массы тела на его скорость, характеризует способность механического движения передаваться от одного тела к другому.
- •Импульс силы () векторная величина, численно равная произведению силы на время ее действия и совпадающая по направлению с направлением силы. Второй закон Ньютона
- •Главный вектор системы или равнодействующая (результирующая) сила; n количество сил. Третий закон Ньютона
- •Импульс системы материальных точек, уравнение движения центра масс. Закон сохранения импульса. Закон сохранения импульса для механической системы
- •3. Моментом импульса материальной точки относительно точки о называется векторное произведение радиуса-вектора материальной точки на ее импульс
- •Уравнение моментов
- •Закон сохранения момента импульса
- •Работа при вращательном движении
- •Мощность при поступательном и вращательном движении
- •Кинетическая энергия
- •Потенциальная энергия
- •Потенциальная энергия в поле сил тяжести
- •Потенциальная энергия в поле упругих сил
- •Закон сохранения механической энергии
- •9. Соударение тел. Упругое и неупругое взаимодействия
- •Абсолютно упругий центральный удар двух тел
- •Абсолютно неупругий центральный удар двух тел
- •Колебательное движение и его характеристики: смещение, амплитуда, фаза, циклическая частота, период, скорость, ускорение, сила, энергия
- •Кинематические и динамические характеристики свободных незатухающих колебаний
- •Векторные диаграммы для представления гармонических колебаний
- •Сложение параллельных колебаний одинаковой частоты. Биения.
- •Вынужденные колебания. Резонанс
- •14. Волновое движение. Уравнение плоской незатухающей бегущей волны. Энергия упругой волны. Вектор плотности потока энергии
- •Уравнение плоской бегущей волны
- •Фазовая скорость
- •Энергия упругой волны. Вектор Умова
- •Термодинамическая система. Параметры состояния термодинамической системы. Основные положения молекулярно - кинетической теории газов
- •Параметры состояния идеального газа
- •Молекулярно-кинетическая теория газов
- •16. Основное уравнение молекулярно-кинетической теории газов (уравнение Клаузиуса). Уравнение состояния идеального газа (Менделеева - Клапейрона) Уравнение Клаузиуса
- •Уравнение Менделеева - Клапейрона
- •Закон равномерного распределения энергии по степеням свободы молекул
- •Работа и теплота. Теплоемкость, ее виды
- •Виды теплоемкости
- •Первый закон термодинамики
- •Определение теплоемкостей Ср , сv
- •18. Основные термодинамические процессы идеального газа. Политропный процесс, его частные случаи: изобарный, изотермический, адиабатный, изохорный
- •Теплота в политропном процессе
- •Энтропия, второй закон термодинамики
Закон равномерного распределения энергии по степеням свободы молекул
Числом степеней свободы i материального объекта называется число независимых координат, однозначно определяющих положение этого объекта относительно рассматриваемой системы отсчета.
Рис. 2

|
Число атомов в молекуле |
1 |
2 |
3 |
|
Число степеней свободы i |
3 |
5 |
6 |
Закон равномерного распределения энергии по степеням свободы: энергия молекулы равномерно распределяется по степеням свободы, т.е. на каждую степень свободы, независимо от конструкции молекулы, приходится одинаковая энергия, равная kT/2.
Уравнение Клаузиуса
![]() ,
,
![]()
![]()
![]() (1)
(1)
Уравнение Менделеева
– Клапейрона
![]() (2)
(2)
![]()
![]()
![]()
![]()
![]()
![]() ;
;
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() (3)
(3)
Уравнение Клаузиуса было получено в предположении, что молекулы газа – материальные точки (одноатомные молекулы), имеющие 3 степени свободы поступательного движения. Так как все направления движения равновероятны, полная энергия молекулы поровну распределяется между тремя степенями свободы и на каждую степень свободы приходится kT/2 энергии
![]() .
(4)
.
(4)
Энергия одной
молекулы:
![]() .
.
Энергия одного
киломоля:
![]() .
.
Энергия произвольной
массы газа
![]() .
.
Работа и теплота. Теплоемкость, ее виды

Элементарная работа, совершаемая газом при перемещении поршня на отрезок dh,
![]() ,
(5)
,
(5)
Работа, совершаемая при конечном изменении объема газа от V1 до V2,
 .
(6)
.
(6)
Правило знаков
Если dV > 0, то dA > 0: система совершает работу над внешними телами – отдает им часть своей энергии.
Если dV < 0, то dA < 0: внешние тела совершают над системой работу – система получает энергию извне.

Графически работа изображается в координатах p и V (рабочая диаграмма) площадью, ограниченной кривой р = f (V) и двумя ординатами, соответствующими начальному V1 и конечному V2 объемам.
Передача тепловой энергии (теплоты) сопровождается изменением температуры тела. Для характеристики способности тел повышать свою температуру за счет полученного извне тепла вводится понятие теплоемкость.
Теплоемкость С – скалярная физическая величина, характеризующая связь между количеством сообщенного системе тепла и изменением ее температуры.
Виды теплоемкости
Полная теплоемкость Спол численно равна количеству тепла, которое необходимо сообщить системе, чтобы повысить ее температуру на один градус
![]()
![]() (7)
(7)
![]()
![]()
![]()
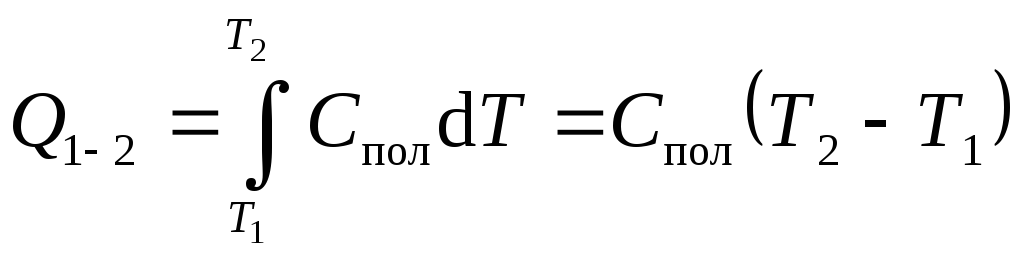 . (8)
. (8)
Молярная теплоемкость С численно равна количеству тепла, которую нужно сообщить одному киломолю вещества, чтобы повысить его температуру на один градус:
![]()
![]() (9)
(9)

![]()
![]()
![]() (10)
(10)
 В
зависимости от характера процесса
различают теплоемкости при постоянном
объемеСVи при постоянном
давленииСр.
В
зависимости от характера процесса
различают теплоемкости при постоянном
объемеСVи при постоянном
давленииСр.
![]() - уравнение
Майера
- уравнение
Майера
Первый закон термодинамики
Подобно тому, как в основе механики лежат законы Ньютона и все задачи могут быть решены с их помощью, так в основе термодинамики лежат два закона – два начала термодинамики.
Первое началотермодинамики утверждает тот факт, что в любых процессах должен соблюдаться закон сохранения и превращения энергии, т.е. первое начало представляет собой формулировку закона сохранения и превращения энергии применительно к тепловым процессам.
Второе начало уточняет первое и показывает направление протекания всех процессов – стремление любой системы к минимуму потенциальной энергии.
Рис. 6

![]() (11)
(11)
Тепло, подведенное к термодинамической системе, затрачивается на изменение ее внутренней энергии и на совершение системой работы над окружающими телами.

![]()
![]()
![]() , (12)
, (12)
в тепловых двигателях невозможно совершить работу, превышающую получаемую энергию, т.е. вечный двигатель 1-го рода невозможен.
