
- •Химия (Часть 1)
- •Введение
- •Техника лабораторных работ Порядок работы
- •Реактивы и обращение с ними
- •Меры предосторожности при работе в лаборатории
- •Лабораторная работа №1 Определение молярной массы эквивалента магния Краткие теоретические сведения
- •Количество вещества. Молярные массы
- •Молярный объем вещества.
- •Закон эквивалентов:
- •Экспериментальная часть
- •Условия и результаты опыта для расчета молярной массы эквивалентов магния
- •Давление насыщенного водяного пара при различных температурах
- •Расчет молярной массы эквивалентов магния
- •Вопросы для домашней подготовки
- •Упражнения
- •Лабораторная работа №2 Классы неорганических веществ Краткие теоретические сведения
- •Экспериментальная часть опыт №1. Идентификация кислот и оснований
- •Опыт №2. Реакция нейтрализации
- •Опыт №3. Получение средней и кислой солей
- •Опыт №4. Получение основной соли и гидроксида кобальта
- •Вопросы для домашней подготовки
- •Упражнения
- •Лабораторная работа №3 Скорость химических реакций и химическое равновесие Краткие теоретические сведения
- •Зависимость скорости реакции от концентрации. Гомогенные реакции
- •Гетерогенные реакции
- •Зависимость скорости реакции от температуры.
- •Химическое равновесие и принцип Ле Шателье
- •Экспериментальная часть Опыт № 1: Зависимость скорости гомогенной реакции от концентрации реагирующих веществ
- •Опыт № 2. Зависимость скорости гетерогенной реакции от величины активной поверхности реагирующих веществ
- •Опыт № 3 Смещение химического равновесия при изменении концентрации реагирующих веществ
- •Вопросы для домашней подготовки
- •Упражнения
- •Литература
Экспериментальная часть
Реактивы и оборудование
1. Раствор соляной кислоты, 10 %.
2. Навеска магния.
3. Прибор для вытеснения водорода из кислоты.
Выполнение опыта
Опыт проводится
на приборе для определения объема
вытесненного водорода из кислоты
металлом. Прибор (рис. 1) состоит из двух
бюреток 2 и 3, соединенных между собой
резиновой трубкой. Бюретки заполнены
подкрашенной водой приблизительно до
половины их объема.
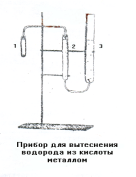
Рис. 1.Прибор для измерения объема газа
Верхний открытый конец левой бюретки 2 с помощью газоотводной стеклянной трубки и двух резиновых пробок соединен с пробиркой 1, в которой будет проводиться реакция взаимодействия магния с соляной кислотой.
Порядок выполнения опыта
1. Проверьте прибор на герметичность. Для этого опустите правую бюретку 3 на 15-20 см и наблюдайте за положением воды в левой бюретке. Если прибор герметичен, то уровень в ней не изменится.
2.Убедившись в герметичности прибора, закрепите бюретки таким образом, чтобы уровень воды в левой бюретке был на нулевом делении (по нижнему мениску).
3. В пробирку налейте 3-4 мл 10%-ного раствора соляной кислоты. Держа пробирку наклонно, осторожно положите в нее навеску магния, (заранее взвешенную и завернутую в папиросную бумагу) так, чтобы он не упал в кислоту. Затем соедините пробирку с левой бюреткой и резко переведите в вертикальное положение, чтобы навеска с магнием упала в соляную кислоту. Наблюдайте бурную реакцию взаимодействия магния с соляной кислотой и выделение газообразного водорода.
Mg+2HCl=MgCl2+H2
Проследите, чтобы вся навеска магния прореагировала с кислотой.
4. После окончания реакции дайте пробирке остыть. Затем, опуская правую бюретку, приведите воду в обеих бюретках к одинаковому уровню, чтобы создать в левой бюретке давление, равное атмосферному.
По положению нижнего мениска воды в левой бюретке определите объем выделившегося водорода V1.
Определите температуру проведения опыта t термометром, и величину атмосферного давления по показанию барометра.
Запишите условия опыта и результаты в табл. 1 .
Таблица 1
Условия и результаты опыта для расчета молярной массы эквивалентов магния
|
№ п/п |
Экспериментальные данные |
Ед. измерения |
Обозначения |
Результаты измерений и вычислений |
|
|
|
|
|
|
|
1 |
Масса метала |
г |
m |
|
|
2 |
Объём выделившегося водорода |
мл |
V1 |
|
|
3 |
Температура |
0С |
t |
|
|
4 |
Абсолютная температура |
К |
T1 = 273 + t |
|
|
5 |
Атмосферное давление |
мм. рт. ст. |
p |
|
|
6 |
Давление насыщенного водяного пара при данной температуре h (табл. 2) |
мм. рт. ст. |
h |
|
|
7 |
Парциальное давление водорода |
мм. рт. ст |
p1 = p - h |
|
Примечание. Так как в проведенном опыте водород собирается над поверхностью воды, то давление в левой бюретке, равное атмосферному, складывается из давления водорода и водяного пара. Величину давления водяного пара, зависящего от температуры, определите по из таблице 2.
Таблица 2
