
- •А. В. Скворцов
- •Галоген- и кислородсодержащие соединения
- •Оглавление
- •Введение функциональные производные углеводородов
- •Глава 7. Галогенопроизводные углеводородов
- •7.1. Номенклатура. Изомерия
- •7.2. Физические свойства
- •7.3. Химические свойства
- •7.3.1. Реакции замещения
- •7.3.2. Реакции отщепления
- •7.3.3. Восстановление галогенидов водородом
- •7.3.4. Образование металлоорганических соединений
- •7.4. Получение
- •7.5. Специфика фторопроизводных
- •7.6. Использование галогенопроизводных
- •Глава 8. Оксипроизводные углеводородов (спирты и фенолы)
- •8.1. Спирты одноатомные (алкоголи)
- •8.1.1. Изомерия и номенклатура
- •8.1.2. Физические свойства
- •Физические свойства спиртов
- •8.1.3. Химические свойства
- •Б. Реакции, протекающие с разрывом связи с–он
- •В. Реакции спиртов с участием их радикалов
- •8.1.4. Получение спиртов
- •8.1.5. Использование спиртов
- •8.2. Многоатомные спирты (полиолы)
- •8.2.1. Изомерия и номенклатура
- •8.2.2. Свойства полиолов
- •8.2.3. Получение и применение полиолов
- •8.3. Фенолы и нафтолы
- •8.3.1. Физические свойства
- •Физические свойства фенолов
- •8.3.2. Химические свойства
- •8.3.3. Получение и применение
- •Глава 9. Простые эфиры
- •9.1. Изомерия и номенклатура
- •9.2. Получение
- •9.3. Свойства простых эфиров
- •9.4. Эпоксиды (органические оксиды)
- •9.5. Использование простых эфиров
- •Глава 10. Альдегиды и кетоны – оксопроизводные углеводородов
- •10.1. Предельные альдегиды и кетоны
- •10.1.1. Физические свойства
- •Физические свойства альдегидов и кетонов
- •10.1.2. Химические свойства
- •I. Реакция присоединения
- •1. С цианистым водородом
- •2. Со спиртами (образование полуацеталей, ацеталей и кеталей):
- •3. С бисульфитом натрия (NaHso3)
- •4. Присоединение аммиака
- •II. Замещение карбонильного кислорода
- •7. Замещение карбонильного кислорода хлором
- •III. Реакции с участием атомов водорода в -положении
- •8. Галогенирование радикалов оксосоединений
- •9. Альдольно-кротоновая конденсация
- •10. Конденсация с алкинами-1 (синтезы Фаворского)
- •15. Диспропорционирование альдегидов
- •V. Реакции олиго- и полиМеРизации
- •10.2. Непредельные оксосоединения
- •10.2.1. Сопряженные (, -ненасыщенные)
- •4. Оксид серебра окисляет только альдегидную группу
- •10.2.2. Кетены (карбонилы с кумулированными связями
- •10.3. Дикарбонильные соединения
- •10.4. Получение оксосоединений
- •10.5. Применение оксосоединений
- •Глава 11. Карбоновые кислоты и их производные
- •11.1. Одноосновные предельные кислоты
- •11.1.1. Физические свойства
- •Физические свойства некоторых одноосновных карбоновых кислот
- •11.1.2. Химические свойства
- •11.1.3. Способы получения
- •11.2. Одноосновные непредельные кислоты
- •11.2.1. Свойства непредельных кислот
- •11.2.2. Получение непредельных кислот
- •11.3. Двухосновные кислоты
- •11.3.1. Свойства диовых кислот
- •11.3.2. Получение двухосновных кислот
- •11.4. Функциональные производные
- •11.4.1. Галогенангидриды
- •11.4.2. Ангидриды карбоновых кислот
- •11.4.3. Сложные эфиры органических
- •11.5. Применение карбоновых кислот
- •Глава 12. Номенклатура гетерофункциональных органических соединений
- •Глава 13. Оксикислоты (спиртокислоты)
- •13.1. Хиральность. Оптическая изомерия
- •13.2. Свойства оксикислот
- •13.3. Получение и применение оксикислот
- •Глава 14. Оксокислоты (альдегидо-
- •14.1. Получение и свойства
- •14.2. Ацетоуксусный эфир и таутомерия
- •Краткое руководство для студентов к решению задач
- •3. Отщепление:
- •IV. Правила реагирования органических соединений.
- •V. Некоторые именные реакции.
- •4. Вильямсона синтезы
- •9. Синтезы Гриньяра:
- •VI. Стандартные приемы получения функциональных групп различных классов органических соединений.
- •3. Получение группы (-он) спиртов.
- •4. Получение фенолов.
- •5 .. Получение оксогрупп
- •6. Получение карбоксилов (соон).
- •7. Реакции между Ме- и Hal-производными (синтезы Вильям-сона).
- •9. Дегидратация «длинных» диовых кислот.
- •VII. Виды заданий и последовательность их выполнения.
- •Андрей Вениаминович Скворцов
8.1.5. Использование спиртов
В наибольших объемах в пищевой промышленности используется этанол (спирт-ректификат) – для изготовления различных спиртных напитков.
Бензиловый спирт (C6H5–CH2OH) – компонент ароматообразующих веществ пшеничного хлеба. Изоамиловый спирт (3-метилбутанол-1) является исходным для получения уксусноизоамилового эфира («грушевая эссенция)», используемого в приготовлении конфет, фрукто- вых вод.
Все спирты как высоко реакционноспособные вещества являются исходными для получения самых разнообразных химических продуктов: альдегидов, кетонов и карбоновых кислот; галогенопроизводных и непредельных углеводородов; каучуков и пластмасс и др. Являются хорошими растворителями многих органических веществ. Широко используются в парфюмерной промышленности. Так, 2-фенил-этанол (C6H5–CH2–CH2–OH) является главной составной частью «розового масла» – стабилизатора запахов, непременного компонента духов.
8.2. Многоатомные спирты (полиолы)
Многоатомными называются спирты, содержащие в молекуле больше одной оксигруппы. С одним атомом углерода может быть связана не более чем одна оксигруппа. Геминальные полиолы неустойчивы. В момент образования они, за редким исключением*, отщепляют воду, превращаясь в альдегиды (а), кетоны (б) или карбоновые кислоты (в)
а) б) в) 1,1-дибромалкан – – 2,2-дибромалкан 1,1,1-трибромалкан – –
8.2.1. Изомерия и номенклатура
Изомерия многоатомных спиртов обусловлена изменениями структуры С-скелета и различным положением оксигрупп.
Некоторые полиолы имеют тривиальные названия (этиленгликоль, глицерин, инозит и др.). Двухатомные спирты называются гликолями. Гликоли с оксигруппами у соседних углеродов называют -гликолями;
в -гликолях эти углероды разделены одной метиленовой группой,
––––––––––––––––––––––––––
*![]()
![]() (кристаллич.
вещество)
(кристаллич.
вещество)
хлораль хлоральгидрат (Т пл. = 51,7)
в -гликолях – двумя метиленовыми группами:
![]()
![]()
![]()
бутандиол-2,3 бутандиол-1,4 2-метилпропандиол-1,3
(-гликоль) (-гликоль) (-гликоль)
Диолы различных структур являются основой диольных липидов.
![]()
![]()

этиленгликоль глицерин инозит
этандиол-1,2 пропантриол-1,2,3 гексаоксициклогексан
8.2.2. Свойства полиолов
Важнейшими из многоатомных спиртов являются этиленгликоль и глицерин. Это вязкие, сладкие на вкус жидкости, тяжелее воды, хорошо растворимые в воде, в низших спиртах, в ацетоне, но не растворимые в жирах, бензоле, бензине. Кипят при гораздо более высоких температурах, чем одноатомные спирты с соответствующим числом атомов углерода, за счет дополнительных водородных связей (табл. 12).
Высшие полиолы (тетриты, пентиты, гекситы и др.) – бесцветные кристаллы сладкого вкуса, хорошо растворимые в воде.
По химическим свойствам гликоли и глицерины похожи на одноатомные спирты. Отличия: повышенная подвижность атомов водорода оксигрупп и возможность участия в реакциях как одной, так и нескольких оксигрупп.
1. Алкоголяты образуются при взаимодействии не только со щелочными металлами, но и со щелочами и даже с гидроксидами тяжелых металлов
 гликолят меди
гликолят меди
(внутрикомплексное соединение)
Реакция растворения осадка гидроксида меди (II) сопровождается ярким внешним эффектом (образуется синий раствор) и является качественной на многоатомные спирты.
2. Сложные эфиры легко образуются и с органическими, и с неорганическими кислотами
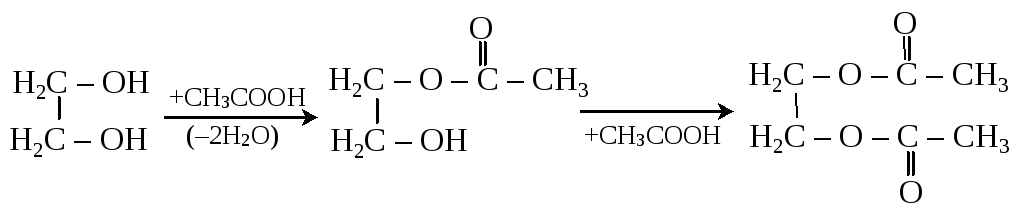
этиленгликоль неполный эфир полный эфир

глицерин тринитроглицерин
3. Окисление протекает легко. Могут образовываться различные продукты
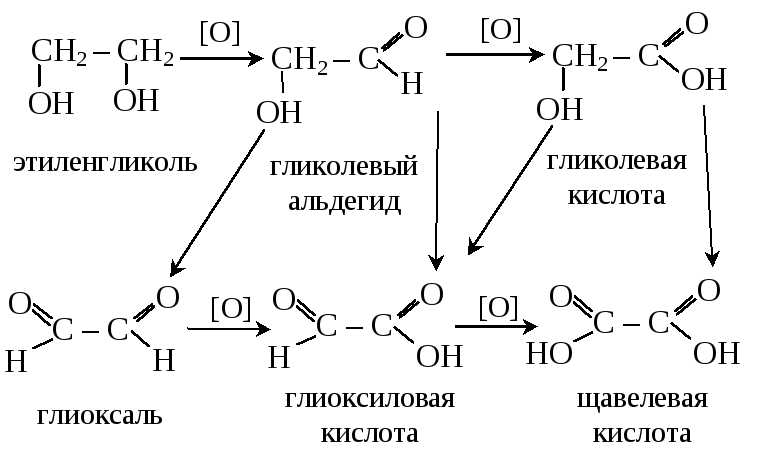
4. Дегидратация протекает по-разному в зависимости от условий реакции и строения исходного спирта:
(а) из -гликолей получаются эпоксиды
;
(б) из -гликолей – непредельные спирты
![]()
пропандиол-1,3 аллиловый спирт
(в) -гликоли образуют циклические эфиры

бутандиол-1,4 тетрагидрофуран
