
- •Госсударственная корпорация по атомной энергии «росатом»
- •1.Введение
- •2.Открытие фосфора.
- •3.Фосфор в природе
- •4.Фосфорные удобрения
- •5. Двойной суперфосфат
- •Состав монокальцийфосфата
- •6. Химизм процесса
- •1320 – Плотность кислоты, кг/м3
- •210 И 1,33 – выход суперфосфата и количество гипса, поступающего с фосфорной кислотой.
2.Открытие фосфора.
История открытия химических элементов полна личных драм, различных неожиданностей, таинственных загадок и удивительных легенд. Успех оказывался верным спутником тех, кто умел пристально всматриваться в природные явления.
Древние фолианты сохранили для нас отдельные эпизоды из жизни отставного солдата и гамбургского купца. Звали его Хенниг Бранд (1630-?). Его купеческие дела шли не блестяще, и именно по этой причине он стремился выбраться из нищеты. Она его ужасно угнетала. И Бранд решил попытать счастья в алхимии. Тем более что в XVII веке считалось вполне возможным найти «философский камень», который способен превращать неблагородные металлы в золото.
Бранд провел уже множество опытов с различными веществами, но ничего дельного у него не получалось. Однажды он решил провести химический эксперимент с мочой. Выпарил ее почти досуха и оставшийся светло-желтый осадок смешал с углем и песком, нагревая в реторте без доступа воздуха. В результате Бранд получил новое вещество, которое обладало удивительным свойством – светиться в темноте. Так в 1669 г. был открыт фосфор, играющий исключительно важную роль в живой природе: в растительном мире, в организме животных и человека. Счастливый ученый не замедлил воспользоваться необычным свойством нового вещества и стал демонстрировать светящийся фосфор знатным особам за довольно высокое вознаграждение. Все, что соприкасалось с фосфором, приобретало способность светиться. Достаточно было помазать фосфором пальцы, волосы или предметы, и они вспыхивали таинственным голубовато-белым светом. Религиозно и мистически настроенные богатые люди того времени диву давались, смотря на различные манипуляции Бранда с этим «божественным» веществом. Он ловко использовал огромный интерес ученых и широкой публики к фосфору и стал продавать его по цене, превосходившей даже стоимость золота. X. Бранд производил фосфор в больших количествах и держал способ его получения в строжайшей тайне. Никто из других алхимиков не мог проникнуть в его лабораторию, и поэтому многие из них стали лихорадочно ставить различные опыты, стремясь раскрыть секрет изготовления фосфора.
В 1680г. секрет получения фосфора был открыт в Англии знаменитым химиком Р. Бойлем. После смерти Р. Бойля его ученик немец А. Ганквиц, улучшив методику получения фосфора, наладил его производство и даже попытался изготовить первые спички. Он снабжал фосфором научные учреждения Европы и отдельных лиц, желающих приобрести его. Для расширения торговых связей А. Ганквиц посетил Голландию, Францию, Италию и Германию, заключая новые договора на продажу фосфора. В Лондоне им была основана фармацевтическая фирма, получившая широкую известность.
Лишь столетие спустя после обнаружения фосфора он перешел из мира торговли и наживы в мир науки.
3.Фосфор в природе
Фосфор по своей важности ничуть не уступает азоту. Он участвует в великом природном круговороте веществ, и, не будь фосфора, растительный и животный мир был бы совсем иным. Однако фосфор встречается в природных условиях не так уж часто, в основном в виде минералов, и на его долю приходится 0,08% массы земной коры. По распространенности он занимает тринадцатое место среди других элементов. Интересно отметить, что в теле человека на долю фосфора приходится примерно 1,16%. Из них 0,75% уходит на костную ткань, около 0,25% – на мышечную и примерно 0,15% – на нервную ткань. Фосфор редко встречается в больших количествах, и в целом его следует отнести к рассеянным элементам. В свободном виде в природе он не обнаружен, так как обладает очень важным свойством – легко окисляется, но содержится во многих минералах, число которых уже составляет 190. Главнейшие из них - фторапатит, гидроксилапатит, фосфорит. Несколько реже встречаются вивианит, монацит, амблигонит, трифилит и совсем в ограниченных количествах - ксенотит и торбернит.
Что касается минералов фосфора, то они делятся на первичные и вторичные. Среди первичных наиболее распространены апатиты, представляющие в основном породы магматического происхождения. Химический состав апатита - фосфат кальция, содержащий некоторое количество фторида и хлорида кальция. Кроме того, они содержат от 5 до 36% Р2О5. Обычно эти минералы в большинстве случаев встречаются в зоне магмы, но нередко они обнаруживаются в местах, где изверженные породы соприкасаются с осадочными. Из всех известных месторождений фосфатов наиболее значительные имеются в Норвегии и Бразилии. Крупное отечественное месторождение апатитов открыто академиком А. Е. Ферсманом в Хибинах в 1925 г. «Апатит в основном соединение фосфорной кислоты и кальция, – писал А. Е. Ферсман. –Внешний вид этого минерала так разнообразен и странен, что старые минералоги назвали его апатитом, что значит по-гречески «обманщик». То это прозрачные кристаллики, до мелочей напоминающие берилл или даже кварц, то это плотные массы, неотличимые от простого известняка, то это радиально-лучистые шары, то порода зернистая и блестящая, как крупнозернистый мрамор».
Апатиты в результате действия процессов выветривания, жизнедеятельности бактерий, разрушения различными почвенными кислотами переходят в формы, легко потребляемые растениями, и таким образом вовлекаются в биохимический круговорот. Следует отметить, что фосфор усваивается только из растворенных солей фосфорной кислоты. Однако фосфор из почвы частично вымывается, а большое количество его, поглощенное растениями, не возвращается обратно в почву и уносится вместе с урожаем. Все это приводит к постепенному истощению почвы. При внесении в почву фосфорных удобрений урожайность увеличивается.
Несмотря на значительные потребности в фосфорных удобрениях, особых опасений, связанных с истощением запасов сырья, для их производства, по всей видимости, нет. Эти удобрения могут быть получены при комплексной переработке минерального сырья, донных морских отложений и различных геологических пород, богатых фосфором. При разложении богатых фосфором соединений органического происхождения нередко образуются газообразные и жидкие вещества. Иногда можно наблюдать выделение газа с запахом гнилой рыбы – фосфористого водорода, или фосфина, РН3. Одновременно с фосфином идет образование другого продукта – дифосфина, Р2Н4, представляющего собой жидкость. Пары дифосфина самовоспламеняются и поджигают газообразный фосфин.
Фосфин и дифосфин в природе встречаются довольно редко, и чаще приходится иметь дело с такими соединениями фосфора, как фосфориты. Это вторичные минералы-фосфаты органического происхождения, играют особо важную роль в сельском хозяйстве. На островах Тихого океана, в Чили и Перу они образовались на основе птичьего помета – гуано, который в условиях сухого климата накапливается мощными слоями, нередко превышающими сотню метров.
Образование фосфоритов может быть связано и с геологическими катастрофами, например с ледниковым периодом, когда гибель животных носила массовый характер. Подобные процессы возможны и в океане при массовой гибели морской фауны. Быстрое изменение гидрологических условий, которое может быть связано с различными процессами горообразования, в частности с действием подводных вулканов, несомненно, в отдельных случаях приводит к смерти морских животных. Фосфор из органических остатков частично усваивается растениями, но в основном, растворяясь в морской воде, переходит в минеральные формы. Морская вода содержит фосфаты в довольно больших количествах – 100-200 мг/м3. При определенных химических процессах в морской воде фосфаты могут выпадать в осадок и скапливаться на дне. А при поднятии морского дна в различные геологические периоды залежи фосфоритов оказываются на суше. Подобным образом могло образоваться крупное отечественное месторождение фосфоритов вблизи Кара-Тау в Казахстане. Встречаются фосфориты и в Подмосковье.
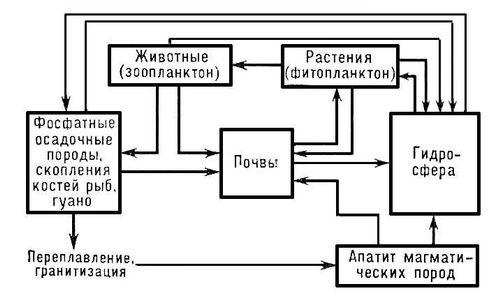
Рис. 1 Круговорот фосфора в природе
