
- •Лекція 1. Окновні поняття теорії систем і моделювання
- •2.2 Технологічний регламент і матеріальний баланс
- •2.3 Розрахунок матеріальних балансів лінійних процесів
- •2.4 Спрощений спосіб розрахунків лінійних балансів
- •2.5. Укладання матеріальних балансів для процесів з рециклами
- •Лекція 14. Основи хімічної кінетики Мета лекції
- •Зміст лекції
- •14.1 Поняття динамічної моделі. Мікро і макрокінетика
- •14.2 Швидкість хімічної реакції
- •14.3 Моделювання мікрокінетики хімічних реакцій. Пряма й зворотна задача
- •14.4 Метод а.А.Баландіна
- •14.5 Інтегральний метод встановлення порядку реакцій
- •Контрольні запитання
- •Завдання для самостійної роботи
- •Перелік рекомендованої літератури
2.3 Розрахунок матеріальних балансів лінійних процесів
Проілюструємо розрахунок матеріального балансу лінійного процесу на наступному прикладі. По описанню характеристик процесу (інформаційної моделі процесу) побудувати матеріальний баланс процесу отримання сульфату амонію.
Процес містить такі стадії:
а) нейтралізація - взаємодія 10 %-ного водного розчину сірчаної кислоти з еквімолярною кількістю 25 %-ного розчину аміаку (аміачною водою):
H2SO4+ NH3= (NH4)2SO4. (2.7)
Вихід по стадії:100 %
б) сушка розчину сульфату амонію з утворенням технічного продукту, що містить 99 % сульфату амонію і 1 % води. Втрати технічного сульфату амонію складають 1 % по масі.
Густина 10 %-ного розчину сірчаної кислоти складає 1052 кг/м3; густина 25 %-ного розчину аміаку: 910 кг/м3.
Побудову матеріального балансу починаємо з побудови блок-схеми матеріальних потоків системи. Її зображено на рис. 2.1
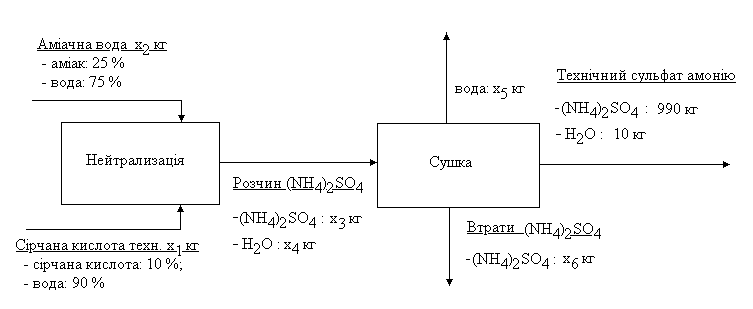
Рисунок 2.1 – Схема матеріальних потоків
На схемі помістимо склад кожного з технічних продуктів. В разі, коли вміст речовини є невідомим, позначаємо за х з відповідним індексом кількість речовини в кг, що приводить до 1000 кг технічного продукту. Оскільки склад кінцевого продукту є відомим, одразу розраховуємо кількість вихідних речовин у складі 1000 кг технічного сульфату амонію:
- сульфату амонію 100 % : 100099 % = 990 кг;
- води: 10001% = 10 кг.
Як випливає зі схеми, матеріальний баланс є лінійним, оскільки на схемі немає циклів.
Виходячи зі схеми, наявні 6 невідомих величин, тому для розрахунків ми повинні скласти 6 рівнянь. Ці рівняння можуть відображати:
- закони збереження при перебігу хімічних реакцій;
- закони збереження при перебігу процесів перерозподілу речовин у фізико-хімічних процесах (без хімічних перетворень).
Побудуємо баланс по стадії нейтралізації:
а) молярні маси речовин складають:
Н2SO4– 98;
NH3– 17;
(NH4)2SO4– 132;
б) розрахуємо взаємозв’язок між кількостями сірчаної кислоти та аміаку.З інформаційної моделі процесу в нього уводять еквімолярні кількості сірчаної кислоти і аміаку, тобто, підтримуючи співвідношення їх молів 1 : 2.
Зі схеми (рис. 2.1): кількість кілограмів 100 %-ної сірчаної кислоти складає 0,1х1; кількість кг-моль буде: 0,1х1/98;
Кількість кілограмів 100 %-ного аміаку складає 0,25х2; кількість кг-моль буде: 0,25х2/17;
Співвідношення молів:
![]() ,
(2.8)
,
(2.8)
Після приведення подібних у (2.2) отримуємо перше рівняння системи:
![]() ;
(2.9)
;
(2.9)
в) знайдемо кількість сульфату амонію, що створюється у відповідності з рівнянням (2.1) в умовах процесу. У відповідності з ним з 1 моля сірчаної кислоти створюються 1 моль сульфату амонію. Звідси кількість кілограмів сульфату амонію, що утворилось ( х3на схемі на рис.2.1), складає:
![]() (2.10)
(2.10)
Після приведення подібних отримуємо друге рівняння системи:
![]() ;
(2.11)
;
(2.11)
г) Підрахуємо, скільки води стало на виході зі стадії нейтралізації. Оскільки вода в реакції (2.1) не утворюється, кількість кілограмів води (х4) дорівнює сумі кількостей води з технічної сірчаної кислоти (0,9х1) і з аміаку (0,75х3). Звіди отримаємо третє рівняння системи:
0,9х1+ 0,75х2- х4= 0. (2.12)
Побудуємо баланс по стадії сушки:
а) кількість води, що поступило на стадію сушки (х4) дорівнює кількості води, що вийшла з усіма продуктами: водою, що випарена (х5, рис. 2.1) і водою, що міститься у складі сульфату амонію ( 10 кг):
х4= х5+ 10, (2.13)
звідси четверте рівняння системи:
х4- х5= 10; (2.14)
б) кількість сульфату амонію, що поступило на стадію сушки (х3) дорівнює сумі мас втрат (х6) і сульфату амонію в складі технічного продукту (990 кг):
х3= х6+990, (2.15)
звідси п’яте рівняння системи:
х3- х6= 990; (2.16)
в) з інформаційної моделі кількість втрат сульфату амонію (100 %)дорівнює 1 % від кількості, що створюється, тобто: х6/х3= 0.01, або:
0,01х3– х6= 0. (2.17)
Поєднаємо рівняння (2.3), (2,5), 2,6), (2,8), (2,10) і (2,11) , отримаємо систему лінійних рівнянь (2.12):
 (2.18)
(2.18)
Складемо розширену матрицю системи:
|
х1 |
х2 |
х3 |
х4 |
х5 |
х6 |
В | |
|
1 |
3,4 |
-24,5 |
0 |
0 |
0 |
0 |
0 |
|
2 |
13,2 |
0 |
-98 |
0 |
0 |
0 |
0 |
|
3 |
0,9 |
0,75 |
0 |
-1 |
0 |
0 |
0 |
|
4 |
0 |
0 |
0 |
1 |
-1 |
0 |
10 |
|
5 |
0 |
0 |
1 |
0 |
0 |
-1 |
990 |
|
6 |
0 |
0 |
0,01 |
0 |
0 |
-1 |
0 |
Розв’язок системи (2.18):
|
х1 |
7424,242 |
|
х2 |
1030,303 |
|
х3 |
1000 |
|
х4 |
7454,545 |
|
х5 |
7444,545 |
|
х6 |
10 |
Підставивши ці величини у таблиці матеріального балансу й виконав необхідні розрахунки, отримаємо таблицю матеріального балансу (табл. 2.4).
Дані по густині розчинів були одержані з довідкової літератури, зокрема із «Довідника хіміка». Значення густини для розчину сульфату амонію були отримані шляхом інтерполяції значень між густинами 10 і 12 % розчинів.
При представленні результатів розрахунків матеріального балансу прийнято округляти:
- масові долі – до 2 цифр після коми;
- маси – до 2 цифр після коми;
- кількість кмоль – до 4-5 цифр після коми;
- об’єм – до 3 цифр після коми.
