
- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Вопросы и упражнения
3.8.3. Способы получения
Нитроалканы получают нитрованием алканов, нуклеофильным замещением галогена в галогеналканах или окислением других азотсодержащих соединений.
Нитрование алканов рассмотрено подробно в свойствах алканов (гл. 2.4.1). Жидкофазное и парофазное нитрование алканов применяется в промышленности. Объём мирового производства важнейших алифатических нитросоединений — десятки тысяч тонн.
Замещение атома галогена при взаимодействии галогеналканов с неорганическими нитритами — типичное нуклеофильное замещение в молекулах галогеналканов — гл. 3.2.2.1.
Окисление аминов (гл. 3.7.3.7) также может быть использовано для получения нитроалканов. Однако для получения геминальных ди- и тринитросоединений нашёл применение способ окисления оксимов:
![]()
3.8.4. Физиологическое действие и Важнейшие представители
Нитроалканы обладают сильным местным раздражающим действием и являются токсичными веществами. Они относятся к клеточным ядам общего действия и особенно опасны для печени. Хлорированные и непредельные в 5—10 раз токсичнее.
Нитрометан — бесцветная жидкость, малорастворим в воде; температура кипения 357 К. Ядовит. В промышленности получают парофазным нитрованием пропана.
Используется в качестве растворителя и как исходное вещество для дальнейших синтезов.
3.9. Кремний-, фосфор- и мышьякорганические соединения
Органические соединения кремния, фосфора, мышьяка и других элементов относятся к элементорганическим соединениям. Здесь рассмотрены только некоторые из них.
3.9.1. Кремнийорганические соединения
Кремний и углерод расположены в одной группе Периодической таблицы. По сравнению с углеродом кремний менее электроотрицателен, он не образует многих типов соединений, известных для углерода. Кратные связи Si=Si, Si=C, Si=O, Si=S для него неизвестны. Атомы кремния могут соединяться между собой, образуя цепи небольшой длины, но связиSi–Si чрезвычайно непрочны и легко могут претерпевать как гомолитическое, так и гетеролитическое расщепление.
Все кремнийорганические соединения могут быть представлены в виде следующих групп веществ:
замещённые силаны, например:
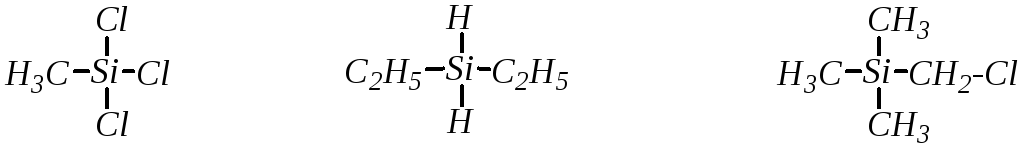
метилтрихлорсилан диэтилсилан хлорметилтриметилсилан
органосилоксаны— соединения, включающие структурный фрагментSi–O–Si, например,

гексаметилдисилоксан диметилполисилоксан
органосилазаны— соединения, имеющие связиSi–N–Si, например:
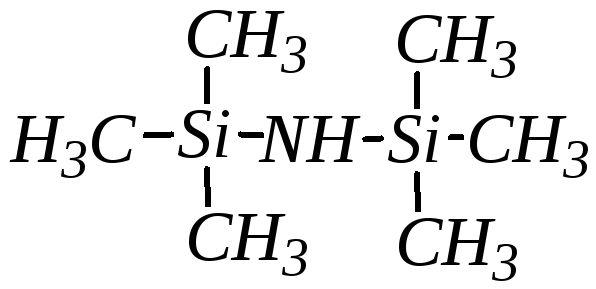
и другие.
Кремнийорганические соединения являются бесцветными жидкостями, реже — кристаллическими веществами. Обычно они не имеют запаха, не растворяются в воде.
В молекулах алкилсиланов атом кремния является электронодонорным заместителем, и на атоме углерода, связанном с кремнием, возникает частичный отрицательный заряд.
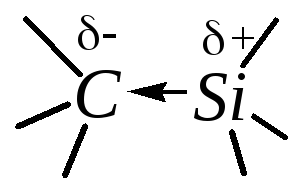
Поэтому алкилсиланы отличаются от рассмотренных ранее производных алканов распределением электронной плотности в молекулах и, конечно же, химическим поведением. Результатом этого является химическая инертность этих соединений по отношению к большинству реагентов в обычных условиях. В этом алкилсиланы обнаруживают большое сходство с углеводородами.
Связь Si–Clсильнополярна, и поэтому алкилхлорсиланы легко реагируют с водой, спиртами, аминами, металлорганическими соединениями и другими основными реагентами. Гидролиз протекает энергично, причём образующиеся силанолы нестойки, легко теряют воду и образуют силоксаны. Например:
2(CH3)3Si-Cl
+2H2O
![]() 2(CH3)3Si-OH
(CH3)3Si-O-Si(CH3)3
+ H2O
2(CH3)3Si-OH
(CH3)3Si-O-Si(CH3)3
+ H2O
триметилхлорсилан триметилсиланол гексаметилдисилоксан
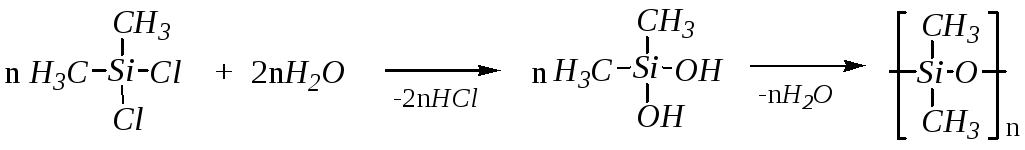
диметилдихлорсилан диметилсиландиол диметилполисилоксан
Алкоголиз хлорсиланов приводит к алкоксисиланам, аминолиз — к силазанам, а взаимодействие с реактивами Гриньяра — к алкилсиланам. Например:

Некоторые особенности имеет нуклеофильное замещение атома галогена в галогенометилтриалкилсиланах
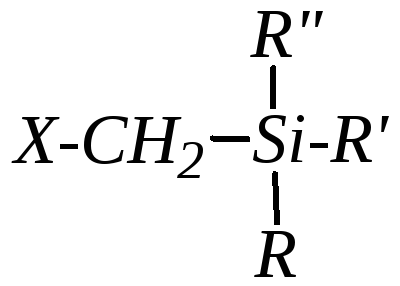
Эти реакции наиболее полно изучены для тех случаев, в которых замещаемой группой Х является атом хлора. Схема реакции для этих соединений, например, при взаимодействии с вторичными аминами, такая же, как и в общем случае:
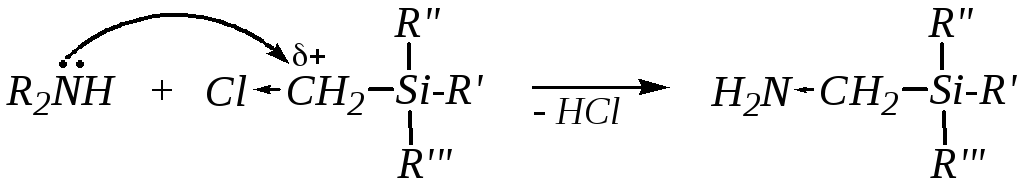
хлорметилтриалкилсилан
Механизм реакции здесь, как и следовало ожидать, близок механизму бимолекулярного замещения, но первоначальная атака нуклеофила происходит по атому кремния, и образование переходного состояния происходит не сразу, а через промежуточный комплекс, который затем претерпевает перегруппировку с переносом реакционного центра на атом углерода:
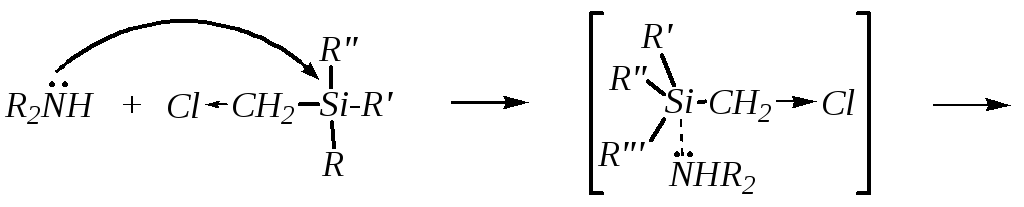
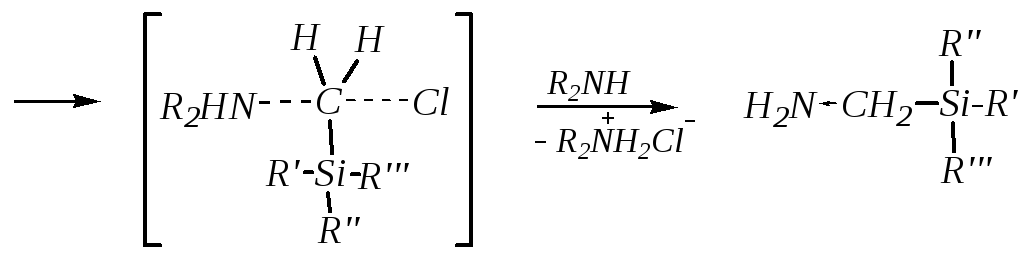
Координационная связь силанов с нуклеофилом осуществляется за счёт вакантных d-орбиталей кремния и наиболее вероятна для соединений, содержащих небольшие по объему алкильные (и алкоксильные) заместители у кремния (-CH3, -C2H5, -OCH3, -OC2H5). При этом промежуточный комплекс нуклеофила с кремнием образуется быстро, а лимитирующей стадией является его перегруппировка и превращение в продукты реакции. Из-за образования этого комплекса реакция нуклеофилов с низшими хлорметилсиланами протекает почти в 10 раз быстрее, чем с соответствующими углеродными аналогами, и ускоряется электроноакцепторными заместителями у атома кремния, способствующими образованию этого комплекса. Однако наличие двух и трёх алкоксильных групп у кремния приводит к значительному увеличению электронной плотности на нём, вызванному положительными мезомерными эффектами алкоксигрупп за счёт взаимодействия неподелённых электронных пар кислорода с вакантными орбиталями кремния, и электростатическому отталкиванию молекул нуклеофила атомами кислорода заместителей. Поэтому скорость взаимодействия с нуклеофилом ди- и триалкоксихлорметилсиланов почти не отличается от скорости аминирования моноалкоксихлорметилсиланов.
Из всех кремнийорганических соединений наиболее широкое применение получили полисилоксаны. Они представляют собой бесцветные вязкие жидкости или эластичные массы. Они термически и химически очень стабильны. Полисилоксаны («силиконы») используют в качестве смазочных масел, каучуков (силиконовые эластомеры), тормозных жидкостей и др. Резины на основе кремнийорганических каучуков применяются преимущественно как электроизоляционные материалы, и благодаря биоинертности, тромборезистентности и хорошей тканесовместимости их используют в медицине для изготовления различных эндопротезов (суставов, мягких тканей) длительного пользования.
